
Lägesbild av den nationella cancerstrategin
Kartläggning av styrkor och utvecklingsbehov
Förord
Sedan 2009 har det funnits en nationell cancerstrategi, som legat till grund för många insatser på olika nivåer, för att förbättra cancervården. Myndigheten för vård- och omsorgsanalys har på regeringens uppdrag tagit fram en lägesbild över den nationella cancerstrategin ur ett patient-, verksamhets- och systemperspektiv.
Vi vill rikta ett varmt tack till alla som tagit sig tid att delta i våra intervjuer, svara på våra enkäter och till alla som bidragit till arbetet på andra sätt. Arbetet med promemorian har gjorts av utredaren Kajsa Hanspers, analytikern Annasara Agfors och utredaren Daniel Zetterberg. I arbetet har även praktikanten Julia Belcastro, juristen Ellen Ringqvist, utredaren Caroline Vidigsson Schmölzer och utredaren Carl Lundgren deltagit. Institutet för hälsoekonomi (IHE) har bidragit med en underlagsrapport och Statens beredning för medicinsk utvärdering (SBU) har bidragit med en litteratursökning.
Stockholm i januari 2024
Jean-Luc af Geijerstam, generaldirektör, Myndigheten för vård- och omsorgsanalys
Resultat i korthet
Vård- och omsorgsanalys har på regeringens uppdrag tagit fram en lägesbild av den nationella cancerstrategin. I denna PM belyser vi styrkor och utvecklingsbehov i strategin. I enlighet med uppdraget har vi tagit fram lägesbilden utifrån ett patient-, verksamhets- och systemperspektiv och inkluderat de standardiserade vårdförloppen och barncancervården. Vi har även identifierat ett antal omvärldsfaktorer som kan föranleda ändringar av cancerstrategin.
Våra slutsatser är:
- Den nationella cancerstrategin ger struktur och riktning men brister i prioritering, implementering och uppföljning.
- Måluppfyllelsen och insatserna skiljer sig åt mellan cancerstrategins olika målområden.
- De standardiserade vårdförloppen har skapat sammanhållna flöden i cancer vården men behöver utvecklas.
- Barncancervården har blivit en del i cancerstrategin men utvecklingsbehov kvarstår.
- Medicinteknisk utveckling, EU-initiativ och omställningen till god och nära vård behöver vägas in i en ny strategi.
Sammanfattning
Vård- och omsorgsanalys har på regeringens uppdrag tagit fram en lägesbild av den nationella cancerstrategin. I denna PM belyser vi styrkor och utvecklingsbehov i strategin. I enlighet med uppdraget har vi tagit fram lägesbilden utifrån ett patient-, verksamhets- och systemperspektiv och inkluderat de standardiserade vårdförloppen och barncancervården. Vi har även identifierat ett antal omvärldsfaktorer som kan föranleda ändringar av cancerstrategin.
Lägesbilden har tagits fram utifrån följande tre frågor:
- Vilka är styrkorna och utvecklingsbehoven i styrningen genom cancerstrategin?
- Vilka är styrkorna och utvecklingsbehoven i måluppfyllelsen och implementeringen av insatserna inom ramen för cancerstrategin?
- Vilka omvärldsfaktorer skapar behov av förändringar i cancerstrategin?
Den nationella cancerstrategin
Utredningen En nationell cancerstrategi överlämnade sitt betänkande 2009. Antalet personer med cancersjukdom beräknades öka kraftigt i framtiden. För att möta utvecklingen och förbättra cancervården identifierade utredningen fem övergripande mål och gav en rad olika förslag till åtgärder. Målen är
- att minska risken för insjuknande i cancer,
- att förbättra kvaliteten i omhändertagandet av patienter med cancer utifrån ett tydligt patientperspektiv,
- att förlänga överlevnadstiden efter en cancerdiagnos och förbättra livskvaliteten efter en cancerdiagnos,
- att minska regionala skillnader i överlevnadstid efter en cancerdiagnos samt
- att minska skillnader mellan befolkningsgrupper i insjuknande och överlevnadstid.
Den nationella cancerstrategin har operationaliserats i styrningen genom i första hand överenskommelser mellan regeringen och Sveriges kommuner och regioner samt uppdrag till myndigheter. I dessa framgår vilka konkreta insatser kopplade till cancerstrategin som ska genomföras. År 2018 beslutade regeringen om en långsiktig inriktning för cancervården. Den långsiktiga inriktningen anger en viljeriktning och innehåller inte bindande åtgärder, utan operationaliseras genom främst överenskommelser och myndighetsuppdrag.
De sex regionala cancercentrumen och deras ledning- och samverkansfunktion RCC i samverkan har en central roll i arbetet med att genomföra den nationella cancerstrategin, och utgör en struktur för kunskapsstyrningen av cancervården.
Strategin ger struktur och riktning men brister i prioritering, implementering och uppföljning
Enligt vår studie är synen på cancerstrategin överlag positiv. Cancerstrategin upplevs ha gett en gemensam inriktning för arbetet och skapat en struktur för nationell samverkan på flera områden och på så sätt blivit en modell för att skapa större enhetlighet i cancervården i Sveriges decentraliserade hälso- och sjukvårdssystem. Samtidigt finns det möjligheter att utveckla strategin som styrmedel. Det handlar främst om målens konkretionsgrad, prioriteringar och uppföljningen.
Målen för cancerstrategin är fortfarande relevanta, men kan utvecklas
Cancerstrategins mål uppfattas i hög grad som relevanta och tar sikte på centrala aspekter av hälso- och sjukvårdens mål, samtidigt som de utgår från relevanta utmaningar och tydliga förbättringsbehov. En svaghet i cancerstrategins övergripande mål är dock att målen inte konkretiserats i mer mätbara mål, kompletterats med målnivåer eller tidsatts. Det bidrar till brister i uppföljningen och ansvarsutkrävandet och medför en osäkerhet om måluppfyllelsen.
Strukturen för genomförande kännetecknas av förbättrad samverkan men bristande förutsättningar för implementering
Vår bedömning är att cancerstrategin har skapat en struktur för helhetssyn, samsyn och samverkan mellan olika aktörer, särskilt staten, RCC och regionerna.
Ansvarsfördelningen inom cancerstrategin är i huvudsak tydlig när det gäller RCC och statliga myndigheter. RCC:s möjligheter att svara mot sitt uppdrag begränsas dock av att man är en kunskapsstyrningsorganisation utan beslutsmandat. Ett återkommande tema är att uppdraget ibland inte upplevs motsvara möjligheterna att påverka. De förändringar som drivs av RCC kräver regionala beslut och prioriteringar, men regionernas ansvar är otydligt i överenskommelserna.
En annan utmaning i styrningen genom cancerstrategin är att styrdokumenten saknar vägledning för prioriteringar – både mellan olika mål och insatser inom cancervården och mellan cancervården i förhållande till annan vård. Osäkerhet kring vad som bör prioriteras och strukturella utmaningar, till exempel kompetensförsörjning, bidrar till en ofullständig och ojämn implementering.
Strategin har bidragit till förbättrade uppföljningsmöjligheter, men strategin har inte följts upp systematiskt
Cancerstrategin har bidragit till värdefull utveckling av uppföljningen inom cancervården. Några exempel på det är utvecklingen av uppföljning av patientrapporterade upplevelsemått, väntetidsdata och register för cancerläkemedel.
Det kvarstår samtidigt flera utvecklingsbehov när det gäller förutsättningarna för uppföljning, både för nationell uppföljning, verksamhetsutveckling och forskning. Utmaningarna är i regel gemensamma med de utmaningar som finns i hälso- och sjukvården i stort. En sådan utmaning är att det saknas uppgifter om primärvårdens insatser och rekvisitionsläkemedel i nationella hälsodataregister. En annan utmaning, särskilt för nationell uppföljning och hälsoekonomisk utvärdering av nya läkemedel, är att strukturen för datakällor är fragmentarisk, att olika källor inte kan kopplas ihop, att kvaliteten brister och att det behövs kommunicerande it-system och automatisk överföring för att minska den administrativa bördan. Det innebär att det är svårt att få tillgång till och koppla ihop nödvändiga data från olika källor, för att kunna analysera måluppfyllelsen och stödja implementeringen av cancerstrategin.
Utvecklingen inom precisionsmedicin och EU-samarbeten gör det också angeläget med förbättringar i informationshanteringen och uppföljningsmöjligheter av till exempel nya läkemedel. Även EU-initiativ kring delning av hälsodata inom EU skapar behov av ökad nationell samordning av hälsodata.
Ett utvecklingsbehov är uppföljningen av cancerstrategin i sin helhet. Utredningen som lade grunden för cancerstrategin lämnade flera förslag på hur cancerstrategin borde följas upp. Bland annat föreslog man att målen skulle följas upp löpande för att ge kunskap om utvecklingsbehoven och för att kunna justera insatserna. Även om det gjorts vissa punktinsatser i den riktningen, har det saknats en systematisk uppföljning.
Den sammantagna bilden från våra intervjuer är att förbättrad uppföljning kan göra cancerstrategin till ett tydligare och mer effektivt styrinstrument. Det anses önskvärt att någon aktör får i uppdrag att ta fram ett ramverk för uppföljning, definiera centrala indikatorer och löpande följa upp utvecklingen inom de olika målen i cancerstrategin. Det finns också ett behov av att följa upp genomslaget för riktlinjer. Vissa intervjupersoner lyfter även fram att det är viktigt att vidta åtgärder då riktlinjerna inte efterlevs. Det knyter i sin tur an till behovet av välmotiverade och konkreta mål i cancerstrategin.
Måluppfyllelsen och insatserna skiljer sig åt mellan strategins olika målområden
Cancerstrategin kan ses som ett paraply för en rad insatser inom cancerområdet. Insatsernas omfattning varierar stort – från uppbyggnaden av RCC till mer avgränsade aktiviteter som en förstudie om en telefonrådgivningstjänst för cancer.
Vår undersökning gör det inte möjligt att avgöra i vilken utsträckning insatserna inom cancerstrategin direkt har påverkat resultatet i relation till cancerstrategins fem mål. Däremot kan vi se att det finns en variation i hur långt man kommit inom respektive mål. Ett övergripande resultat är att insatserna inom cancerstrategin sammantaget tycks ha fungerat bättre när det gäller frågor som lättare kan avgränsas till den specialiserade cancervården – som omhändertagande och medicinsk kvalitet i behandlingen. Däremot har det varit svårare att arbeta med många av de frågor som är bredare och som kräver samverkan med aktörer utanför specialistvården.
Överlevnad och omhändertagande framstår som starkare områden
Utvecklingen när det gäller uppfyllelse av cancerstrategins mål varierar. Det finns en positiv utveckling särskilt när det gäller målen om förbättrad kvalitet i omhändertagandet, ökad överlevnad och minskade regionala skillnader i överlevnadstid. Däremot kan vi inte se en positiv utveckling när det gäller målet att minska skillnader mellan befolkningsgrupper i insjuknande. Vi har inte kunnat undersöka utvecklingen inom samtliga mål och för flera av målen saknas det ett tydligt sätt att mäta måluppfyllelsen.
Prevention som rör ohälsosamma levnadsvanor, livskvalitet och jämlikhet mellan grupper framstår som svagare områden
När det gäller målet att minska risken för insjuknande är det svårt att bedöma hur utvecklingen sett ut sammantaget. För de cancerformer vi undersökt närmare har risken för insjuknande utvecklats i olika riktning, och jämförelser över tid kompliceras av att diagnostiken sannolikt förbättrats. Prevention som rör ohälsosamma levnadsvanor har varit relativt lite i fokus i den nationella styrningen under större delen av perioden. Mer fokus har legat på prevention och tidig upptäckt genom screening. Ett mer övergripande arbete med prevention som rör ohälsosamma levnadsvanor har tagit form under de senaste åren, men det är ännu för tidigt för att se hur det faller ut.
Det är svårt att avgöra hur utvecklingen sett ut i relation till målet om förbättrad livskvalitet, eftersom det saknas sätt att följa upp utfall i livskvalitet på nationell och cancerövergripande nivå. Indikatorer över arbetssätt tyder på att den palliativa vården på flera sätt blivit bättre under perioden. När det gäller rehabilitering saknas underlag om hur tillgång och kvalitet utvecklats. Både palliativ vård och rehabilitering ingår i RCC:s uppdrag och RCC: arbete uppfattas ha bidragit till förbättringar. Dessa områden har samtidigt varit i jämförelsevis lite fokus i den nationella styrningen fram tills de senaste åren.
När det gäller målet om minskade skillnader mellan befolkningsgrupper har insatser i stort sett saknats i den nationella styrningen. Även om insatser skett inom RCC så tycks det ha saknats ett samlat grepp om frågan, och uppföljning tyder på att skillnader mellan befolkningsgrupper varit en svår fråga för RCC att arbeta med. Skillnaderna i insjuknande mellan befolkningsgrupper tycks vara större idag än när cancerstrategin togs fram. Hur skillnader i överlevnad mellan befolkningsgrupper har utvecklats över tid har vi däremot inte kunnat bedöma inom ramen för det här korta uppdraget.
De standardiserade vårdförloppen har skapat sammanhållna flöden i cancervården men behöver utvecklas
Standardiserade vårdförlopp (SVF) började införas 2015 i cancervården och omfattar ledtider och hur vårdprocessen ska se ut från misstanke till behandlingsstart. Vårdförloppen är en insats inom ramen för cancerstrategin och har även särskilda mål som anges i överenskommelserna. Flera av förslagen i betänkandet En nationell cancerstrategi för framtiden för att skapa mer sammanhållen vård och stärka patienternas ställning har genomförts inom ramen för SVF. De standardiserade vårdförloppen ska bidra till ökad tillgänglighet, patientnöjdhet och jämlikhet.
Vårdförloppen har delvis nått målen men det saknas kunskap om effekterna
När det gäller tillgänglighet har vårdförloppen kopplats samman med kortare väntetider för vissa diagnoser, men det långt kvar till att nå väntetidsmålet om att 80 procent ska inleda behandling inom ledtiden.
När det gäller patientnöjdhet och jämlikhet är målen att det ska ske en förbättring. Patientnöjdheten har ökat kontinuerligt sedan 2018 och de regionala skillnaderna har minskat något, men kvarstår i stor utsträckning.
Det saknas också i stor utsträckning kunskap om SVF:s påverkan på andra dimensioner i vården, vid sidan av målen, till exempel påverkan på medicinska utfall, prioriteringar och eventuell undanträngning av andra patientgrupper samt arbetsbelastningen i vården.
Styrkor och svagheter i vårdförloppen
Som styrkor med SVF har framkommit att de har bidragit till att tydliggöra begrepp och vårdprocesser, förbättra samverkan samt att uppföljningen möjliggjort jämförelser och skapat incitament för förbättring av väntetider.
Som svagheter med SVF har framkommit att ledtiderna av vissa uppfattas som för ambitiösa och att ledtider som inte är medicinskt motiverade bedöms kunna bidra till felaktiga prioriteringar i vården. SVF har bidragit till att ge former för verksamhets- övergripande processarbete men det finns fortfarande utmaningar kvar vad gäller sam- verkan mellan olika aktörer i vårdkedjan.
Barncancervården har blivit en del i cancerstrategin men utvecklingsbehov kvarstår
Barncancer tycks inte från början ha ingått i cancerstrategin, sett till strategins utformning, den nationella styrningen och genomförda insatser, utan tillkom efter regeringens avsiktsförklaring kring cancervården 2018. Sedan barncancer blev en tydligare del av cancerstrategin har flera insatser genomförts, bland annat för att stärka den nationella samordningen inom RCC, förbättra omhändertagandet av patienter, genom till exempel kontaktsjuksköterskor och förbättrad samordning mellan barn- och vuxenvården, stärkt långtidsuppföljning, samt stärkt palliativ vård för barn.
Som starka områden framkommer i barncancervården kvaliteten i omhändertagandet, de medicinska resultaten och den geografiska jämlikheten. Som styrkor i barncancervården lyfts fram starka strukturer för vården samt det nationella samarbetet inom ramen för RCC och i professionsnätverk. Området ligger också långt fram vad gäller tillämpningen av precisionsmedicin.
Som svagheter lyfts kompetensförsörjning och finansiering, samt tillgången till läkemedel och kliniska studier. Det framkommer också att stödet till en förbättrad livskvalitet varierar mellan regionerna, till exempel vad gäller rehabilitering.
Ett särskilt område som aktualiseras för barn och unga vuxna är övergången mellan barncancervården och vuxencancervården. Det lyfts fram att unga vuxna cancerpatienter upplever ensamhet, bristande psykosocialt stöd och stöd när det gäller behov kopplade till fertilitet, sexualitet, studiegång och etableringen på arbetsmarknaden samt bristande informationsöverföring mellan vårdaktörer.
Medicinteknisk utveckling, EU-initiativ och omställningen till en god och nära vård behöver vägas in i en ny strategi
Vår sista slutsats siktar in sig på omvärldsfaktorer som en reviderad cancerstrategi behöver förhålla sig till. Några faktorer som vi vill lyfta fram är EU:s initiativ på cancerområdet, precisionsmedicin, förändringar i organiseringen av cancervården och omställningen till god och nära vård.
EU:s initiativ på cancerområdet
På EU-nivå pågår flera initiativ som en reviderad svensk cancerstrategi behöver förhålla sig till.
EU:s cancerplan, som syftar till att stärka cancervården i EU, är i stor utsträckning förenlig med den nuvarande cancerstrategin. Men det finns vissa skillnader. Exempelvis innehåller den konkreta mål, framför allt kopplat till prevention och tidig upptäckt. Dessutom innehåller den initiativ för att stärka samarbetet mellan EU-länderna i frågor som standardisering och delning av hälsodata samt kunskapsspridning. I arbetet med att revidera cancerstrategin är det viktigt att avgöra hur EU:s cancerplan ska avspeglas i den svenska strategin, till exempel hur en reviderad cancerstrategi ska förhålla sig till målen i EU:s cancerplan.
EU:s initiativ på cancerområdet aktualiserar också behov av att avgöra vilka aktörer som ska representera Sverige, och på vilket sätt samarbetet på EU-nivå ska tas tillvara. Mångfalden av EU-nätverk och satsningar skapar behov av samordning bland svenska aktörer, för att kunna tillgodogöra sig möjligheterna. Man behöver också tydliggöra hur styrstrukturen i Sverige ska knyta an till de strukturer som byggs upp på EU-nivå, och hur Sverige ska representeras i olika sammanhang.
Det pågår en utveckling mot en enhetlig struktur för hälsodata på EU-nivå. Det är särskilt aktuellt för cancerområdet, eftersom EU:s cancerplan berör flera sådana initiativ. Utvecklingen på EU-nivå gör frågor om enhetlig struktur för hälsodata inom Sverige ännu mer angelägna.
En cancerstrategi behöver balansera flera olika mål kopplade till den medicinska utvecklingen
Inom cancerområdet pågår en utveckling mot nya avancerade diagnostiska metoder och behandlingsalternativ. De har möjliggjort tidigare upptäckt, ökad överlevnad och bättre livskvalitet för cancerpatienter.
Inriktningen i den nationella life science-strategin är att Sverige ska vara ett föregångsland när det gäller att införa precisionsmedicin i vården. Frågan om att stärka forskning och medicinsk utveckling bör vara en del av den nationella cancerstrategin. Samtidigt behöver en cancerstrategi balansera flera perspektiv på den medicinska utvecklingen.
Å ena sidan är det positivt att patienter får tillgång till nya effektiva läkemedel, å andra sidan medför det ökade kostnader och behov av prioriteringar. Vi ser att en cancerstrategi behöver skapa en balans mellan en snabb tillgång till läkemedel och andra värden, till exempel kostnadseffektivitet och möjligheter för regionerna att planera och prioritera.
Utvecklingen av precisionsmedicin kommer även innebära flera utmaningar kopplade till exempelvis finansiering, införande och uppföljning. Det kommer finnas behov av att utveckla vårdens infrastruktur, till exempel diagnostik, it-system samt kompetens- och personalförsörjning. En cancerstrategi behöver stötta utvecklingen av en infrastruktur för precisionsmedicin och nya avancerade behandlingar.
Förändringar i organiseringen av cancervården
I det material vi samlat in lyfts framförallt två områden fram när det gäller organiseringen av de övergripande strukturerna för cancervården. Det gäller särskilt relationen mellan RCC och CCC (Comprehensive Cancer Centres, som är internationellt ackrediterade cancercentrum med vård, forskning och utbildning), samt RCC och CCC i förhållande till statliga myndigheter.
Framväxten av CCC parallellt med RCC-strukturen skapar utmaningar. Från ett systemperspektiv lyfter flera aktörer fram att det finns ett behov av att från statlig nivå tydliggöra vilka roller RCC och CCC ska ha och hur de ska förhålla sig till varandra. Det är viktigt bland annat för att undvika dubbelarbete och konflikterande styrsignaler samt för att ta tillvara respektive aktörs styrkor när det gäller att skapa förutsättningar för implementering och samverkan. Behovet av att skapa tydliga roller förstärks ytterligare av utvecklingen inom cancer på EU-nivå. Som vi nämnt ovan behöver det klargöras vilken eller vilka aktörer som ska representera Sverige i EU-sammanhang och hur rollfördelningen ska se ut för att spegla EU:s organisation på cancerområdet.
Omställningen till en god och nära vård
Den ökade medicinska kvaliteten och minskade dödligheten i cancersjukdomar har över tid medfört en förskjutning av cancervården mot ett behov av att hantera långvariga, och ibland kroniska tillstånd. Då blir behovet av till exempel långsiktig rehabilitering, kontinuitet i vården och stöd till att samordna insatser från olika aktörer mer framträdande.
Sett till primärvårdens nya lagreglerade grunduppdrag ser vi att primärvården borde ta ett ansvar när det gäller områden som prevention, rehabilitering och samordning. Men vår kartläggning av cancerstrategins implementering visar att det inom dessa breda områden skapats egna specialiserade cancerspecifika strukturer – till exempel särskilda centrum för cancerrehabilitering, eller att resultaten är bättre för cancerpatienter inom palliativ vård, trots att den typen av insatser är eller borde vara likartade för många grupper av patienter.
Mot den bakgrunden blir det viktigt i arbetet med en ny cancerstrategi att upp- märksamma vilken roll primärvården ska ha i cancervården och hur den pågående omställningen till en god och nära vård kan påverka det. Även den kommunala hälso- och sjukvården kan förväntas få en allt större roll i vården av cancerpatienter, till exempel när det gäller långsiktig rehabilitering och palliativ vård. Det bör också uppmärksammas i en ny cancerstrategi.
I arbetet har framkommit flera andra medskick till en reviderad cancerstrategi
I vårt uppdrag ingår inte att lämna förslag till innehållet i en ny strategi men vi bedömer att våra slutsatser ändå ger vägledning om behovet av förändringar av strategin. Utöver våra slutsatser har vi identifierat tre områden som vi anser bör adresseras i arbetet med en reviderad cancerstrategi.
En cancerstrategi som tar ett bredare grepp
Ett första övergripande medskick är att regeringen bör överväga om cancerstrategin ska utformas så att den tar ett bredare grepp. I vår analys av andra länders cancerstrategier, EU:s cancerplan och våra intervjuer framkommer att vissa aspekter skulle kunna ingå i cancerstrategin på ett tydligare sätt. Det handlar om att strategin bör omfatta alla åldrar, och därmed tydligare innefatta vården av barn och unga vuxna. Vid sidan av patientperspektivet har det också lyfts att närståendeperspektivet behöver bli tydligare i strategin. Det handlar också om att strategin bör omfatta jämlikhet i alla delar av målen och tydligt belysa hela vårdkedjan. Överlevnaden i cancer har i många fall ökat, vilket gör cancer till mer av en kronisk sjukdom, där livskvalitet och långsiktig rehabilitering och palliativ vård efter den akuta behandlingen blir mer framträdande. Flera uttrycker också ett behov av att tydliggöra att cancer är en av flera diagnoser som hälso- och sjukvården behöver förhålla sig till och att vården av cancerpatienter i stor utsträckning sker i verksamheter som också ägnar sig åt flera andra patienter än cancerpatienter.
Ett ökat genomslag för cancerstrategin
Ett andra övergripande område för medskick är insatser för att öka cancerstrategins genomslag i vården. Vi bedömer att det finns flera möjligheter att öka genomslaget. En viktig orsak till ojämn implementering är enligt flera intervjupersoner en otydlig nationell styrning på övergripande nivå, med otydliga prioriteringar och bristande operationalisering av strategin. Många lyfter även fram att styrningen behöver anpassas till regionala förutsättningar – det som ska göras måste också vara genomförbart – och att regionerna behöver finnas med på ett tydligare sätt i strategin. I dagsläget finns det en osäkerhet bland flera aktörer kring om regionerna står bakom strategin, och vilka aktörer som ansvarar för genomförande av insatserna och finansiering i strategins olika delar. Om cancerstrategin operationaliseras i handlingsplaner eller uppdateringar behöver det även klargöras vilken aktör som ansvarar för det, liksom för uppföljningen som dessa bör baseras på.
En cancerstrategi med tydligare roller och mandat
Ett sista övergripande medskick är att roller och mandat i cancerstrategin behöver bli tydligare. Otydliga mandat har i vissa fall inneburit hinder för genomförandet av cancerstrategin. I dagsläget saknas strukturer för att tillgodose behovet av horisontella prioriteringar i kunskapsstyrningen inom cancervården. Mot bakgrund av omvärldsfaktorer som det ökade EU-samarbetet, framväxten av CCC och omställningen till god och nära vård blir tydliga roller och mandat ännu viktigare. Flera intervjupersoner betonar också att det är viktigt att cancerstrategin innehåller eller kompletteras med stöd för horisontella prioriteringar och att det finns en aktör med ansvar för det. Många intervjupersoner nämner också de regionala skillnaderna och efterfrågar en ökad nationell styrning eller samordning på cancerområdet i syfte att öka jämlikheten. Det framkommer också en önskan om ett ökat statligt ansvarstagande eller ett tydligare formulerat uppdrag för någon aktör på en rad delområden som uppfattas som svaga eller där utvecklingen har gått långsamt, till exempel prevention, rehabilitering, palliativ vård och kompetensförsörjning.
1 Inledning
Den nationella cancerstrategin har funnits sedan 2009. Den inleddes med betänkandet En nationell cancerstrategi för framtiden (SOU 2009:11), mot bakgrund av att antalet personer med cancer förväntades öka kraftigt och att det därför var viktigt att arbeta för att förhindra insjuknande och död i cancer, förbättra omhändertagandet av patienter med cancer och stärka patientperspektivet.
Strategin omfattar hela kedjan från förebyggande, diagnos och behandling till rehabilitering och palliativ vård, samt förutsättningarna för god cancervård i form av bland annat organisering, kunskapsstyrning och forskning.
Regeringen har 2023 aviserat att man ska uppdatera den nationella cancerstrategin. Vårt uppdrag har varit att på kort tid göra en lägesbild över den befintliga nationella cancerstrategin, som ingång och underlag för det fortsatta arbetet med att revidera cancerstrategin. I lägesbilden ger vi en överblick över styrkor, svagheter och utvecklings- behov i cancerstrategin utifrån befintlig kunskap, samt ger medskick till en uppdaterad cancerstrategi.
1.1 Lägesbild av den nationella cancerstrategin
Vård- och omsorgsanalys har fått i uppdrag av regeringen att ta fram en lägesbild av den nationella cancerstrategin och dess implementering.
Syftet är att tydliggöra den nationella cancerstrategins styrkor och utvecklingsbehov. Lägesbilden ska tas fram utifrån ett patient-, verksamhets- och systemperspektiv och inkludera de standardiserade vårdförloppen och barncancer. I uppdraget ingår även att identifiera om det finns omvärldsfaktorer som bör föranleda ändringar av den nationella cancerstrategin.
Tre frågeställningar har väglett arbetet med promemorian:
- Vilka är styrkorna och utvecklingsbehoven i styrningen genom cancerstrategin?
- Vilka är styrkorna och utvecklingsbehoven i måluppfyllelsen och implementeringen av insatserna inom ramen för cancerstrategin?
- Vilka omvärldsfaktorer skapar behov av förändringar i cancerstrategin?
1.2 Analysen bygger på intervjuer, indikatorer och tidigare uppföljningar av cancerstrategin
I arbetet har vi använt oss av flera kompletterande källor och metoder. På grund av den begränsade tiden för regeringsuppdraget har vi haft begränsade möjligheter till egen datainsamling, exempelvis i form av omfattande enkäter till regioner och verksamheter, eller några mer omfattande analyser av måluppfyllelse. Vår lägesbild vilar därför i stor utsträckning på tidigare uppföljningar av insatserna inom cancerstrategin samt på de intervjuer vi genomfört.
Dokumentsstudie
I en dokumentstudie har vi kartlagt målen och insatserna inom cancerstrategin utifrån cancerstrategins styrdokument, bland annat betänkandet En nationell cancerstrategi för framtiden (SOU 2009:11), regeringens avsiktsförklaring för cancervården Långsiktig inriktning för cancervården, regeringsuppdrag till myndigheter samt överenskommelser mellan regeringen och Sveriges Kommuner och Regioner (SKR). Vi har sammanställt tidigare uppföljningar av cancerstrategin och dess insatser samt kartlagt utvecklingstendenser med bäring på cancerområdet. Vi har även jämfört med cancerstrategier från andra länder (se bilaga 6). Statens beredning för medicinsk utvärdering (SBU) har gjort en litteratursökning åt oss efter forskning om effekter av de standardiserade vårdförloppen (SVF) i cancervården i Sverige, Danmark och Norge. Utifrån SBU:s sammanställning har vi själva bedömt studiernas relevans och dragit slutsatser kring den befintliga kunskapen om effekterna av SVF.
Intervjuer och möten
Vi har gjort en intervjustudie med patientföreträdare, professionsrepresentanter, forskare, berörda myndigheter och representanter för regionala cancercentrum i samverkan, Comprehensive Cancer Centres (CCC) och SKR. På grund av den korta tiden för genomförandet av regeringsuppdraget har vi gjort flera avgränsningar. Rapporten inkluderar exempelvis inte regioner eller verksamheter, vilket medför att vi bara delvis fångar regionernas och verksamheternas perspektiv, bland annat genom representanter för RCC och CCC:er samt företrädare för professionsorganisationer som Fysioterapeuterna, Föreningen MAS/MAR och Svenska läkaresällskapet.
Intervjuerna har syftat till att identifiera olika aktörers uppfattning om cancervårdens styrkor och utvecklingsbehov, men även implementeringen och uppföljningen av den nationella cancerstrategin samt vilka omvärldsfaktorer som kan föranleda förändringar av cancerstrategin.
Intervjuundersökningen utgick från en semi-strukturerad intervjuguide (se bilaga 1), som har anpassats något efter intervjupersonens befattning och roll. Frågorna berörde i huvudsak styrkor och utvecklingsbehov i styrningen och implementeringen av den nationella cancerstrategin samt utvecklingsbehov i ljuset av omvärldsfaktorer.
Intervjuerna genomfördes via videolänk och var cirka 60 minuter långa. De flesta av intervjuerna genomfördes individuellt. Vid enstaka tillfällen deltog två eller fler personer samtidigt.
Totalt 34 aktörer har kontaktats varav alla utom en ställde upp på en intervju. Vissa intervjuer genomfördes med flera personer från en aktör samtidigt och totalt har 44 personer intervjuats under perioden juni–november 2023. En förteckning av intervju- personerna finns i bilaga 2.
Utöver intervjuerna har vi stämt av och inhämtat medskick till vårt arbete under möten med Hälso- och sjukvårdsdirektörsnätverket, RCC i samverkan samt De forskande läkemedelsföretagen (LIF).
Enkätundersökning med patientorganisationer
Vi har även genomfört en enkätundersökning riktad till diagnosspecifika patient- organisationer inom cancerområdet i Sverige. Syftet med enkäten var att belysa cancer- vården och den nationella cancerstrategin ur ett patientperspektiv.
Undersökningen besvarades under perioden 12 oktober–14 november 2023. Totalt svarade 10 av 22 organisationer på enkäten, vilket motsvarar en svarsfrekvens på 46 procent. Enkäten och deltagande organisationer finns i bilaga 3.
Skriftliga frågor till regionala cancercentrum
Vi har skickat skriftliga frågor till Sveriges sex regionala cancercentrum (RCC). Syftet var att belysa cancerstrategin ur ett verksamhetsnära systemperspektiv.
Frågorna berörde framförallt styrkor och utvecklingsbehov inom styrning, samordning och implementering av den nationella cancerstrategin. Totalt fem av sex RCC besvarade frågorna, som finns i bilaga 4.
Indikatorbaserad analys av utvecklingen i förhållande till målen
Institutet för hälso-och sjukvårdsekonomi (IHE) har på vårt uppdrag genomfört en studie av måluppfyllelsen, utifrån målen för cancerstrategin och ett urval av diagnoser. Utöver att ge en lägesbild av cancervården, inklusive barncancervården och hälso- och sjukvårdens mål i stort, belyser studien jämlikhet mellan befolkningsgrupper och regioner. Underlagsrapporten finns tillgänglig på förfrågan.
Resultatseminarium
För att kvalitetssäkra våra resultat och samla ihop andra medskick till vårt arbete anordnade vi ett resultatseminarium den 5 december 2023. I seminariet deltog femton representanter för patientorganisationer och professionen, forskare, företag, berörda myndigheter samt RCC, för att diskutera preliminära resultat och medskick till innehållet i en uppdaterad strategi. En sammanställning av deltagarna finns i bilaga 5.
1.3 Avgränsningar
Vårt arbete med en lägesbild av cancerstrategin har bedrivits under en relativt kort tids- period och vi har därför behövt göra flera avgränsningar.
En viktig avgränsning är att vi inte har undersökt styrkor och svagheter med att regeringen styr genom en cancerstrategi. Vi har inte belyst om det är lämpligt att prioritera cancer framför andra diagnosområden inom hälso- och sjukvården och inte heller möjligheten att använda andra styrmedel än en strategi för att främja utvecklingen av cancervården. I stället fokuserar vi på styrkor och utvecklingsbehov genom att utgå ifrån att det även framöver kommer att finnas en cancerstrategi. Vi kan inte heller dra några slutsatser om vilka områden som strategin bör omfatta eller om de borde omfattas av någon annan styrning. Det kan till exempel handla om diagnosövergripande områden som prevention som rör ohälsosamma levnadsvanor, rehabilitering och palliativ vård.
Vi har också avgränsat oss när det gäller hur den nationella cancerstrategin påverkar den regionala styrningen ur regionernas perspektiv. Vi har inte analyserat de regionala handlingsplanerna eller intervjuat representanter för regioner och kommuner på högre ledningsnivå. Det arbete och den samverkan som sker mellan framförallt RCC och de aktörerna kan vi därför inte dra några slutsatser om. Vi har inte heller underlag för att belysa cancerstrategin ur den kommunala hälso- och sjukvårdens perspektiv.
Vi har inte på ett fullständigt sätt kunnat belysa utvecklingen i relation till de mål som finns i cancerstrategin. Istället har vi inom ramen för uppdraget genomfört en indikator- studie utifrån fyra cancerformer: njurcancer, bröstcancer, lungcancer och kolorektalcancer.
1.4 Rapportens disposition
I kapitel 2 beskriver vi cancerstrategin som styrmedel.
I kapitel 3 beskriver vi på vilket sätt den nationella cancerstrategin har genomförts, och vilka insatser som gjorts på nationell nivå. Vi beskriver också vilket genomslag insatserna har fått och ger en lägesbild av måluppfyllelsen utifrån centrala indikatorer och utvärderingar.
Kapitel 4 och 5 ger en fördjupad beskrivning av standardiserade vårdförlopp i cancer- vården samt cancervården för barn och unga vuxna.
I kapitel 6 kartlägger vi omvärldsfaktorer som förväntas kunna få konsekvenser för cancervården framöver.
I kapitel 7 presenterar vi våra slutsatser.
2 Cancerstrategin som styrmedel
I det här kapitlet analyserar vi styrkor och svagheter i cancerstrategin som styrmedel i ett tillbakablickande perspektiv. Vi har belyst styrningen genom cancerstrategin utifrån åtta kriterier för en effektiv strategi. Vi jämför också den svenska cancerstrategin med cancerstrategier och cancerplaner i andra länder. Detta är de viktigaste resultaten:
- Den nationella cancerstrategin har varit ett framgångsrikt sätt att sprida Den har bidragit till att bygga upp en struktur för gemensam förändring i ett decentraliserat system.
- Strategin kan utvecklas som styrmedel. I dess nuvarande utformning är det otydligt vilket genomslag den kan förväntas ha. Vår studie pekar på följande förklaringar:
- Strategin saknar konkreta och mätbara mål.
- Det saknas en systematisk uppföljning.
- Genomslaget för insatserna är beroende av regionernas prioriteringar, samtidigt som strategin inte ger något stöd för vilka mål eller insatser som är mest prioriterade.
2.1 Vårt ramverk – kriterier för en strategi som effektivt styrmedel
Vi beskriver styrkor och svagheter i cancerstrategin utifrån åtta kriterier för en effektiv strategi. Liknande kriterier har Statskontoret använt vid tidigare uppföljningar av nationella strategier (se till exempel Statskontoret 2015, 2018 och 2020). Statskontoret (2023) beskriver en strategi som en form av otraditionell styrning, som kännetecknas av frivillighet, samverkan och samordning. Vi har utgått från följande kriterier:
Strategin som inriktningsdokument
- Strategins syfte och mål bör vara tydliga för de aktörer som ska genomföra den. Det innebär att målen bör vara relevanta, realistiska, tydligt definierade, tidsatta och möjliga att mäta.
- Strategin bör peka ut prioriterade områden för insatser. Om strategin innehåller en variation av insatsområden kan prioriteringar mellan dem underlätta genomförandet.
- Insatserna i strategin bör ha en tydlig koppling till målen och de prioriterade områdena. Eftersom aktörer inte är bundna att genomföra en strategi behöver den kopplas till konkreta styråtgärder för att få genomslag. Syftet med en strategi är ofta att beskriva ett samhällsproblem och därmed öka förståelsen och legitimiteten för målen och åtgärderna på ett område. För att öka genomslaget för insatserna är det därför en fördel om de tydligt motiveras utifrån problembilden samt de mål och prioriterade områdena som tagits fram utifrån den.
Struktur för genomförande
- Ansvarsfördelningen mellan de aktörer som ska genomföra strategin bör vara tydlig. En tydlig ansvarsfördelning kännetecknas av att strategin tydligt anger vilken aktör som har vilket uppdrag och att det inte finns ansvar som faller mellan olika aktörer.
- De aktörer som ska genomföra strategin bör ha mandat och goda förut sättningar att genomföra åtgärderna i strategin. Att ansvar åtföljs av mandat, så att den ansvariga aktören har möjlighet att påverka i frågan, är en viktig förutsättning för att kunna genomföra insatserna och nå målen. Förutsättningarna kan också till exempel vara ekonomiska och personalresurser. För att en ansvarig aktör ska kunna genomföra sitt uppdrag kan det krävas att andra aktörer agerar för att skapa förutsättningar.
- Strategin bör skapa förutsättningar för samverkan mellan berörda aktörer. Genomförandet av en strategi som berör många aktörer kräver ofta samordning, exempelvis genom att man skapar en struktur för samverkan. En strategi kan också främja samverkan genom att rikta fokus mot ett område.
Uppföljning av strategin
- Uppföljningen bör ske En systematisk uppföljning förutsätter att det finns en plan för hur uppföljningen ska gå till. Det handlar bland annat om hur målen ska operationaliseras och mätas, hur ofta det ska ske, samt att utse en aktör som har ansvaret.
- Det bör finnas förutsättningar för uppföljning. Förutsättningar för uppföljning innebär att det samlas in data om de mått som ska följas upp, och att data är av god kvalitet och tillgänglig för de aktörer som ska sköta uppföljningen.
2.2 Cancerstrategin som inriktningsdokument
Cancerstrategin är inte ett enda styrdokument, utan kommer till uttryck i en rad olika styrdokument: betänkandet En nationell cancerstrategi för framtiden (SOU 2009:11), överenskommelser mellan regeringen och Sveriges Kommuner och Regioner (SKR), inriktningsdokument för regionala cancercentrum (RCC) och Långsiktig inriktning för det nationella arbetet med cancervården som regeringen beslutat om (Regeringen 2018). I det här avsnittet beskriver vi styrkor och svagheter i den nationella cancerstrategin utifrån en sammanställning av dessa styrdokument.
2.2.1 Cancerstrategin utgår från betänkandet En nationell cancerstrategi för framtiden
Statskontoret (2023) beskriver att strategier som riktar sig till myndigheter och andra aktörer inte brukar ha formen av bindande beslut, utan att strategin snarare är ett sätt att systematiskt presentera olika konkreta åtgärder. Resultatet av strategin beror på hur man genomför de konkreta åtgärder som den presenterar.
Den nationella cancerstrategin utgår främst från betänkandet En nationell cancerstrategi för framtiden (SOU 2009:11). Betänkandet innehåller ett förslag till en nationell cancerstrategi med fem mål för cancerområdet. Målen, motiven till dem och den önskade utvecklingen enligt betänkandet framgår av tabell 1 nedan. I betänkandet föreslås också en rad konkreta åtgärder för att uppnå målen. Värdet av åtgärderna motiveras utifrån ett medborgar-, patient-, och systemperspektiv.
Förslagen i det ovan nämnda betänkandet har inte formaliserats genom något beslut eller annat tillkännagivande från regeringen eller riksdagen. Den har istället operationaliserats i styrningen genom i första hand överenskommelser mellan regeringen och SKR samt uppdrag till myndigheter. Där framgår vilka konkreta åtgärder kopplade till cancerstrategin som ska genomföras. År 2018 beslutade regeringen om en långsiktig inriktning för cancervården (Regeringen 2018). Den långsiktiga inriktningen anger en viljeriktning och innehåller inte bindande åtgärder, utan även den operationaliseras genom främst överenskommelser och myndighetsuppdrag.
Tabell 1. Målen för den nationella cancerstrategin enligt betänkandet En nationell cancerstrategi för framtiden.
| Mål | Motiv | Önskad utveckling |
|---|---|---|
| Minska risken för insjuknande i cancer | • Möjligheterna att påverka insjuknandet i cancer tas inte till vara fullt ut.
• Folkhälsopolitiken saknar tydliga mål och strukturer. |
• Ökade investeringar i prevention.
• Samlade, uthålliga och inriktade insatser mot uppföljningsbara mål. • Ökat statligt ansvar eftersom det krävs prioriteringar på sektorsövergripande nivå. • God och jämlik tillgång till screeningprogram. |
| Förbättra kvaliteten i omhändertagandet av patienter med cancer utifrån ett tydligt patientperspektiv | • Patienter och personal riktar kritik mot att vården är fragmentarisk, med bristande kontinuitet och långa och varierande väntetider. | • Stärkt ställning för patienterna.
• Utveckling av nya insatser för en mer patientfokuserad och sammanhållen vård, utan onödiga väntetider. |
| Förlänga överlevnadstiden och förbättra livskvaliteten efter en cancerdiagnos | • Antalet personer som insjuknar i cancer, väntas öka kraftigt.
• I takt med kunskapsutvecklingen blir behandlingarna mer komplexa och allt större mängder ny kunskap behöver spridas och omsättas i praktik. • Det finns en risk för regionala skillnader. • Den palliativa vården är resursmässigt eftersatt med brister i tillgänglighet och kvalitet samt har stora geografiska skillnader. |
• En mer sammanhållen struktur och en medveten nivåstrukturering, med tydliga roller för primärvård, länssjukvård och de cancercentrum som föreslås inrättas på sjukvårds- regional nivå.
• Ökad närhet mellan vården och forskningen. • Nya gemensamma former för bedömning, introduktion och uppföljning av nya läkemedel. • Ökad prioritering av den palliativa vården. |
| Minska regionala skillnader i överlevnadstid efter en cancerdiagnos | • Den decentraliserade vården har fört med sig omotiverade regionala skillnader i praxis och utfall. | • Ökad samordning av till exempel screeningprogram och gemensamma system för kunskapsspridning och introduktion av nya läkemedel.
• Fastare former för det nationella samarbete som drivits av professionerna. • En mer standardiserad vård, exempelvis genom gemensamma vårdprogram. |
| Minska skillnader mellan befolkningsgrupper i insjuknande och överlevnadstid | • Det finns socioekonomiska skillnader i insjuknande och överlevnadsprognos. | • Särskilda insatser för att minska socioekonomiska skillnader. |
Källa: SOU 2009:11
Långsiktig inriktning förändrade strategin i viss mån
År 2018 beslutade regeringen om en långsiktig inriktning för det nationella arbetet med cancervården (Regeringen 2018). Inriktningen är en avsiktsförklaring med syftet att ”skapa tydlighet kring hur regeringen vill att det nationella arbetet med cancervården ska utvecklas inför framtiden”. Fokus ligger på arbetet fram till 2025, men kan även ses som en vision med mål som är angelägna även på längre sikt. Inriktningen är i stor utsträckning i linje med betänkandet från 2009, och innebär ingen förändring av de fem övergripande målen. Vissa områden lyfts dock fram något tydligare, bland annat prevention, närståendeperspektivet, rehabilitering, uppföljning och palliativ vård, primärvårdens roll samt cancervård för barn och unga. Det blir särskilt tydligt i regeringens bedömning av hur RCC:s arbete bör inriktas i framtiden, där de här områdena ingår.
2.2.2 Cancerstrategin har operationaliserats genom överenskommelser
I överenskommelserna mellan regeringen och SKR anges hur cancerstrategin ska omsättas i regionernas verksamhet. I första hand förväntas det ske genom RCC.
Eftersom överenskommelserna omfattar ett stort antal insatser har vi sammanfattat den huvudsakliga inriktningen för överenskommelserna i tre perioder: 2010–2013, 2015–2019 och 2020–2023.
Överenskommelser 2010–2013: Fokus på cancervårdens förutsättningar
Under perioden 2010–2013 sluts den treåriga överenskommelsen om ”ännu bättre cancervård” och RCC får sin form och inrättas (Socialdepartementet och SKL 2010, 2011, 2012). Ett jämförelsevis stort antal uppdrag riktas också till myndigheter, främst till Socialstyrelsen. Dessa gäller bland annat uppföljningen av cancervården och en modell för bedömning och införande av nationella screeningprogram.
Huvudfokus under den här perioden är insatser inriktade på samtliga mål i strategin, som uppbyggnaden av RCC och förbättrade möjligheter till uppföljning. I övrigt är insatserna relativt jämnt fördelade mellan målen om minskad risk för insjuknande, bättre omhändertagande, överlevnad och livskvalitet och i viss mån minskade regionala skillnader. Minskade skillnader mellan grupper i befolkningen ingår som del i vissa insatser inom prevention och tidig upptäckt.
Överenskommelser 2015–2019: Standardiserade vårdförlopp och omhändertagande i centrum
Under denna tid sluts årliga överenskommelser om ”kortare väntetider i cancervården” inom ramen för ”regeringens cancersatsning 2015–2019” (Socialdepartementet och SKL/ SKR 2015, 2016, 2017, 2018, 2019).
Huvuddelen av insatserna avser diagnos och behandling, främst med fokus på omhändertagandet och särskilt på väntetider. En betydligt mindre andel av insatserna än tidigare handlar om prevention och tidig upptäckt. En stor andel av insatserna och den allra största delen av de ekonomiska medlen i överenskommelserna handlar om att införa standardiserade vårdförlopp. Myndighetsuppdragen handlar främst om finansiering och uppföljning av RCC.
Överenskommelser 2020–2023: Ökat fokus på överlevnad och livskvalitet
Inom ramen för ”regeringens cancersatsning 2020–2022” slöts varje år överenskommelser om ”jämlik och effektiv cancervård med kortare väntetider”, och även 2023 års överenskommelse går under samma namn (Socialdepartementet och SKR 2020, 2021, 2022, 2023).
Insatser inriktade på diagnos och behandling dominerar, men jämfört med 2015–2019 är det mer fokus på cancerpatienters överlevnad och livskvalitet, och mindre på förbättrat omhändertagande. De standardiserade vårdförloppen är fortsatt föremål för mycket av insatserna och de ekonomiska medlen, men är inte lika starkt i fokus som tidigare. En större andel av aktiviteterna handlar istället om medicinsk teknologi och läkemedel, samt om rehabilitering och palliativ vård.
Målet om minskad risk för insjuknande är även under den här perioden i mindre fokus för den nationella styrningen än behandling, men i överenskommelserna ingår att genomföra RCC:s nationella plan för cancerprevention, som i sin tur specificerar en rad förebyggande insatser.
Insatser för barncancer och särskilda ekonomiska medel till barncancerområdet blir under den här perioden tydligare i överenskommelserna, inom ramen för en särskild satsning på barncancer.
2.2.3 Regionala cancercentrumens uppdrag utgår från cancerstrategin
Regionala cancercentrum (RCC) är regionernas kunskapsorganisation inom cancer- området. RCC i samverkan är en nationell samverkansgrupp som består av cheferna för de sex regionala cancerscentrumen och den nationella cancersamordnaren. RCC:s uppdrag definieras i 19 kriterier för RCC, och omfattar samtliga mål i cancerstrategin. Kriterierna presenterades av den nationella cancersamordnaren 2011 i en promemoria (Socialdepartementet 2011).
Kriterier för RCC
Enligt kriterierna från 2011 ska varje RCC:
- leda och samordna sjukvårdsregionens arbete att effektivisera vårdprocesserna inom cancervården
- utarbeta en strategisk utvecklingsplan för cancervården i sjukvårdsregionen
- ha en plan som tillförsäkrar cancerpatienter tillgång till psykosocialt stöd, rehabilitering och palliativ vård av god kvalitet inom hela sjukvårdsregionen
- arbeta för att stödet till närstående till cancerpatienter utvecklas
- arbeta för att en individuell skriftlig vårdplan tas fram för varje cancerpatient
- arbeta för att cancerpatienter får stöd från en kontaktsjuksköterska eller motsvarande kontaktperson
- arbeta för att kunskapen om patientens rätt till förnyad bedömning ökar bland hälso- och sjukvårdspersonalen och att berörda cancerpatienter får information om denna rätt
- arbeta för att patientrapporterade uppgifter samlas in och används i arbetet med att utveckla cancervården
- utforma och implementera en utbildnings- och kompetensförsörjningsplan för sjukvårdsregionens cancervård
- delta i arbetet med nationella riktlinjer och vid behov utarbeta regionala vårdprogram
- stödja att nationella riktlinjer och vårdprogram och annan frontlinjekunskap inom cancervården implementeras i hela sjukvårdsregionen. Detta innefattar den regionala implementeringen av kommande nationella målnivåer
- arbeta för att nationella kvalitetsregister används för cancervårdens verksamhetsutveckling
- arbeta för att stärka den kliniska cancerforskningen i regionen och i landet och för att vetenskapliga framsteg snabbt kommer cancerpatienter till del
- utveckla strukturer för samarbete med akademisk forskning och den forskande industrin samt främja innovationer i cancervården
- ha en tydlig ledningsorganisation med stark förankring i landstings- respektive regionledningarna i sjukvårdsregionen
- samverka med andra RCC ha system för uppföljning av cancervårdens kvalitet
- utarbeta en plan för nivåstrukturering av cancervården i sjukvårdsregionen och stödja arbetet med att implementera planen
- utforma och implementera en plan för sjukvårdsregionens arbete med förebyggande insatser och tidig upptäckt av cancer.
Det ursprungliga uppdraget har uppdaterats i och med den långsiktiga inriktningen (Regeringen 2018), där följande 10 prioriterade områden för RCC angavs:
- Prevention och tidig upptäckt
- Rehabilitering, uppföljning och palliativ vård
- Sammanhållna och effektiva vårdprocesser
- Kompetensförsörjning
- Kunskapsstyrning
- Patientinformation
- Ledning och styrning
- Patienter och närstående
- Forskning och innovation
- Barn och unga
En jämförelse med de tidigare kriterierna för RCC visar att 9 av 10 av de prioriterade områdena redan fanns omnämnda i RCC:s kriterier, och utöver dessa tillkommer barncancerområdet.
2.2.4 Strategins syfte och mål
För att mål ska vara ändamålsenliga bör de vara relevanta, tydligt definierade, tidsatta, mätbara och realistiska (Vård- och omsorgsanalys 2023a; Campbell, Braspenning, Hutchinson, och Marshall 2002; Doran 1981).
Cancerstrategin kan sägas ha två syften. Den ska dels bidra till att rusta cancervården för framtida utmaningar, dels uppmärksamma och ta fram insatser för att åtgärda existerande brister i cancervården. Utifrån de två syftena formuleras fem mål.
Målen uppfattas som relevanta, men det finns utrymme för förbättringar
Målen som presenteras i betänkandet En nationell cancerstrategi för framtiden (SOU 2009:11), och som vi tolkar som vägledande för cancerstrategin sedan dess, stämmer till stor del överens med intentionerna i den samlade lagstiftningen inom hälso- och sjukvårdsområdet. Det handlar bland annat om god hälsa utifrån hälso- och livskvalitetsrelaterade behov, vård på lika villkor och att vården ska vara av god kvalitet och bedrivas på ett personcentrerat och patientsäkert sätt. Målen uppfattas i hög grad som relevanta bland de aktörer vi har intervjuat. De utgår dessutom från en gedigen problembeskrivning och tar sikte på det som utredningen En nationell cancerstrategi 2009 uppfattade som aktuella utmaningar i cancervården.
Sedan 2009 har problembilden förändrats i viss utsträckning. Bland annat lyfter flera intervjupersoner fram att regionala skillnader utöver överlevnadstid har blivit mer aktuella i den politiska debatten, och att det är relevant att låta det reflekteras i målen på ett tydligare sätt. Exempelvis är stora regionala skillnader i kvalitet som inte nödvändigtvis påverkar överlevanden (till exempel palliativ vård och rehabilitering) ett område som enligt flera borde lyftas fram.
Framförallt vissa patientorganisationer men även andra aktörer anser att livskvalitet kan lyftas fram tydligare, bland annat mot bakgrund av att cancer allt mer får karaktären av en kronisk sjukdom. Även i andra länders cancerplaner och cancerstrategier som reviderats på senare år betonas att allt fler lever med cancer, och att det innebär förändrade behov.
En möjlighet man skulle kunna ta ställning till är att tydligare lyfta fram livskvalitet genom att formulera två separata mål för livskvalitet respektive överlevnad. Den norska cancerstrategin är ett exempel på detta. Där ingår ett mål om att fler ska överleva och leva längre med cancer, och ett mål om att cancerpatienter och närstående ska ha bästa möjliga livskvalitet (Helse- og omsorgsdepartementet 2018).
Tydligheten kan förbättras
En svaghet i målen är att det inte är tydligt vad som ska betraktas som måluppfyllelse och när målen ska uppnås, med andra ord är de inte särskilt tydligt definierade och inte heller tidsatta. Eftersom målen är förhållandevis ospecifika (med formuleringar om minskat insjuknande och ökad överlevnad) är de sannolikt realistiska, men till priset av en låg konkretion. Vissa av målen är också svåra att mäta och följa upp i sin helhet. Det gäller framför allt kvaliteten i omhändertagandet utifrån ett tydligt patientperspektiv samt livskvalitet. I strategidokumenten specificeras inte lämpliga mått på målen, vilket innebär att det blir otydligt vad som ska räknas som en framgång.
Med tanke på det decentraliserade svenska hälso- och sjukvårdssystemet kan det vara en fördel med inte alltför detaljerade mål, eftersom det lämnar utrymme för anpassningar utifrån regionala behov. Samtidigt finns det en risk att strategins mål tolkas på olika sätt om de uppfattas som vaga bland de aktörer de riktar sig till. Då blir strategin inte ett fullt så effektivt styrverktyg som det annars kunnat vara.
I vår intervjustudie och undersökning till RCC nämner flera att det vore önskvärt att målen operationaliserades i mer konkreta och mätbara delmål och att de eventuellt bör vara föremål för revideringar med tätare tidsintervall än strategin i sin helhet. Ett förslag är till exempel att Socialstyrelsen skulle kunna göra nationella årliga uppdateringar med förslag till mål och åtgärder som underlag till den nationella cancerstrategin. Ett vanligt argument i intervjuerna är att konkreta och mätbara mål blir mer användbara för styrning och för ansvarsutkrävande.
Som jämförelse ställer vissa andra länders cancerstrategier och cancerplaner upp övergripande mål, med delmål kopplade till de olika målen. Den senaste norska cancerstrategin anger till exempel 5 övergripande mål samt 30 mer konkreta delmål (Helse- og omsorgsdepartementet 2018). Vissa av delmålen är relativt allmänt formulerade, medan andra anger kvantitativt formulerade mål som ska uppnås till ett visst år. Den franska cancerstrategin från 2021 specificerar bland annat hur mycket antalet undvikbara cancerfall ska minska till 2040 (Institut national du cancer 2021), och den engelska strategin från 2015 anger bland annat hur mycket 10-årsöverlevnaden ska förbättras till 2020 (Independent Cancer Taskforce 2015). Även i EU:s cancerplan (se avsnitt 6.1) finns sju kvantitativt formulerade och tidsatta mål kopplade till de åtgärdsområden som ingår i planen.
2.2.5 Otydligt vilka områden som är prioriterade
I strategin anges inga områden specifikt som särskilt prioriterade. Det lämnar utrymme för flexibilitet, eftersom utgångsläget kan vara variera mellan regioner, men samtidigt bidrar det till osäkerhet om vilka områden, insatser eller grupper som är högst prioriterade i de lägen man behöver välja. I vissa andra länders strategier förkommer till exempel prioriterade diagnosgrupper. En relaterad fråga som kommit upp i våra intervjuer är också hur strategin förhåller sig till horisontella prioriteringar mellan cancervården och vården i övrigt.
Det saknas stöd för prioriteringar mellan mål
Våra undersökningar visar att cancerstrategins styrdokument inte ger något tydligt stöd för prioriteringar. I betänkandet ställs fem mål upp och inget av dem pekas ut som viktigare än något annat. Möjligtvis var avsikten att prioriteringen skulle tydliggöras i de överenskommelser där strategin operationaliseras.
Vår bedömning av överenskommelserna mellan regeringen och SKR samt RCC:s uppdrag, som det regleras i RCC:s kriterier, är att de visserligen indikerar prioriterade målområden, men att det saknas tydliga och väl underbyggda motiveringar till de prioriteringar som framställs. Fokus för överenskommelserna har skiftat över tid men vi har inte undersökt hur aktörerna i vår undersökning har upplevt variationen.
En återkommande synpunkt i våra intervjuer och i tidigare uppföljningar är att det inte upplevs som möjligt för regionerna att implementera den kunskapsstyrning som RCC förmedlar genom vårdprogram och standardiserade vårdförlopp fullt ut. Därmed krävs det prioriteringar där man väljer att fokusera på vissa områden eller insatser framför andra. Samtidigt finns en osäkerhet om vilka delar av RCC:s kunskapsstyrning som är högst prioriterade. Ett exempel som återkommer i både intervjuer och myndigheters uppföljning är hur cancerpatienters väntetider borde prioriteras jämfört med andra saker, och om ledtidsmålet för de standardiserade vårdförloppen är en korrekt prioritering (Riksrevisionen 2023; Socialstyrelsen 2023a).
Prioriteringar mellan patientgrupper
Cancerstrategin kan tydligare specificera vad som bör uppnås i relation till olika grupper bland personer med cancer, och om det finns grupper som särskilt behöver prioriteras framöver. En faktor som våra intervjupersoner har lyft fram och som framgår av andra länders cancerplaner, är att olika grupper bland cancerpatienter och canceröverlevare har olika behov, exempelvis beroende på ålder. Nyare strategier i andra länder pekar särskilt på att allt fler som får cancer är äldre personer med flera sjukdomar, som har andra behov av vård och stöd än yngre personer som är i övrigt friska (Helse- og omsorgsdepartementet 2018; Independent Task Force 2015; Scottish Government 2016).
I betänkandet En nationell cancerstrategi för framtiden (SOU 2009:11) tas inte heller ställning till om några patientgrupper utifrån sina behov är särskilt prioriterade. En synpunkt som framkommer i vår kartläggning är att cancer är ett trubbigt begrepp och att det finns skillnader i behov mellan olika cancerformer. I vissa andra länders cancer- strategier finns särskilt prioriterade patientgrupper. I den franska cancerstrategin är till exempel ett mål att signifikant förbättra överlevnadschansen för de cancerformer som har sämst prognos (Institut national du cancer 2021).
Det saknas stöd för prioriteringar gentemot områden utanför strategin
I våra intervjuer tar flera upp frågan om horisontella prioriteringar mellan cancervården och vården i bredare perspektiv. Vissa aktörer ifrågasätter lämpligheten i att det finns en särskild strategi för cancervården. De menar att cancer är ett relativt välfungerande område och att ett alltför starkt fokus på cancer från nationell nivå kan påverka andra områden negativt. Det gäller särskilt mot bakgrund av den positiva utvecklingen i över- levnaden efter en cancerdiagnos.
I takt med att vissa cancerdiagnoser alltmer får karaktären av en kronisk sjukdom kan det enligt vissa aktörer finnas skäl att överväga att tillämpa liknande arbetssätt som för andra kroniska sjukdomar. Det kan till exempel handla om att omhänderta patienter med kronisk cancer i den nära vården och att rehabilitering kanske inte behöver ske cancerspecifikt. I vissa andra länder har man valt att ta fram strategier för flera stora folksjukdomar, där cancer ingår som ett av flera sjukdomsområden. England beslutade exempelvis att istället för en reviderad 10-årsplan mot cancer ta fram en strategi för 6 stora folksjukdomar. Beslutet motiverades bland annat med att man ville främja ett helhetsperspektiv på patienten och motverka vårdens stuprörsorganisering (Department of Health and Social Care 2023a). I Norge har man valt att kombinera en cancerspecifik strategi med en bredare strategi för att förebygga icke-smittsamma kroniska sjukdomar, vilket kopplas till att riskfaktorerna för olika sjukdomar i hög grad överlappar (Helse- og omsorgsdepartementet 2018).
Ett argument för en särskild strategi på cancerområdet är att cancervården ska ”gå före” med att tillämpa nya arbetssätt och därmed bidra med lärande till hälso- och sjukvården i övrigt. Samtidigt menar vissa intervjupersoner och andra informanter att det finns anledning att stärka strukturerna för sådan kunskapsöverföring, både för att se till att arbete på cancerområdet kommer resten av vården till del och för att kunskapsstyrningen inom cancerområdet ska lära av andra vårdområden. De pekar på ett behov av att integrera kunskapsstyrningen av cancervården mer i kunskapsstyrningen på andra områden, med en gemensam målbild.
2.2.6 Operationaliseringen av strategins mål i insatser
För att målen ska uppnås krävs att en strategi pekar ut insatser som kan förväntas bidra till måluppfyllelsen. För att tydliggöra värdet av implementering för de berörda aktörerna är det en fördel om insatserna är tydligt motiverade utifrån problembilden och att det framgår vilken prioritet de har. De konkreta insatser som föreslås i betänkandet från 2009 motiveras tydligt utifrån de behov som beskrivs. Däremot är insatser i högre grad konkretiserade inom vissa av målen. I genomförandet av cancerstrategin har vissa områden varit mer i fokus än andra, och fokus har förändrats över tid. Vi kan inte bedöma om det är motiverat.
I det här avsnittet redovisar vi en sammanställning av de insatser som beskrivs i den nationella styrningen utifrån deras koppling till cancerstrategins fem mål, för att få en bild av vilka områden som prioriterats i implementeringen av strategin. Mängden insatser som beskrivs i den nationella styrningen behöver inte spegla hur mycket arbete som skett inom olika områden i regionerna. Vi har inte kartlagt de insatser som regionerna själva beslutat om, men eftersom större delen av RCC:s verksamhet styrs av de nationella överenskommelserna (SKR 2021a) bör sammanställningen ändå kunna ge en bild av inriktningen på arbetet inom cancerområdet.
Vissa mål har varit mer i fokus
Sammantaget ser vi att det finns mål i cancerstrategin som varit mindre i fokus för den nationella styrningen, sett till hela perioden. Det gäller framför allt målet om skillnader mellan befolkningsgrupper, men även i viss mån målet om minskad risk för insjuknande. Den nationella styrningen för att genomföra cancerstrategin har främst riktats mot insatser för ett förbättrat omhändertagande, överlevnad och livskvalitet för cancerpatienter, minskade regionala skillnader samt övergripande frågor som berör alla målen.
De områden som varit mindre i fokus har dock ingått i RCC:s uppdrag hela perioden, och det framgår av uppföljningar att RCC arbetat särskilt med rehabilitering och palliativ vård. De områdena tar större plats i överenskommelserna efter den långsiktiga inriktningen och ingår även i RCC:s inriktning från 2018.
Vi har noterat i vår undersökning om patientmedverkan inom hälso- och sjukvården (Vård- och omsorgsanalys 2024) att personer med erfarenhet av patient- och närståenderåd inom RCC ofta efterfrågar ett ökat fokus på andra delar av vårdprocessen än enbart behandling. De lyfter fram bland annat tidig upptäckt, diagnostisering och rehabilitering.
För närmare beskrivningar av insatser som skett inom cancerområdet, se kapitel 3.
Tabell 2. Områden med fler och färre insatser i den nationella styrningen sett till hela perioden 2009–2023.
| Mål 1: Minska risken för insjuknande i cancer | Mål 2: Förbättra kvaliteten i omhändertagandet | Mål 3: Förlänga överlevnadstiden och förbättra livskvaliteten | Mål 4: Minska regionala skillnader i överlevnadstid | Mål 5: Minska skillnader mellan befolkningsgrupper i insjuknande och överlevnadstid | Områden som berör samtliga mål | |
|---|---|---|---|---|---|---|
| Områden med fler insatser |
|
Många insatser:
|
Många omfattande insatser riktade mot överlevnad | Ingår som del i många insatser | Delmål för vissa aktiviteter kring deltagande i screening |
|
| Områden med färre insatser | Levnadsvanor | Livskvalitet palliativ vård och rehabilitering | Saknas i stort sett insatser i nationella styrningen | Kompetensförsörjning |
RCC:s uppdrag gäller alla mål
RCC:s uppdrag som det definieras i kriterierna från 2011 berör samtliga mål i cancer- strategin. Särskilt fokus ligger på bättre omhändertagande och stärkt ställning för patienter, samt målövergripande frågor om kunskapsstöd och uppföljning.
Det ursprungliga uppdraget har uppdaterats i och med den långsiktiga inriktningen, där 10 prioriterade områden för RCC angavs. Förutom de områden som ingick i det ursprungliga uppdraget har barncancer tillkommit. Utifrån de här områdena har RCC i samverkan (2023d) formulerat en rad mål och prioriterade insatser för de kommande åren. Även de berör samtliga mål i cancerstrategin, men särskilt fokus ligger på målet om överlevnad och livskvalitet, målet om förbättrat omhändertagande samt övergripande frågor som berör alla mål.
Fokus för överenskommelser och myndighetsuppdrag
Bland de insatser som beskrivs i överenskommelser och myndighetsuppdrag under perioden 2009–2023 handlar en stor andel om målet om bättre omhändertagande, målet om förbättrad överlevnad och livskvalitet samt övergripande strukturella frågor som berör alla målen i strategin. Många av dessa insatser handlar också om minskade skillnader mellan regioner. Målet om minskade skillnader mellan olika grupper i befolkningen i insjuknande och överlevnad har bara ingått som en del i vissa insatser kring screening.
De ekonomiska medlen i överenskommelserna
Överenskommelserna mellan regeringen och SKR har omfattat omkring 500 miljoner varje år. Det är inte möjligt att jämföra hur ekonomiska medel fördelats mellan cancerstrategins mål. Skälet är att insatserna inte alltid är uttalat kopplade till ett visst mål, ofta syftar till att uppnå flera mål, och de ekonomiska medlens fördelning mellan insatsområden redovisas på olika sätt under perioden. Efter 2015 har merparten av de ekonomiska medlen i överenskommelserna varit kopplade till väntetidssatsningen, främst de standardiserade vårdförloppen.
Fokus för insatserna har förändrats över tid
Vilka områden som framstår som mest prioriterade i den nationella styrningen skiljer sig mellan olika perioder. Sammanfattningsvis var insatserna i överenskommelser och myndighetsuppdrag under den första delperioden 2010–2013 relativt jämnt fördelade mellan alla målen, utom målet om minskade skillnader mellan grupper i befolkningen där det överlag saknats insatser i överenskommelserna. Särskilt fokus låg på att bygga upp strukturer för kunskapsstyrning genom RCC, vårdprogram med mera. Från 2015 och framåt skedde ett skifte i fokus över till förbättrat omhändertagande, där de standardiserade vårdförloppen stod i centrum. Sedan 2020 har överlevnad och livskvalitet varit mer i fokus, med bland annat insatser inom vårdprogrammen för rehabilitering och palliativ vård.
Under åren efter den långsiktiga inriktningen (Regeringen 2018) syns ett ökat fokus i överenskommelserna på rehabilitering och palliativ vård, samt ett mer samlat grepp om cancerprevention som rör ohälsosamma levnadsvanor i form av RCC:s nationella preventionsplan. En särskild satsning på barncancer ingår också sedan 2019. Insatser inom barncancer har tidigare bara i undantagsfall ingått i överenskommelserna på cancerområdet.
Eftersom förändringarna i fokus över tid inte tydligt motiveras i överenskommelserna vet vi inte vilka avvägningar som ligger till grund för prioriteringarna. Utvecklingen över tid kan ses som naturlig i och med att det kan vara aktuellt att hitta nya inriktningar i takt med att tidigare insatser genomförs. Det skulle till exempel kunna förklara varför uppbyggnaden av strukturer varit mer i fokus i början av perioden, och fokus sedan skiftat till andra insatser.
2.3 Struktur för genomförande
Strategier är inte något formellt styrinstrument. Genomslaget för en strategi beror följaktligen på vilka styråtgärder som kopplas till strategin. Styrningen genom cancerstrategin kan sägas gå genom tre nivåer (se figur 1). Styrningen utgår från den nationella cancerstrategin, som i sin tur operationaliseras i styrningen genom överenskommelser, regeringsuppdrag, lagstiftning och inrättandet av en nationell samordnare och RCC med vissa ansvarsområden. De här styrkanalerna avgör i sin tur vilka insatser som ska genomföras. Till en del kan det handla om åtgärder som föreslagits i cancerstrategin, samtidigt som det kan handla om insatser som finns med i överenskommelser men som inte fanns med i betänkandet från 2009.
Figur 1. Styrningen genom cancerstrategin
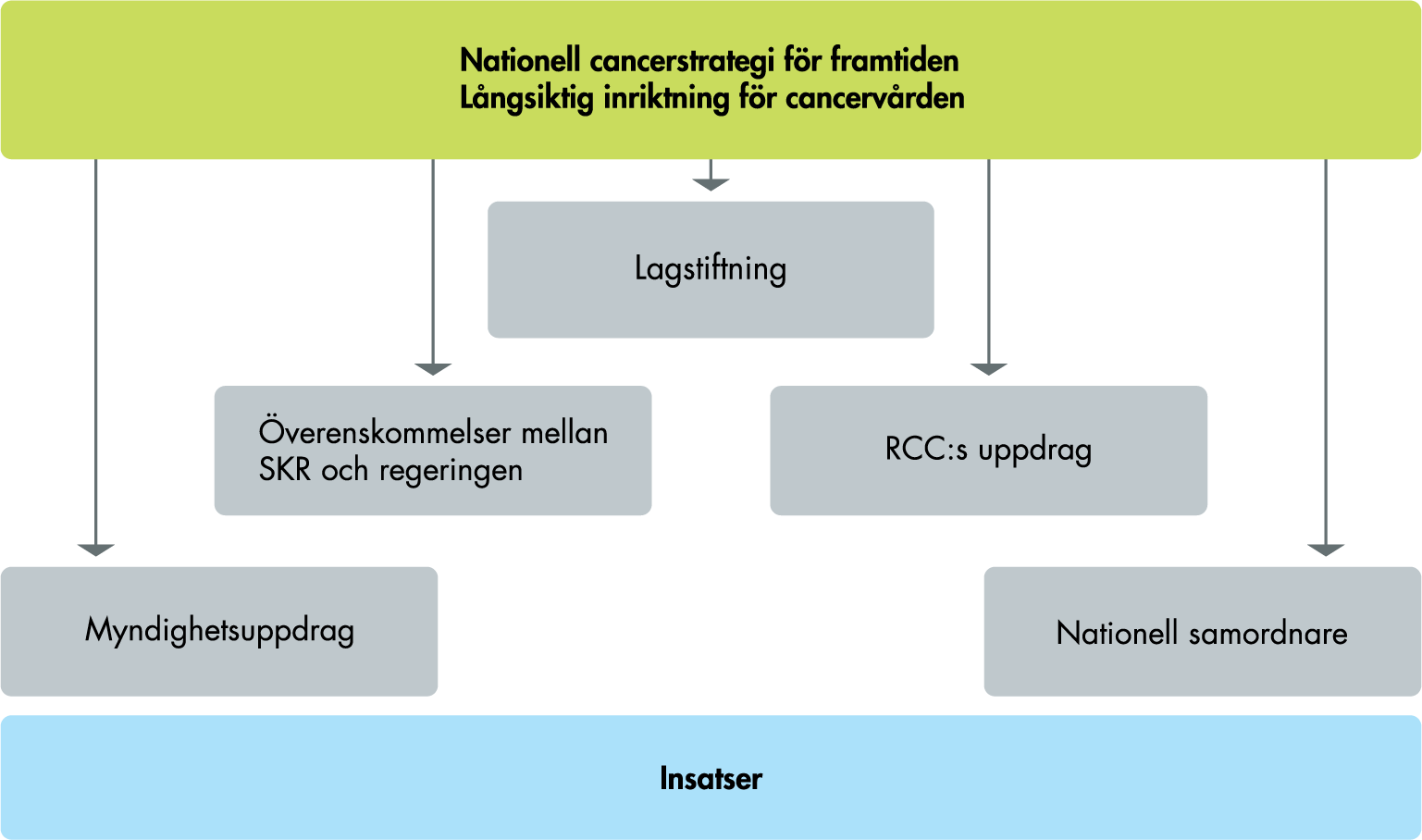
I betänkandet föreslogs att regeringen och sjukvårdshuvudmännen skulle sluta en överenskommelse om den nationella cancerstrategin. Den huvudsakliga formen för genomförandet av cancerstrategin på nationell nivå har varit årliga överenskommelser mellan regeringen och SKR (tidigare SKL), där aktiviteter och finansiering specificeras. Implementeringen i regionerna sker i stor utsträckning genom de respektive RCC som tar fram regionala cancerplaner och stödjer implementeringen i regionerna. I studien fokuserar vi på den nationella nivån och kan därför inte uttala oss om genomförandet ur ett regionalt perspektiv.
2.3.1 Rollfördelningen mellan de aktörer som ska genomföra strategin är tydlig, men ansvaret är mer oklart
Vår bedömning är att rollerna i huvudsak är tydliga i strategin. På vissa områden pekas dock oklar ansvarsfördelning ut som ett problem både i intervjuer och tidigare uppföljning, framförallt inom området prevention som rör ohälsosamma levnadsvanor. Det är även oklart vilket ansvar som regionerna har i implementeringen och för måluppfyllelsen. I överenskommelserna är det inte tydligt vad regionerna åtar sig att göra.
Det är i första hand RCC som har ansvaret för kunskapsstyrning, att utveckla vårdprocesserna och dialog med regionerna. Myndigheternas uppdrag har huvudsakligen gått ut på att stötta med kompletterande strukturer och uppföljning.
RCC har en nyckelroll i att implementera cancerstrategin
De sex regionala cancercentrumen och deras lednings- och samverkansfunktion RCC i samverkan har en central roll i arbetet med att genomföra den nationella cancerstrategin, och är en struktur för kunskapsstyrningen av cancervården.
För merparten av de insatser som definieras i överenskommelserna på cancerområdet under perioden anges RCC-strukturen som den aktör som ska genomföra insatsen. Det handlar till exempel om att stödja, stimulera, främja, och samordna olika processer i regioner och sjukvårdsregioner, göra analyser, ta fram dokument som vårdprogram och standardiserade vårdförlopp för att sedan främja implementeringen av dem, samt ta fram nationella och regionala planer och arbeta för implementeringen av dem (Socialdepartementet och SKR/SKL 2015–2023, Socialdepartementet 2011).
RCC-organisationen
Det finns ett RCC i varje sjukvårdsregion. Antalet regioner som varje RCC arbetar mot varierar därmed. Förutsättningar och arbetssätt skiljer sig åt mellan de olika RCC. Samtliga sex RCC har dock sjukvårdsregionala processledare som har en nyckelroll i arbetet med att förbättra vårdprocessen för patienter inom en viss process eller viss diagnos i sjukvårdsregionen. Processledarna delar ofta sin tid mellan RCC och den kliniska verksamheten (Socialstyrelsen 2023a).
Arbetet inom RCC-organisationen sker i stor utsträckning i arbetsgrupper bestående av främst kliniskt verksamma. RCC erbjuder stödfunktioner. Större delen av det operativa arbetet på nationell nivå sker i de omkring 100 nationella arbetsgrupperna, bland annat nationella vårdprogramgrupper. Ansvaret för olika verksamhetsområden, till exempel nationella arbetsgrupper och kvalitetsregister för en viss cancerdiagnos, är fördelat mellan de olika RCC men stöds också av RCC i samverkan (SKR 2021a).
RCC i samverkan samordnar RCC:s arbete nationellt. RCC i samverkan består av RCC-cheferna och den nationella cancersamordnaren, och stöds av det så kallade ”cancerteamet” på SKR. Alla beslut fattas i konsensus och man har inget mandat att direkt styra de olika RCC, utan fungerar mer som en stödfunktion. Däremot har RCC i samverkan i praktiken en viktig roll i förhandlingarna om överenskommelserna på cancerområdet mellan regeringen och SKR (SKR 2021a).
RCC:s verksamhet finansieras huvudsakligen med medel från nationell nivå, men får också medel från regionerna utifrån deras prioriteringar. RCC:s verksamhet styrs huvudsakligen av den nationella cancerstrategin och överenskommelserna mellan regeringen och SKR. Regionerna har dock ansvar för ekonomi och redovisningar för respektive RCC (SKR 2021a). RCC:s uppdrag definieras i 19 kriterier och 10 prioriterade områden (se avsnitt 2.2.3).
RCC har ett bredare uppdrag än exempelvis de senare programområdena inom kunskapsstyrningsorganisationen (SKR 2021a). Socialstyrelsen bedömde 2016(b) att det breda uppdraget fört med sig en helhetssyn på patienten. Samtidigt påpekade Socialstyrelsen att RCC:s uppgifter, som de definieras i kriterierna från 2011, inkluderar delar som är svåra för RCC att påverka. Särskilt områden som kompetensförsörjning och prevention som rör ohälsosamma levnadsvanor kräver samverkan med andra aktörer. I uppföljningarna kritiserar flera att RCC har ett uppdrag som är bredare än dess mandat att påverka (Socialstyrelsen 2016a, 2021d). Det bekräftas i vår undersökning till RCC, som visar att det finns ett behov av att förtydliga uppdrag och ansvarsfördelning mellan olika aktörer, särskilt inom områden som involverar många aktörer. Socialstyrelsen (2021d) bedömer dock sammantaget att det breda uppdraget är en tillgång.
I betänkandet från 2009 syftar ”cancercentrum” på centrum som bedriver både kunskapsstyrning, vård och forskning, det vill säga både det som RCC idag gör och det som universitetssjukhus eller Comprehensive Cancer Centres (CCC) gör (se 6.2). I samband med inrättandet valde man att istället att ge RCC en mer renodlad roll inriktad på kunskapsstyrning. I vår intervjustudie betonas att det var en pragmatisk lösning med stöd i samtliga regioner. Alla RCC utom Stockholm-Gotland är i dag organisatoriskt placerade utanför linjeorganisationen (Socialstyrelsen 2023a).
Regionernas roll
Strategin har till största delen operationaliserats i överenskommelser mellan regeringen och regionerna (representerade av SKR). Regionerna är som huvudmän de aktörer som förväntas besluta om att genomföra det mesta av cancerstrategin, t.ex. att införa standardiserade vårdförlopp och att implementera innehållet i vårdprogrammen. Samtidigt är det sällan som regionernas ansvar pekas ut i överenskommelserna, utan det som specificeras är främst hur RCC ska arbeta för att stödja regionerna. Ändå är det regionerna som i första hand är de aktörer som behöver fatta de beslut som i realiteten genomdriver den förändring som strategin och RCC pekar ut.
Däremot omfattar överenskommelserna ekonomisk styrning där huvuddelen av medlen i överenskommelserna har gått till regionerna (Riksrevisionen 2023). Delar av de ekonomiska medlen har betalats ut direkt till regionerna villkorat med exempelvis införande av standardiserade vårdförlopp (SVF) (Socialdepartementet och SKL/SKR 2015–2018). I de senaste överenskommelserna finns skrivningar om att regionerna ska arbeta för att nå inklusions- och ledtidsmålen i SVF.
Enligt våra intervjuer och även tidigare utvärderingar framstår genomslaget för RCC:s kunskapsstyrning i regionerna som en svaghet. Vår undersökning har inte omfattat regionerna, så vi saknar närmare kunskap om varför det ser ut så. En möjlig förklaring som kommer fram i våra intervjuer och i undersökningen till RCC är att det bristande genomslaget kan vara kopplat till att styrningen inte är eller uppfattas som tillräckligt bindande av regionerna. Trots det gemensamma arbetet genom RCC ska vårdprogram och andra kunskapsstöd anpassas i respektive region. Det skapar både en tröghet i systemet och bristande jämlikhet, eftersom respektive region ytterst beslutar om hur vården ska utformas och prioriteras. Flera anser att RCC:s begränsade mandat är en svaghet, där RCC bara ger rekommendationer men inte kan fatta några beslut om åtgärder som ska genomföras i verksamheterna. Flera upplever att det är svårt att få verkan av RCC:s styrning i regioner och verksamheter samt att det är ännu svårare när det gäller kommunerna. Det kan också vara så att det saknas kapacitet i regionerna att ta hand om kunskapen på verksamhetsnivå, till exempel på grund av svårigheter med kompetensförsörjningen, eller att det saknas det ledningsstöd som krävs med verksamhetschefer som stöttar implementeringen lokalt. Det finns också många konkurrerande perspektiv i primärvården där cancerpatienter är en patientgrupp bland många.
Myndigheter har haft uppdrag men inte övergripande ansvar
Vi har gjort en översiktlig inventering av de uppdrag regeringen gett statliga myndigheter kopplat till cancerstrategin. Uppdragen till myndigheter har berört de flesta områden i cancerstrategin, men varit särskilt inriktade på uppbyggnad och stöd till RCC-strukturen, uppföljning samt kunskapsutveckling och innovation.
Socialstyrelsen har bedrivit mest arbete och haft ett bredare fokus inom cancerområdet, medan Tandvårds- och läkemedelsförmånsverket (TLV) och Vinnova haft vissa uppdrag kopplade till medicinsk teknologi, läkemedel samt innovation och forskning. Folkhälsomyndigheten och Strålsäkerhetsmyndigheten har haft roller inom prevention som rör ohälsosamma levnadsvanor. Även andra myndigheter, som E-hälsomyndigheten och Inspektionen för vård och omsorg (IVO), bedriver verksamhet som berör cancerområdet (Socialstyrelsen 2021b).
Bland myndigheterna har Socialstyrelsen haft den bredaste rollen. Samtidigt beskriver Socialstyrelsen i våra intervjuer att myndigheterna överlag inte har någon omfattande roll på cancerområdet. Socialstyrelsen (2021b) finner i en kartläggning med utgångspunkt i Rådet för styrning med kunskap (som består av 10 myndigheter på hälso- och sjukvårdens och socialtjänstens område) att flera av myndigheterna som ingår i rådet inte har cancerspecifika uppdrag. Myndigheterna har inte organisatoriska funktioner som är särskilt inriktade på cancerfrågor. Socialstyrelsen beskriver i intervjuer att i och med att kunskapsstyrningen övergått till RCC-organisationen arbetar färre personer på Socialstyrelsen med cancerfrågor. Sedan RCC började ta fram vårdprogram har Socialstyrelsen till exempel avvecklat sitt arbete med nationella riktlinjer på cancerområdet.
Lagändringar och andra initiativ på statlig nivå
Cancerområdet berörs även av andra statliga initiativ. Vi har inte gjort någon omfattande kartläggning, men det finns vissa initiativ som har pekats ut i anslutning till cancerstrategin. I betänkandet presenterades förslag om höjd åldersgräns för solarier och åtgärder för tobaksprevention: höjda priser på tobak, rökfria miljöer, marknadsföringsförbud samt varningstexter och bildillustrationer på tobaksförpackningar. Flera av förslagen har genomförts sedan cancerstrategin togs fram, men alla förändringar är inte kopplade till cancerstrategin specifikt.
Flera bredare initiativ har skett inom folkhälsoområdet, som kan påverka insjuknandet i cancer. I den långsiktiga inriktningen pekar regeringen (2018) bland annat på primärvårdens lagreglerade grunduppdrag, där förebyggande arbete ingår, och uppdraget till Socialstyrelsen att stödja implementeringen av sina riktlinjer för prevention och behandling vid ohälsosamma levnadsvanor (se även avsnitt 3.1.2).
Patientmedverkan har ökat men kan bli bättre
Patientmedverkan och närståendemedverkan har pekats ut som framgångsfaktor för lärande, patientperspektiv och processarbete i uppföljningar av insatser på cancerområdet (Socialstyrelsen 2016a, 2021d, 2023a). Varje RCC har ett patient- och närståenderåd. Patient- och närståenderepresentanter deltar också i många av de nationella vårdprogramgrupperna och i de vårdprocessgrupper som är knutna till de olika RCC (RCC i samverkan 2023a).
Inrättandet av RCC bedöms ha inneburit en förbättring när det gäller patientmedverkan, genom att man institutionaliserat patientmedverkan och drivit de perspektiven (Socialstyrelsen 2017, 2016b, 2021d). Utifrån vår undersökning av patient- och närståendemedverkan inom hälso- och sjukvården, där bland annat ledamöter i RCC:s patient- och brukarråd ingår, framstår det som att patient- och närståendemedverkan är jämförelsevis väl organiserad (Vård- och omsorgsanalys 2024). Medverkande från RCC:s råd tycks överlag ha en mer positiv bild än personer i andra patient- och närståenderåd när det gäller faktorer som tydlighet i rollerna och att patient- och närståenderepresentanters perspektiv tas tillvara.
De patient- och närståendeorganisationer som vi varit i kontakt med har olika uppfattningar om hur väl patientmedverkan fungerar inom RCC. Vissa av dem lyfter fram att RCC har ett bra upplägg och är en bra ingång för patientorganisationerna. Andra uppfattar organisationen som stelbent och icke lyhörd. Socialstyrelsen (2021d) har tidigare bedömt att även om patientmedverkan utvecklats väl över tid så finns fortfarande förbättringspotential, till exempel att ytterligare formalisera patientmedverkan, arbeta för mer heterogen representation och öka kunskapen om nyttan med patientmedverkan inom vården.
Olika uppfattningar om rollfördelningen i strategin
Aktörerna som vi har intervjuat har olika bilder av om rollfördelningen på cancerområdet varit tydlig. De pekar dock på RCC som avgörande för den utveckling som har skett inom cancerområdet. Socialstyrelsen uppfattar att RCC fungerat väl som en länk mellan den statliga och regionala nivån, och flera patientorganisationer uppfattar RCC som en tydlig ingång för dem. En framgångsfaktor enligt intervjupersoner har varit att RCC lutar sig mot cancerstrategin, med ett tydligt uppdrag och resurser. RCC:s breda uppdrag anknyter också tydligt till cancerstrategin (Socialdepartementet 2011). Att RCC, till skillnad från vad som föreslogs i betänkandet, fokuserat på kunskapsstyrning på övergripande nivå har enligt vissa av våra intervjupersoner varit positivt för att ge RCC en tydlig roll.
Samtidigt anser intervjupersoner och andra informanter också att RCC:s mandat, samt styrningen och organiseringen är oklara. De menar att det totalt sett finns många olika aktörer, men att det är otydligt vem som styr över resurser och har mandat att fatta beslut. I Socialstyrelsens (2023a) analys framkommer även att det finns tolkningsutrymme i överenskommelserna om hur RCC ska arbeta. Socialstyrelsen ser därför ett behov av att i en reviderad cancerstrategi och i kommande överenskommelser tydliggöra RCC:s uppdrag och handlingsutrymme i relation till regionerna, de andra nationella programområdena inom kunskapsstyrningen och myndigheterna.
Rollfördelningen uppfattas som mer oklar inom vissa av strategins målområden. Det handlar framför allt om områden som är bredare än cancerområdet och där det kan finnas många aktörer som är involverade, till exempel prevention som rör ohälsosamma levnadsvanor, rehabilitering och palliativ vård. Kommissionen för jämlik hälsa (2017) menade att uppdragen inom folkhälsa generellt var otydliga. Socialstyrelsen (2023a) pekar på att Folkhälsomyndighetens roll inom cancerprevention upplevs som oklar inom RCC, vilket gör det svårt att identifiera RCC:s roll. Även i vår undersökning till RCC framkommer önskemålet att Folkhälsomyndigheten får ett tydligt samordningsuppdrag för prevention som rör ohälsosamma levnadsvanor.
Flera av de aktörer vi intervjuat menar att det finns ett behov av ett tydligare formulerat uppdrag för någon aktör på en rad delområden. Det gäller särskilt områden som uppfattas som svaga eller där utvecklingen uppfattas ha gått långsamt. Socialstyrelsen nämns som förslag på en sådan aktör. Att Socialstyrelsens roll minskat kan vara positivt för att undvika dubbelarbete och dubbla styrsignaler. Samtidigt innebär avvecklandet av de nationella riktlinjerna att det inte finns någon aktör som ansvarar för prioriteringsstöd på cancerområdet. Just behovet av en aktör på övergripande nivå som kan ta ställning till de horisontella prioriteringarna var något som särskilt lyftes fram vid vårt resultatseminarium.
2.3.2 Ansvariga aktörer har begränsade möjligheter att genomföra strategin
För att en strategi ska få önskat genomslag behöver de aktörer som ska stå för utförandet ha förutsättningar att göra det. Bland annat behöver individen eller gruppen som berörs av målet ha en viss kontroll över resultaten, så att målet går att påverka (Latham och Locke 2006). Med andra ord behövs ett tydligt mandat, och också förutsättningar att bedriva den verksamhet man ska, samt möjlighet att påverka förutsättningarna för implementeringen. Eftersom RCC-organisationen har en nyckelroll i implementeringen av cancerstrategin blir framförallt RCC:s förutsättningar viktiga.
RCC saknar beslutsmandat men är fristående
En utmaning för RCC som återkommit i uppföljningar sedan inrättandet är att RCC och dess processledare inte ingår i de regionala linjeorganisationerna och därför saknar mandat att styra verksamheterna (Socialstyrelsen 2014a, 2016a, 2021d, 2023a). Även på områden där RCC har ett tydligt ansvar blir det enligt vissa av våra intervjupersoner svårt för RCC att nå ut till vården. Patientorganisationer, men även andra aktörer, pekar på att styrningen av till exempel vårdförloppen och vårdprogrammen inte är mer bindande. Det upplevs att det är svårt att få verkan av RCC:s styrning i regioner och verksamheter och ännu svårare i kommunerna. Ett exempel är att RCC kan ta fram uppdragsbeskrivning för kontaktsjuksköterska men inte se till att respektive region anställer och skapar förutsättningar för sådana att arbeta enligt uppdragsbeskrivningen.
Samtidigt är bristande genomslag för kunskapsstyrning en utmaning även i ett bredare perspektiv än i cancervården, till exempel när det gäller nationella riktlinjer (SOU 2017:47). Med tanke på att det är svårt att nå ut med kunskapsstyrning i det decentraliserade hälso- och sjukvårdssystemet, uppfattar många RCC:s arbete som framgångsrikt givet att det är regionerna som har mandatet.
Intervjupersoner och andra informanter beskriver samtidigt att det är en styrka att RCC är en fristående part i dialog med andra aktörer. Vissa menar att det hade varit svårare att få verksamheterna att anamma vårdprogram och processutveckling om RCC haft en annan roll. Socialstyrelsen (2023a) konstaterar också utifrån intervjuer att RCC-representanter inte beskriver avsaknaden av beslutsmandat som något större problem. Det samverkansinriktade arbetssätt man har idag uppfattas som välfungerande. RCC- representanterna menar att det inte vore önskvärt att ”peka med hela handen”, eftersom arbetet ändå måste förankras hos dem som ytterst ska genomföra det, och att det snarare är detta som är utmaningen (Socialstyrelsen 2023a).
I avsaknad av mandat är RCC:s möjligheter att påverka beroende av samverkan, dialog, förankring och kommunikation med verksamheter och regionledningar. Ett framgångsrikt genomförande av olika insatser kopplas i uppföljningar till medverkan från professionen samt dialog och förankring på olika nivåer i verksamheterna. Kopplingen till linjeorganisationen lyfts återkommande fram i uppföljningar, och det beskrivs som en framgångsfaktor att lokala processledare även är kliniskt verksamma (Socialstyrelsen 2014a, 2016a, 2016b).
I vår undersökning till RCC nämns att viktiga element i RCC:s samarbete med regionerna är en bred representation från de regioner som omfattas av respektive RCC, att den nationella cancerstrategin omsätts i regionala cancerplaner och att det finns regionala cancersamordnare som har en nyckelroll när det gäller att ta emot och införa kunskapsstöd och insatser men också för att identifiera frågor som behöver lyftas till nationell nivå. De regionala planerna underlättar enligt Socialstyrelsens (2021d) intervjuer för RCC att få genomslag, eftersom de visar på politisk vilja. Relationen till regionledningarna har lyfts fram som viktig, och under införandeprocessen har Socialstyrelsen (2014a, 2014c, 2016a) efterfrågat mer stöd till RCC från regionerna.
En faktor som gett förutsättningar för RCC att arbeta långsiktigt är att RCC haft en god och långsiktig finansiering (Socialstyrelsen 2021d). Även den höga kompetensen inom RCC-organisationen har lyfts fram som en framgångsfaktor (Socialstyrelsen 2016b, 2021d). Samtidigt beskrivs de olika RCC:s skilda förutsättningar, exempelvis resurser och antal regioner i sjukvårdsregionen, som en svårighet för samverkan mellan RCC. De skilda förutsättningarna ställer enligt våra intervjupersoner krav på att man försäkrar sig om att exempelvis de nationella arbetsgrupperna har likvärdiga förutsättningar, trots att förutsättningarna skiljer sig åt mellan de RCC som har värdskapet. Ett allt vanligare problem är också att någon eller några regioner saknar representant i arbetsgrupper, på grund av problemen med kompetensförsörjning.
Förtroendet för RCC beskrivs som starkt i flera av våra intervjuer, och även i Socialstyrelsens uppföljningar (Socialstyrelsen 2016b, 2021d). Samtidigt upplever flera intervjupersoner att RCC:s ställning är försvagad. Även om RCC haft en stor betydelse, så kan det enligt vissa finnas anledning att se över modellen mot bakgrund av framväxten av CCC:er och risken för att RCC glider längre ifrån vården och blir mer av en administrativ stödfunktion. Samtidigt betonar andra att det är viktigt att inte göra förändringar som förstör de strukturer som byggts upp (se även avsnitt 6.2).
Strukturella hinder påverkar genomslaget för cancerstrategin
Cancerstrategin är inriktad på en diagnos, men genomslaget är beroende av hela hälso- och sjukvårdssystemet. Flera av de svagheter vi har tagit upp här är kopplade till strukturella utmaningar i hälso- och sjukvården. I uppföljningar under perioden återkommer kompetensbristen i vården, och generella utmaningar med fragmentariska och icke ändamålsenliga it-system och register som faktorer som försvårat genomförandet av insatserna inom cancerstrategin.
Brist på personal med rätt kompetens är inte bara en fråga för cancervården, utan en generell utmaning. Redan i betänkandet lyfte man fram att utvecklingen med ett ökat antal cancerpatienter och framsteg inom behandlingar kommer att medföra utmaningar med kompetensförsörjning och resurser. Däremot presenterades inga konkreta förslag på området. Enligt våra intervjuer och vår undersökning till RCC kan RCC påverka kompetensutvecklingen inom cancervården, men inte dimensioneringen av anställda, som är regionernas ansvar. Även Socialstyrelsen har i sin uppföljning pekat på att kompetensförsörjning är en fråga som regionerna ansvarar för och som RCC har begränsade möjligheter att påverka.
Vi har ovan nämnt att strategin inte åtföljs av stöd för horisontella prioriteringar, vilket skapar osäkerhet och bristande legitimitet för genomförandet. Det är liksom kompetensförsörjningen inte en fråga som bara berör cancervården, utan något som är en generell utmaning inom hälso- och sjukvården (Vård- och omsorgsanalys 2020).
Ytterligare ett strukturellt hinder som påverkat genomförandet är primärvårdens bristande kapacitet. Det har exempelvis funnits utmaningar med att införa SVF i primärvården, och flera beskriver primärvårdens förutsättningar som otillräckliga när det gäller till exempel det preventiva arbetet och rehabilitering. Det framgår av vår intervjustudie och i undersökningen till RCC, liksom i tidigare uppföljningar (se till exempel Vård- och omsorgsanalys 2023b och Socialstyrelsen 2021d, 2023a).
Vissa aktörer efterfrågar mer statlig styrning
Flera intervjupersoner menar att det bristande genomslaget för kunskapsstyrningen motiverar ett tydligare statligt ansvarstagande på en rad delområden som rör cancervården. Många som vi intervjuat efterfrågar även en ökad statlig styrning eller samordning på cancerområdet för att öka jämlikheten mellan regioner och att stärka styrningen inom områden där utvecklingen uppfattas ha gått långsamt, till exempel prevention som rör ohälsosamma levnadsvanor, screening, rehabilitering och palliativ vård. Det gäller det man uppfattar som statens generella ansvar för en jämlik vård och hälsa där både mål och uppföljning av måluppfyllelse borde vara ett statligt ansvar. Aktörerna menar att staten skulle kunna bidra till att utjämna skillnaderna i förutsättningar mellan regionerna. Vissa menar också att det decentraliserade sjukvårdssystemet innebär att det uppstår många parallella processer i regionerna, som borde kunna skötas mer samlat.
Andra menar ökad statlig styrning inte nödvändigtvis bidrar till ett ökat genomslag. I Socialstyrelsens (2023a) intervjuer har flera också uttryckt att det svåraste steget i implementeringen är att förankra arbetet inom verksamheterna, där det i sista led ska genomföras, och att mer kraftfull styrning inte är det bästa verktyget.
2.3.3 Strategin har förbättrat samverkan men många vill ha mer gemensamt arbete
Cancerstrategin och inrättandet av RCC har enligt många medfört bättre samverkan, genom att skapa en gemensam utgångspunkt och struktur för dialog i ett annars decentraliserat system. Samtidigt har det varit svårare att nå välfungerande samverkan på områden som berör många aktörer, och RCC:s samverkan med kommunal och regional primärvård fungerar inte lika väl. Många aktörer vill se mer nationell samverkan och nationell styrning.
Aktörerna har en positiv bild av samverkan …
Inrättandet av RCC-strukturen framstår som centralt för samverkan inom cancerområdet. Socialstyrelsen (2023a) bedömer att samverkan mellan de olika RCC på flera sätt fungerar väl. Värdet av samverkan mellan de olika RCC och med RCC i samverkan handlar bland annat om lärande och effektiva arbetssätt (Socialstyrelsen 2021d). Även RCC- företrädare som intervjuats av SKR lyfter fram värdet av att ha ett forum för dialog och erfarenhetsutbyte, och menar att formatet med RCC i samverkan gjort att man kunnat överbrygga meningsskiljaktigheter som annars finns inbyggda i ett system med långtgående regionalt självstyre (SKR 2021a). Även i våra intervjuer har flera lyft fram att det är en fördel med ett samlande organ som RCC-organisationen som också samverkar med myndigheter, och att samarbetet mellan Socialstyrelsen och RCC fungerar väl.
I vår undersökning till RCC finns en bred samsyn om att strukturen med de sex RCC är ändamålsenlig och att samverkan fungerar väl, på olika nivåer. Att RCC återkommande träffas genom RCC i samverkan ses som viktigt för att de sex RCC-kanslierna ska kunna samarbeta effektivt. RCC-strukturen ses som effektiv genom att det som görs sjukvårdsregionalt vid ett RCC kan tas tillvara nationellt och att RCC:erna ger draghjälp till varandra. Det ses också som viktigt att respektive RCC har en sjukvårdsregional förankring, med kännedom om lokala förhållanden. Det möjliggör återkoppling till det nationella arbetet och ger i regel goda förutsättningar för implementering eftersom de nationella arbetsgrupperna har representation från varje sjukvårdsregion.
Inom respektive sjukvårdsregion beskriver RCC-representanter som Socialstyrelsen (2023a) intervjuat att de har en välfungerande samverkan med regionerna. Även i vår undersökning till RCC är de eniga om att samarbetet med regionerna över lag fungerar bra. Det är ett mångfacetterat samarbete, på många nivåer – från det sjukvårdsregionala samarbetet till samarbete på den lokala nivån. En framgångsfaktor bedöms vara att RCC gör allt samlat nationellt och får stöd av varandra, vilket gör det svårare för en enskild region eller gruppering att motsätta sig arbetet. Men det lyfts också att det är viktigt att det finns en förankring av överenskommelserna i regionerna så att uppdrag och mål stämmer överens och att det finns en vilja att arbeta med den aktuella frågan i regionen. Cancerstrategins bidrag är att den gett cancerområdet en samlad riktning på ett sätt som ofta saknas i hälso- och sjukvården, enligt vissa av våra intervjupersoner. Socialstyrelsen (2021d) bedömer att cancerstrategin har haft stor betydelse för att mobilisera förändringsvilja och att skapa nationell gemensam riktning som grund för arbetet (Socialstyrelsen 2021d).
… men det har också funnits utmaningar
En slutsats från tidigare uppföljningar (Socialstyrelsen 2016a 2022c 2023a) är att trots de samverkansformer som finns inom cancerområdet har det i vissa fall inte varit tillräckligt för att få fullt genomslag för cancerstrategins ambitioner. Det gäller särskilt områden som berör bredare frågor om cancervårdens förutsättningar, och områden där det krävs samverkan med aktörer utanför cancervården. Ett exempel är kompetensförsörjning, som inte bara kräver samverkan mellan RCC och linjeorganisationen utan även med aktörer utanför vården, som högskolor och universitet (Socialstyrelsen 2016a).
I vår undersökning till RCC nämns särskilt problemen med kompetensförsörjning som svagheter i samarbetet med regionerna. De gör att det många gånger är svårt att engagera vårdens medarbetare i sjukvårdsregionalt och nationellt arbete vilket leder till att en viktig del av processen för förankring och implementering går förlorad. Det är också svårt att få med företrädare från primärvården i både processarbetsgrupperna och ledningen. Den låga bemanningen, svaga ekonomin och de olika förutsättningarna i regionerna innebär att det kan vara svårt att ”gå från ord till handling”. I undersökningen framkommer vidare att samarbetet mellan RCC och kommuner är svagt. Ett mer strukturerat samarbete sker främst på området palliativ vård, och där benämns det i något fall som ”ett guldkorn med välutvecklat samarbete med medicinskt ansvariga sjuksköterskor och kommunsjukvård”. En informant nämner behovet av att utveckla samarbetet med kommunerna inom fler områden, bland annat inom prevention som rör ohälsosamma levnadsvanor och rehabilitering.
Samarbetet med den kommunala och regionala primärvården har även återkommande pekats ut i Socialstyrelsens uppföljning som ett viktigt område där det finns stora utmaningar (Socialstyrelsen 2014a, 2014c, 2021d, 2023a). Svårigheterna bottnar enligt Socialstyrelsen bland annat i organiseringen av primärvården, att det oftast saknas en gemensam kanal i regionen för att nå alla primärvårdaktörer och bristen på personal i primärvården. Socialstyrelsen (2023a) bedömer att de nuvarande samverkansformerna behöver utvecklas med utgångspunkt i primärvårdens förutsättningar och behov, vilket skulle underlättas av att tydliggöra RCC:s roll i omställningen till en god och nära vård. På den statliga nivån har Socialstyrelsen (2021b) funnit att den samverkan som sker mellan myndigheter nästan uteslutande är kopplad till specifika projekt eller regeringsuppdrag. Däremot sker inte samverkan för att forma en gemensam inriktning framåt för staten som helhet.
Mer gemensamt nationellt arbete efterfrågas
En faktor som återkommer i uppföljningar av olika insatser på cancerområdet är att det hade behövts mer nationell samordning och gemensamt agerande. Socialstyrelsen (2023a) bedömer att det finns ett behov av mer samarbete mellan samtliga RCC, för att öka det gemensamma lärandet om hur olika insatser fungerat, dra nytta av varandras arbete och minska dubbelarbetet. Socialstyrelsen lyfter särskilt fram att det behövs mer samordning i arbetet för jämlikhet mellan grupper i befolkningen.
I Socialstyrelsens (2021b) undersökning av den statligt nationella samordningen uttrycker de flesta myndigheter att de ser ett behov av mer övergripande samordning när det gäller vården generellt, även om de inte kunnat bedöma behovet inom specifikt cancerområdet. Socialstyrelsen bedömer att satsningar och snabba förändringar på cancerområdet sannolikt kommer att innebära att det krävs mer samverkan och bred statlig samordning framöver.
2.4 Uppföljningen av cancerstrategin har inte varit systematisk
Betänkandet som lade grunden för cancerstrategin lämnade konstruktiva förslag på hur cancerstrategin skulle följas upp och hur resultaten från uppföljningen skulle användas. Utredningens förslag till struktur för uppföljning av cancerstrategin bedömer vi därför som en styrka.
Inom flera områden har möjligheterna till uppföljning stärkts under den period som cancerstrategin har funnits. Det handlar särskilt om patientrapporterade upplevelsemått och väntetidsdata.
Däremot är frånvaron av en plan för en systematisk uppföljning en brist inom strategin. Ingen nationell aktör har haft ett tydligt uppdrag att ta fram ett ramverk för uppföljning, målen har inte operationaliserats i lämpliga uppföljningsmått och det har inte skett någon löpande uppföljning av utvecklingen utifrån målen.
Uppföljningen bör stärkas för att möjliggöra lärande och utveckling av strategin
I betänkandet En nationell cancerstrategi för framtiden föreslogs att uppföljningen skulle ske genom att löpande följa upp cancerstrategins mål, med syftet att få kunskap om behovet av ytterligare insatser och revideringar. Det anges också att uppföljningen ska ske på ett sakkunnigt, oberoende och öppet sätt samt att både hälso- och sjukvårdens och statens insatser ska omfattas av uppföljningen. I betänkandet föreslogs även att en baslinjemätning av läget i förhållande till målen skulle genomföras (SOU 2009:11).
När det gäller uppföljning av specifika mål föreslogs att insjuknande skulle följas genom regelbundna internationella jämförelser och i förhållande till ett kontrafaktiskt scenario. Mot bakgrund av att det saknades patientrapporterade mått på omhändertagande och livskvalitet föreslogs även att information om patienternas upplevelser av vården skulle samlas in genom patientrapporterade erfarenhetsmått (PREM) och att mått på livskvalitet skulle samlas in i patientregister.
Vår bedömning är att dessa förslag var välmotiverade. Det skulle tydliggöra hur styrkor och svagheter för de olika målen utvecklas, för att man sedan skulle kunna sätta in lämpliga insatser för att åtgärda behoven. En löpande uppföljning som ger kunskap om utvecklingsbehoven och gör det möjligt att justera implementering är något som implementeringsforskningen lyfter fram som en framgångsfaktor (Vård- och omsorgsanalys 2021b).
Systematisk uppföljning saknas
Cancerstrategin har inte följts upp systematiskt sedan den infördes. I våra intervjuer framkommer att det är ett angeläget utvecklingsbehov. Intervjupersonerna efterfrågar bland annat att någon aktör får ett övergripande ansvar för uppföljningen av strategin, att den görs skarpare genom att indikatorer kopplas till målen, och att staten värderar vad den ska använda uppföljningen till för att skapa tydligare ansvarskänsla hos regionerna. Det framstår, utifrån en rad uppdrag till Socialstyrelsen (2010, 2011a) kort efter att utredningen En nationell cancerstrategi lämnade sitt förslag, som om regeringen tog ett systematiskt grepp om uppföljningen. Socialstyrelsen (2010) fick tidigt i uppdrag att genomföra en baslinjemätning och förslag på en modell för att följa upp skillnader i insjuknande och överlevnadstid mellan regioner och socioekonomiska grupper. Det skulle bidra till att möjliggöra utvärderingar av cancerstrategin, och kunna användas i arbetet med kontinuerligt redovisade öppna jämförelser av cancervårdens kvalitet och effektivitet. Förslaget till modell för uppföljning baseras på tre produkter inom Öppna jämförelser, och utgår från de nationella riktlinjerna. Socialstyrelsen fick även i uppdrag att ta fram en särskild utgåva av Öppna jämförelser för att kunna jämföra olika landsting (Socialstyrelsen 2011a).
Förutom Socialstyrelsen har även Tandvårds- och läkemedelsförmånsverket (TLV) haft flera uppdrag om förutsättningarna för nationell uppföljning, med fokus på nya läkemedel och medicinsk teknologi. Det beskrivs närmare i kapitel 3.
De här initiativen har dock inte följts av någon systematisk uppföljning av strategin i sin helhet. De senaste åren har regeringen tagit initiativ till flera övergripande uppföljningar. Socialstyrelsen fick 2020 ett uppdrag om att utveckla den statligt nationella samordningen och uppföljningen av cancervården. I uppdraget ingår att stärka den nationella samordningen inom cancerområdet, samt utöka sin nationella uppföljning och analys av cancervårdens utveckling och behov (Socialdepartementet 2020). Det gäller uppföljning av cancervårdens kapacitet, vårdutfall, tillgänglighet, patientsäkerhet, jämlikhet, effektivitet samt, i den mån det är möjligt, kostnadseffektivitet, nya arbetssätt och teknologiska framsteg. I ett första steg har Socialstyrelsen kartlagt vilken information som finns i dag och vilken information som behöver utvecklas för att på ett strukturerat sätt kunna följa upp och analysera utvecklingen av cancervården.
Socialstyrelsen beskriver 2021 att man arbetar vidare med att fortsätta kartlägga vilken information som finns och hur den behöver utvecklas för att man ska kunna följa upp och analysera utvecklingen inom cancervården på ett strukturerat sätt. Tanken var att Socialstyrelsen skulle ha en aktiv roll i att bedriva ett mer systematiskt och proaktivt arbete, samt följa upp cancervården med fokus på utvecklingsbehov och möjliga insatser (Socialstyrelsen 2021b). Varken i uppdragen eller i rapporter anknyter man dock uttryckligen till de tidigare uppdragen. Uppdraget förlängdes inte efter 2021. RCC arbetar också med uppföljning genom kvalitets- och väntetidsregistren, men inte med något helhetsgrepp med utgångspunkt i cancerstrategin.
Utöver den övergripande uppföljningen av cancerområdet har regeringen gett uppdrag åt Socialstyrelsen under perioden att återkommande följa upp vissa av insatserna inom cancerstrategin, framför allt RCC:s uppbyggnad och arbete samt de standardiserade vårdförloppen. Anslaget i uppföljningen framstår som lärandeinriktat med analys och rekommendationer riktade till de olika RCC, men vi har inte haft möjlighet att undersöka om de har uppfattat uppföljningen som ett stöd för lärande under implementeringen. Socialstyrelsen (2021d) har samtidigt efterfrågat fler utvärderingar, även externt utförda, av de insatser som RCC gör för att ge mer stöd för lärande och en mer samlad bild av RCC:s resultat.
Bättre förutsättningar att följa upp cancerstrategin trots brister
När cancerstrategin togs fram saknades förutsättningar att följa upp flera delar. En del i strategin var att skapa bättre möjligheter att följa upp cancervården, särskilt patientupplevelser och väntetider.
Förutsättningarna har förbättrats på flera sätt under perioden. Det finns i dag fler kvalitetsregister. Patientrapporterade data samlas in i nästan alla kvalitetsregister och genom patientenkäten till personer som genomgått SVF. Dessutom mäts och följs väntetider upp inom ramen för SVF (se avsnitt 3.6.4).
Det finns dock fortfarande svårigheter med att följa upp olika delar i cancerstrategin nationellt. Även om det finns mycket data så är strukturen för datakällor fragmentarisk och har luckor, vilket leder till att det är svårt att få tillgång till och koppla ihop data från olika källor (TLV 2021a; Socialstyrelsen 2023a). Det gör det svårt att analysera måluppfyllelsen i relation till cancerstrategin på vissa områden, och att stödja implementeringen av cancerstrategin genom lärande.
I våra intervjuer ser man positivt på initiativen för bättre och mer nationellt samordnade datakällor och automatisk inhämtning. Några exempel på initiativ är E-hälsomyndighetens uppdrag på området (Regeringen 2023a, 2023b S2023/02108 och S2023/02109) och utredningarna om infrastruktur för hälsodata som nationellt intresse (dir. 2022:98), sekundäranvändning av hälsodata (SOU 2023:76) och hälsodataregister (dir. 2023:48) samt tillsättandet av en nationell samordnare för en nationell digital infrastruktur i hälso- och sjukvården (dir. 2023:177). Samtidigt pekar vissa på att förutsättningarna för uppföljning på cancerområdet är förhållandevis goda, och anser att det därför är viktigt att fortsätta med det som fungerar i dag i väntan på att de mer övergripande initiativen har nått god funktionalitet.
3 Måluppfyllelse och insatser inom cancerstrategin
Cancerstrategin kan ses som ett paraply för en rad insatser inom cancerområdet. Insatsernas omfattning varierar – från omfattande insatser som uppbyggnaden av RCC-organisationen till mer avgränsade aktiviteter som en förstudie om en telefonrådgivningstjänst för cancer. I det här kapitlet utgår vi från cancerstrategins fem övergripande mål. Vi beskriver dels måluppfyllelsen när det är möjligt, dels de insatser som har genomförts med utgångspunkt i cancerstrategin samt vilken betydelse och genomslag de fått.
Vi baserar resultaten på bland annat överenskommelser, RCC:s uppdrag, myndig- hetsuppdrag, uppföljningsrapporter från olika aktörer, vår intervjustudie samt data om cancervården.
Det här är de viktigaste resultaten:
- Utvecklingen när det gäller uppfyllelse av cancerstrategins mål varierar. Det finns en positiv utveckling särskilt för målen om förbättrad kvalitet i omhändertagandet, ökad överlevnad och minskade regionala skillnader i överlevnadstid. Däremot kan vi inte se en positiv utveckling för målet att minska skillnader mellan befolkningsgrupper i insjuknande. Vi har inte kunnat undersöka utvecklingen inom samtliga mål och för flera av målen saknas det ett tydligt sätt att mäta måluppfyllelsen.
- Totalt har många initiativ tagits till insatser på nationell nivå inom ramen för strategin, varav flera omfattande insatser berör samtliga mål. Särskilt uppbyggnaden av en gemensam struktur för kunskapsstyrning genom RCC har varit mycket i fokus och har över lag bedömts som framgångsrikt.
- På vissa målområden finns många specifika insatser. Det gäller insatser för ett bättre omhändertagande av patienter, där flera av de verktyg för bättre omhändertagande som föreslogs i strategin har genomförts och förutsättningarna för personcentrering och sammanhållen vård tycks ha stärkts. Många insatser har också initierats riktade mot målen om ökad överlevnad och minskade regionala skillnader, och över lag har insatserna bedömts vara välfungerande.
- Inom prevention och tidig upptäckt har mycket fokus legat på screening, medan färre insatser för att påverka levnadsvanor och för tidig upptäckt i primärvården har initierats i den nationella styrningen. Det tycks ha saknats ett samlat grepp inom prevention som rör ohälsosamma levnadsvanor fram tills de senaste åren.
- När det gäller målet att förbättra livskvaliteten har tidigare relativt få insatser initierats från nationellt håll inom till exempel rehabilitering och palliativ vård. Men även de områdena verkar ha kommit mer i fokus de senaste åren.
- I den nationella styrningen framkommer mycket få insatser där minskade skillnader mellan befolkningsgrupper är det huvudsakliga målet. Det tycks inte heller ha tagits några mer systematiska grepp nationellt.
3.1 Minska risken för insjuknande i cancer
I betänkandet En nationell cancerstrategi för framtiden framhölls att det mest betydelsefulla för att minska sjuklighet och död i cancer är prevention. Utredningen menade att det fanns större möjligheter att påverka insjuknandet i cancer än vad som dittills tagits tillvara, och att ett nyckelproblem var att folkhälsopolitiken saknade tydliga mål och strukturer (SOU 2009:11).
Prevention delas ibland upp i primärprevention, som handlar om att förebygga insjuknande genom att bland annat minska riskfaktorer, och sekundärprevention som handlar om att genom tidig upptäckt förbättra förutsättningarna för behandling (SOU 2009:11). Insatser inom screening, som kan handla både om att upptäcka förstadier till cancer och om tidig upptäckt av cancer, beskrivs i det här avsnittet. Tidig upptäckt av cancer som börjat ge symptom, genom framförallt primärvården, beskrivs i avsnitt 3.3 kopplat till målet om ökad överlevnad.
Vi har sett att utvecklingen av insjuknande varierar mellan olika cancerformer. Att förebygga cancer genom att påverka levnadsvanor har varit i mindre fokus under perioden och det tycks ha saknats ett samlat grepp på det området fram tills de senaste åren. Mer fokus har legat på screening och vaccin.
3.1.1 Utvecklingen i insjuknande varierar mellan cancerformer
Totalt sett har insjuknandet i cancer ökat under perioden sedan 2009. Hur risken för insjuknande har utvecklats totalt har vi däremot inte underlag att bedöma. För de fyra cancerformer som vi undersökt har utvecklingen gått i olika riktning. Vi har analyserat utvecklingen av insjuknande i njurcancer, kolorektalcancer (tjock- och ändtarmscancer), lungcancer och bröstcancer. För njurcancer och kolorektalcancer syns små förändringar i andelen som insjuknade mellan 2009 och 2021, både i positiv och negativ riktning. För lungcancer var antalet fall i stort sett oförändrat för kvinnor men minskade kraftigt för män. För bröstcancer syns en tydlig ökning (Socialstyrelsen 2023b).
Skillnaderna i insjuknande mellan regioner har också utvecklats i olika riktning för olika cancerformer och kön. Utifrån en analys av dessa cancerformer tycks de regionala skillnaderna i insjuknande inte vara påtagligt mindre idag än 2009. Analysen tyder på större skillnader mellan regioner i insjuknande i njurcancer bland kvinnor, lungcancer bland män och i bröstcancer. Skillnaderna i insjuknande tycks däremot ha minskat mellan regionerna när det gäller njurcancer bland män och kolorektalcancer bland kvinnor. För lungcancer bland kvinnor och kolorektalcancer bland män var skillnaderna oförändrade (Socialstyrelsen 2023b).
Inom de här cancerformerna har skillnaderna i insjuknande mellan utbildningsgrupper överlag blivit större under perioden. Mer om det i 3.5.
3.1.2 Prevention som rör ohälsosamma levnadsvanor är ett utmanande område
I betänkandet från 2009 pekade utredningen på att en väsentlig andel av fallen av insjuknande i cancer skulle kunna förebyggas, och lyfte fram skillnader i levnadsvanor kopplat till skillnader i insjuknande mellan grupper i befolkningen.
Mindre fokus på levnadsvanor i början
Det tycks ha saknats ett samlat grepp på området prevention som rör ohälsosamma levnadsvanor fram tills de senaste åren. Den nationella styrningen på cancerområdet beskriver jämförelsevis få insatser för att förebygga cancer genom att påverka levnadsvanor under perioden, även om det ingått i RCC:s uppdrag att utforma och implementera en plan för sjukvårdsregionens arbete med förebyggande insatser och tidig upptäckt. Ett område som varit föremål för särskilda insatser i början av perioden är dock minskning av tobaksrökning. Det skedde framför allt genom tobaksslutarstöd och fortbildningar för vårdpersonal i att arbeta med rökavvänjning (Socialdepartementet och SKL/SKR 2010–2023).
Efter att den långsiktig inriktningen (Regeringen 2018) beskrivit att det förebyggande arbetet borde stärkas inom RCC, fick den nationella arbetsgruppen för cancerprevention 2020 i uppdrag att ta fram en nationell cancerpreventionsplan, som följts av en uppdaterad plan för 2024–2030 (RCC i samverkan 2023m). Handlingsplanen utgår från den europeiska kodexen mot cancer, som är framtagen av WHO och innehåller 12 punkter om levnadsvanor för att undvika cancer. Att sprida kunskap om kodexen ingår även i EU:s cancerplan (Europeiska kommissionen 2021a).
Generella initiativ kring folkhälsa och levnadsvanor
Initiativ utanför cancerområdet har betydelse även för cancerprevention. Vi har inte gjort någon systematisk kartläggning av det bredare folkhälsoarbetet. Ett större initiativ på statlig nivå är dock Kommissionen för jämlik hälsa, som under 2015–2017 tog fram förslag till ett uppdaterat folkhälsopolitiskt ramverk och struktur för genomförande. Kommissionen föreslog åtgärder för ett system för långsiktigt arbete för folkhälsa och jämlik hälsa, som omfattade bland annat en ny struktur på statlig nivå och en tydligare samordnande roll för Folkhälsomyndigheten (SOU 2017:4; SOU 2017:47).
År 2018 publicerade Socialstyrelsen nationella riktlinjer för prevention och behandling vid ohälsosamma levnadsvanor, vilket berör både cancerprevention och prevention bredare. De flesta av de rekommenderade åtgärderna bestod av rådgivande samtal från hälso- och sjukvården som stöd till personer att förändra ohälsosamma levnadsvanor. Riktlinjerna betonade särskilt åtgärder som riktar sig till specifika riskgrupper (Socialstyrelsen 2018).
Oklart hur arbetet med levnadsvanor gått
Utredningen En nationell cancerstrategi beskrev att området prevention behövde prioriteras. Socialstyrelsen bedömer att området prioriteras mer idag än tidigare, men fortfarande är lägre prioriterat än annat (Socialstyrelsen 2023a). Enligt Cancerfondens (2019) analys är levnadsvanor den lägst prioriterade delen i folkhälsoarbetet.
Idag bedöms 28 procent av cancerfallen i Sverige kunna förebyggas genom levnadsvanor (Socialstyrelsen 2021a; Cancerfonden 2020b). Vi har inte underlag att beskriva utvecklingen sedan 2009, utan kan bara konstatera att det fortsatt finns mycket kvar att göra för att motverka insjuknande i cancer.
Olika levnadsvanor har förändrats i olika riktning. Cancerfonden pekar på att tobaks- rökningen minskat, men att riskfaktorer för matvanor och motion försämrats över tid (Cancerfonden 2019).
Prevention är en bred och utmanande fråga
Några generella slutsatser om prevention som rör ohälsosamma levnadsvanor är att det är viktigt med samordning eftersom det är en fråga som berör många aktörer (Cancerfonden 2019), nationella initiativ (Socialstyrelsen 2014a) och ett tydligt uppdrag till vården (Socialstyrelsen 2023a).
Flera försvårande omvärldsfaktorer har pekats ut i uppföljningar. Socialstyrelsen och Cancerfonden menar att pressade resurser i vården gör att man inte hinner arbeta förebyggande, och i stället prioriterar det som är mer akut (Socialstyrelsen 2023; Cancerfonden 2020b). Budget- och organisationsstrukturer i vården främjar heller inte preventionsarbete (Socialstyrelsen 2023, Cancerfonden 2019). Det är dessutom generellt svårt att nå ut till befolkningen i frågorna (Socialstyrelsen 2023a) och levnadsvanor uppfattas som en känslig fråga för vårdmöten (Cancerfonden 2020b).
I vår intervjustudie lyfter flera fram att det både är en styrka och svaghet att preventionsåtgärderna på cancerområdet till stor del överlappar med andra folksjukdomar. En fördel är att åtgärderna hänger ihop på alla nivåer där det kan vara många aktörer som arbetar mot samma mål. Men en nackdel är att det är otydligt vem som ansvarar för dessa frågor och vad uppdraget är. I intervjuerna nämns till exempel att det inom RCC har tagit tid för preventionsfrågor att ingå som ett naturligt arbetsområde, att det är svårt att prioritera preventiva insatser i primärvården och att det är oklart vem som ansvarar för att ta ett samlat grepp på preventionsområdet.
RCC har en otydlig roll och få möjligheter att påverka
Socialstyrelsen finner att prevention som rör ohälsosamma levnadsvanor varit ett särskilt svårt område för RCC att arbeta med på ett framgångsrikt sätt (Socialstyrelsen 2023a). De kartläggningar som RCC tidigt gjorde av levnadsvanor och insatser bedömdes som en bra grund för fortsatt arbete. RCC bedömdes också ha hittat bra strukturer för samarbete i sjukvårdsregionerna, och Socialstyrelsen lyfte fram det höga förtroendet för RCC bland samarbetspartner (Socialstyrelsen 2016b). Samtidigt har uppföljningar under perioden också pekat på att RCC haft en alltför otydlig roll inom prevention gällande levnadsvanor (Socialstyrelsen 2014a, 2015, 2023a) och det framkommer också att RCC delvis inte sett prevention som sin uppgift (Socialstyrelsen 2016b, 2023a). Våra intervjuer ger en liknande bild.
Som vi nämnt i 2.3.2 har RCC ett begränsat mandat i frågan och är beroende av att regioner och kommuner väljer att prioritera insatserna (Socialstyrelsen 2023a). Möjligheterna för RCC att själva genomföra insatser varierar (Socialstyrelsen 2023) och RCC har bedömts behöva mer stöd från regionerna i det preventiva arbetet (Socialstyrelsen 2016b). Socialstyrelsen menar också att det saknas ett långsiktigt perspektiv i regionerna på frågan (Socialstyrelsen 2023a).
Socialstyrelsen har också bedömt att det varit svårt för RCC att hitta rätt metoder (Socialstyrelsen 2014a). Uppföljningen har enligt Socialstyrelsen inte varit tillräcklig, vilket gjort det svårt att bedöma effekterna av arbetet med prevention som rör ohälsosamma levnadsvanor och på så sätt lära (Socialstyrelsen 2016b).
Primärvårdens bristande förutsättningar försvårar
Primärvården har en särskilt viktig roll i prevention som rör ohälsosamma levnadsvanor. Analyser visar på en stark vilja i primärvården att arbeta preventivt, samt att det finns verktyg och formellt stöd (Socialstyrelsen 2023a; Cancerfonden 2020b), men att förutsättningarna att arbeta preventivt brister (Cancerfonden 2020b). En försvårande faktor som lyfts fram är att kunskaperna om riskfaktorer för cancer varierar bland personalen, som beskriver en otrygghet i att prata om levnadsvanor. Cancerfonden pekar också på att primärvården har ont om resurser, bristande kontinuitet och it- stöd (Cancerfonden 2020b). En liknande bild har vi fått i vår pågående utvärdering av omställningen till en god och nära vård. Både samverkan och förebyggande arbete ses som centrala för att nå omställningens mål, men det saknas resurser för att tillräckligt kunna prioritera dessa uppdrag (Vård- och omsorgsanalys 2023b). En sammanfattande bedömning i Socialstyrelsens nationella riktlinjer var att mer resurser behöver tillföras hälso- och sjukvården för att fler personer med ohälsosamma levnadsvanor ska kunna erbjudas de rekommenderade åtgärderna (Socialstyrelsen 2018).
Bristande styrning i folkhälsoarbetet generellt
När det gäller folkhälsoarbetet över lag beskriver Kommissionen för jämlik hälsa ett nuläge 2017 som i mycket liknar det som utredningen om cancerstrategin beskrev 2009. Man beskriver brister i styrning, att det varit otydligt vem som har ett övergripande ansvar och att det därför är svårt att få genomslag för de politiska målen om folkhälsan (SOU 2017:47). Även Socialstyrelsen (2023a) har lyft fram att oklarheter i exempelvis Folkhälsomyndighetens roll gör det svårare att identifiera RCC:s roll inom cancerprevention. Cancerfonden menar att det också varit fel balans mellan samhällsåtgärder och individuellt stöd. Cancerfonden har bland annat efterfrågat åtgärder för att genom skatter och på andra sätt påverka matvanor (Cancerfonden u.å). Även i vår intervjustudie framkommer att det i verksamheter kan finnas en mättnad när det gäller försöken att stärka levnadsvanor genom individuellt stöd, och att ökade insatser på policynivå efterfrågas.
3.1.3 Satsning för att utrota livmoderhalscancer
Utredningen En nationell cancerstrategi menade att cancervacciner i framtiden skulle kunna förebygga cancer, och att dessa borde införas på ett nationellt samordnat sätt för att komma alla medborgare till del. Sedan dess har vaccination mot HPV-virus implementerats i en ”Särskild satsning för att utrota livmoderhalscancer”. Uppdragen till RCC-strukturen har bland annat handlat om att på nationell nivå främja samverkan för erfarenhetsutbyte och på sjukvårdsregional nivå stötta regionerna i arbetet (Socialdepartementet och SKR 2022, 2023).
Socialstyrelsen bedömer att regionerna ligger i fas med WHO:s mål om att utrota livmoderhalscancer (Socialstyrelsen 2022c). I övrigt saknar vi kunskap om hur implementeringen av insatsen fungerat.
3.1.4 Screening för förebyggande och tidig upptäckt
Screeningprogram syftar både till att förebygga cancer och att upptäcka cancer tidigt, och rör alltså både mål 1 och 3 i cancerstrategin. De screeningprogram som varit mest i fokus under perioden handlar åtminstone delvis om att förebygga insjuknande genom att hitta förstadier till cancer, och därför beskrivs screening under målet om minskat insjuknande. Arbetet med förebyggande och tidig upptäckt genom screening har varit inriktat på att testa och införa nya screeningprogram, samordna befintliga screeningprogram med exempelvis gemensamma kallelser, samt att öka täckningsgraden i befintliga screeningprogram och göra deltagandet mer jämlikt. Vissa av dessa insatser beskrivs närmare i avsnitt 3.4 om minskade skillnader mellan regioner.
RCC-strukturen har haft en rad uppdrag att stötta regionerna i arbetet med screening. Socialstyrelsen har tidigt under perioden tagit fram en nationell modell för bedömning och införande av nya screeningprogram som började användas 2014. Socialstyrelsen har även under slutet av perioden haft i uppdrag att utveckla ett mer samordnat nationellt arbete samt utveckla uppföljningen och utvärderingen av screeningprogrammen (Socialstyrelsen 2022c).
Ytterligare ett screeningprogram har börjat införas under perioden
Vid startpunkten för den nationella cancerstrategin fanns två etablerade screeningprogram på nationell nivå i Sverige: screening för livmoderhalscancer och mammografi.
Idag bedömer Socialstyrelsen att mammografin och screeningen för livmoderhalscancer är väl organiserade med högt men ojämlikt deltagande (Socialstyrelsen 2019c; Cancerfonden 2021). Den genomsnittliga deltagargraden i bröstcancerscreening i Sverige är idag drygt 80 procent. Täckningsgraden för screening för livmoderhalscancer låg 2020 på 78 procent för hela riket (Socialstyrelsen 2020a).
Ytterligare ett screeningprogram, för kolorektalcancer, håller på att införas. Screeningprogrammet har införts gradvis sedan det började testas 2009, och 2022 började det införas i samtliga regioner (RCC i samverkan 2022e).
Möjligheterna att följa upp screeningen i nationella register brister fortfarande (Socialstyrelsen 2022c).
Olika uppfattningar om nyttan av screening
Vår intervjustudie visar att det finns olika uppfattningar om hur forskningen ska tolkas och hur nyttan med screeningsprogrammen ska förstås. Det finns olika synsätt på screening inom forskningen. Vissa bedömer att det bara undantagsvis finns evidens för att screeningprogrammen påverkar dödlighet i cancer (Bretthauer m.fl. 2023) men att det däremot finns flera negativa aspekter, som överbehandling. Vissa forskare har därför argumenterat för att det bör ske ett omtag av riktlinjerna på screeningområdet (Adami m.fl. 2023). Socialstyrelsen bedömer dock att det finns vetenskapligt stöd för de screeningprogram som införts, men att det kan finnas skäl att undersöka om vissa av screeningprogrammen, exempelvis för bröstcancer, kan utformas till att bli mer träffsäkra i förhållande till riskgrupper.
3.2 Förbättra kvaliteten i omhändertagandet av patienter med cancer
Utredningen En nationell cancerstrategi beskrev 2009 att även om de medicinska resultaten i svensk cancervård var goda ur ett internationellt perspektiv, så var patienter och personal kritiska mot att vården var fragmentarisk, med bristande kontinuitet och långa och varierande väntetider.
Vi kan inte fullt ut beskriva utvecklingen över tid eftersom det inte finns jämförbara data, men generellt sett har cancerpatienter idag ett gott helhetsintryck av vården. Det har skett en rad insatser för ett bättre omhändertagande som representanter för patienter och närstående bedömer har förbättrat omhändertagandet. Bland annat har kontaktsjuksköterskor och individuella vårdplaner införts, och man har arbetat för bättre vårdprocesser och kortare väntetider genom standardiserade vårdförlopp (SVF). Insatser har också gjorts för att kunna följa upp patienters upplevelser av vården. Samtidigt kvarstår vissa grundläggande frågor, som att vården präglas av fragmentisering och att väntetiderna varierar.
3.2 1 Patienters upplevelser är positiva och stabila över tid
Det saknas jämförbara uppgifter om patienters upplevelser över längre tid. Här redovisar vi utvecklingen sedan 2016, första gången PREM-enkäten till patienter inom SVF skickades ut.
Över lag bedöms andelen nöjda cancerpatienter vara hög (RCC i samverkan 2019) och nivåerna är generellt sett stabila över tid (Åkesson och Tufvesson Stiller 2019).
Det gäller även de cancerformer vi undersökt närmare. Patienter som utreds för misstänkt cancer inom SVF för njurcancer, lungcancer och kolorektalcancer har ett gott helhetsintryck av vårdupplevelsen. Både 2016 och 2022 uppgav patienter inom kolorektalcancer det lägsta helhetsintrycket och patienter med bröstcancer det bästa. Inom alla cancerformerna var patienterna både 2016 och 2022 mest nöjda med respekt och bemötande och minst nöjda med emotionellt stöd samt delaktighet och involvering (Patientenkäten, Patienter utredda inom SVF).
Över tid syns inga stora förändringar i patienternas upplevelser. För lungcancer, kolorektalcancer och bröstcancer syns en viss förbättring i upplevelsen av delaktighet och involvering samt tillgänglighet mellan 2016 och 2022. En viss förbättring i upplevelsen av emotionellt stöd syns också över tid för patienter med njurcancer och lungcancer.
En synpunkt som framförts av patientorganisationer är att stödet till närstående också är en viktig, men bristande, del.
3.2 2 Arbetet med kontaktsjuksköterskor och individuell vårdplan uppfattas som framgångsrikt
I betänkandet En nationell cancerstrategi för framtiden föreslogs flera insatser för ökad personcentrering. Två områden som varit i fokus för arbetet med förbättrat omhändertagande är individuella vårdplaner och kontaktsjuksköterskor.
En kontaktsjuksköterskas främsta uppgift är att ha ett övergripande ansvar för patient och närstående genom vårdkedjan (RCC i samverkan 2023i). Insatser för fler kontaktsjuksköterskor ingick i 2010–2013 års överenskommelser. RCC och SKR har bland annat arbetat med kartläggningar, en gemensam beskrivning av uppdraget och främjat införandet av fler kontaktsjuksköterskor (Socialdepartementet och SKL 2010–2013).
RCC-strukturen har också under hela perioden haft i uppdrag att arbeta med individuella vårdplaner. Min vårdplan är en annan benämning på individuell vårdplan och definieras enligt RCC som dokument som patienten har tillgängliga under hela vårdprocessen, som fungerar som informationsstöd för patienter och deras närstående (RCC i samverkan 2023c).
Positiv utveckling av kontaktsjuksköterskor och individuella vårdplaner
Det tycks ha skett en positiv utveckling när det gäller tillgången till kontaktsjuksköterskor och individuella vårdplaner. Bland de fem cancerformer vi undersökt närmare ingår kontaktsjuksköterska och individuell vårdplan bara i kvalitetsregistren för njurcancer och bröstcancer. För dessa cancerformer syns en positiv utveckling i måluppfyllelse, framför allt inom njurcancer där utgångsläget var sämre.
Socialstyrelsen (2021d) bedömer att insatserna har stärkt patienternas ställning. I vår intervjustudie lyfter också flera fram att införandet av kontaktsjuksköterska bidragit till trygghet och stärkt kontinuitet för patienterna.
Arbetet med kontaksjuksköterskor uppfattas som framgångsrikt
Kontaktsjuksköterskor är ett område där RCC enligt Socialstyrelsens uppföljningar lyckats särskilt väl (Socialstyrelsen 2016a) och det beskrivs som framgångsrikt när det gäller att stärka patientens ställning (Socialstyrelsen 2021d; SKL 2013e). Kontaktsjuksköterskor bedöms som viktiga av representanter för patienter och närstående, som beskriver att kontaksjuksköterskan fungerar som spindeln i nätet för att hålla ihop vården (Socialstyrelsen 2021d). Tidigt under perioden konstaterades att det var stor variation i tillgången till kontaktsjuksköterskor och att innehållet i uppdraget skilde sig åt (SKR 2013e). Regionala skillnader finns fortfarande (Socialstyrelsen 2021d).
Indikatorerna för tillgång till kontaktsjuksköterska skiljer sig åt mellan kvalitetsregistren. Det kan till exempel formuleras som att man blivit erbjuden kontaktsjuksköterska, eller att man har en namngiven kontaktsjuksköterska. Indikatorerna är därmed inte jämförbara mellan cancerformerna. När vi tittar närmare på njur- och bröstcancer syns en påtaglig förbättring över tid för njurcancer, där måluppfyllelse och regionala skillnader hade sämre utgångsläge. Förändringen över tid är mindre för bröstcancer, där utgångsläget i måluppfyllelse och spridning var bättre. Generellt visar statistiken på stora ökningar av andelen patienter med njurcancer med en namngiven kontaktsjuksköterska mellan 2014 och 2022. Skillnaderna mellan regioner har minskat kraftigt och ökningen har skett från i vissa fall mycket låga nivåer. För bröstcancerpatienter syns en liten ökning av andelen som erbjudits kontaktsjuksköterska mellan 2015 och 2022, men för specifika regioner ses både ökningar och minskningar. Skillnaderna mellan regioner var relativt liten både 2015 och 2022 (Kvalitetsregistren för respektive cancerform).
Även målnivåerna som specificeras i kvalitetsregistren skiljer sig åt mellan cancer- formerna. För njurcancer når merparten av regionerna den lägre målnivån och omkring hälften även den högre målnivån. För bröstcancer är måluppfyllelsen högre. Alla regioner utom en når den lägre målnivån, och drygt hälften når den högre målnivån.
Ökning av individuella vårdplaner skiljer sig åt mellan cancerformer
Av uppföljningsrapporter framgår att det pågått arbete med individuella vårdplaner under hela perioden, men att processen varit mödosam och tagit tid (Socialstyrelsen 2014a, 2016a). Senare uppföljning visar att införandet av individuella vårdplaner upplevs som framgångsrikt och viktigt av patient- och brukarrepresentanter (Socialstyrelsen 2021d). Även när det gäller individuell vårdplan skiljer sig målnivåerna mellan njur- och bröstcancer. Merparten av regionerna når den lägre målnivån för bröstcancer, och hälften når den lägre målnivån för njurcancer. Förändringen över tid är positiv för båda cancerformerna. Andelen njurcancerpatienter med individuell vårdplan ökade mellan 2016 och 2022 i de flesta regioner, och nästan tredubblades på riksnivå. Antalet regioner som nådde upp till den lägre målnivån gick från inga till hälften. För bröstcancerpatienter ökade förekomsten av individuell vårdplan betydligt mindre, men utgångsläget var också betydligt bättre. Andelen regioner som når upp till målnivåerna har ökat även inom bröstcancer.
Utvecklingen i skillnader mellan regioner skiljer sig åt mellan de båda cancerformerna. Inom njurcancer rådde stora regionala skillnader både 2016 och 2022. För bröstcancer har skillnaderna däremot minskat kraftigt.
Involvering av patienter och närstående uppfattas som en framgångsfaktor
Samverkan med representanter för patienter och närstående bedöms ha varit en framgångsfaktor i arbetet med förbättrat omhändertagande (Vård- och omsorgsanalys 2024). Socialstyrelsen lyfter fram formaliserad medverkan av patienter och närstående inom ramen för RCC-strukturen som viktigt för lärande. I Socialstyrelsens intervjuer lyfter flera också fram samverkan i den nationella arbetsgruppen för patientmedverkan som viktigt för gemensamt lärande och erfarenhetsutbyte (Socialstyrelsen 2021d).
Behov av att ytterligare utveckla patientmedverkan har dock lyfts fram (RCC i samverkan 2021b). Socialstyrelsen har också bedömt att organisationsperspektivet premierats över patientperspektivet på det sättet att kontaktsjuksköterskor varit knutna till respektive vårdenhet, så att patienter inte kunnat ha samma kontaktsjuksköterska genom processen. Samtidigt har kontaktsjuksköterskor också lyft fram att de behöver vara specialiserade inom klinikens område för att kunna ge stöd (Socialstyrelsen 2016a).
Verksamheter har inte alltid sett behovet
En svårighet i arbetet med kontaksjuksköterskor och individuella vårdplaner som framkommer i våra intervjuer är att verksamheter inte alltid sett behovet, och ansett att kontaktsjuksköterskor inte behövts utöver den fasta vårdkontakten som är lagreglerad eller att det har räckt med de befintliga vårdplanerna (se även Socialstyrelsen 2016a).
Som för många andra insatser har införandet försvårats av kompetensbrist. Sjuk- sköterskebristen lyfts särskilt fram kopplat till kontaktsjuksköterskorna (Socialstyrelsen 2021d).
3.2.3 Försöksverksamheter för patientfokuserad och sammanhållen vård
Under 2009–2013 pågick genomförandet av ”försöksverksamhet för en patientfokuserad och sammanhållen cancervård” inom ramen för överenskommelserna mellan regeringen och SKR. Försöksverksamheterna skulle bidra till ökad personcentrering genom att utveckla, testa och utvärdera nya arbetssätt.
Försöksverksamheterna hade bara hunnit börja när projektet avrapporterades 2013 (SKL 2013b). Utvärdering pågick då av flera av försöksverksamheterna, men vi har inte haft möjlighet att närmare studera resultatet från utvärderingarna.
3.2.4 Patientupplevelser följs upp mer
En insats för att förbättra omhändertagandet av patienter är att följa upp patienters upplevelser av vården och vårdens resultat. Patientupplevelser följs upp i betydligt högre grad idag än när cancerstrategin togs fram.
Vi beskriver det här närmare i avsnitt 3.6.4 om förutsättningarna för uppföljning av cancervården.
3.2.5 Standardiserade vårdförlopp
En omfattande insats för ett bättre omhändertagande av cancerpatienter med kortare väntetider, sammanhållna vårdkedjor och mer jämlik vård, har varit införandet av standardiserade vårdförlopp.
De standardiserade vårdförloppen beskrivs i utförligare i kapitel 4.
3.3 Förlänga överlevnadstiden och förbättra livskvaliteten efter en cancerdiagnos
Det har skett en mängd olika insatser för att förbättra överlevnaden och livskvaliteten efter en cancerdiagnos. Överlevnaden har ökat under perioden sedan cancerstrategin tog fram. När det gäller livskvalitet är utvecklingen mer oklar.
En viktig del i förutsättningarna att behandla cancer är tidig upptäckt. För merparten av de personer som får cancer upptäcks cancern i primärvården. Även screening (se 3.1.4) syftar till att upptäcka cancer tidigt.
Kopplat till målet om förbättrad överlevnad har man även bland annat arbetat med nivåstrukturering av cancervården för att främja tillgång till bästa kunskap. Arbete har också skett med patienters tillgång till medicinsk teknik och nya läkemedel, samt tillgång till multidisciplinära konferenser.
När det gäller livskvaliteten efter en cancerdiagnos är rehabilitering och palliativ vård viktiga områden.
3.3.1 Överlevnaden har ökat, medan utvecklingen i livskvalitet är oklar
Överlevnadstiden efter en cancerdiagnos har förbättrats sedan cancerstrategin togs fram. För de diagnoser som vi undersökt närmare (njurcancer, lungcancer, tjocktarmscancer, ändtarmscancer och bröstcancer) syns en ökad relativ 5-årsöverlevnad för samtliga på mellan 4 och 10 procentenheter från 2010 till 2020 (se figur 2).
Figur 2. Relativ 5-årsöverlevnad hos patienter 30–89 år för olika cancerformer.
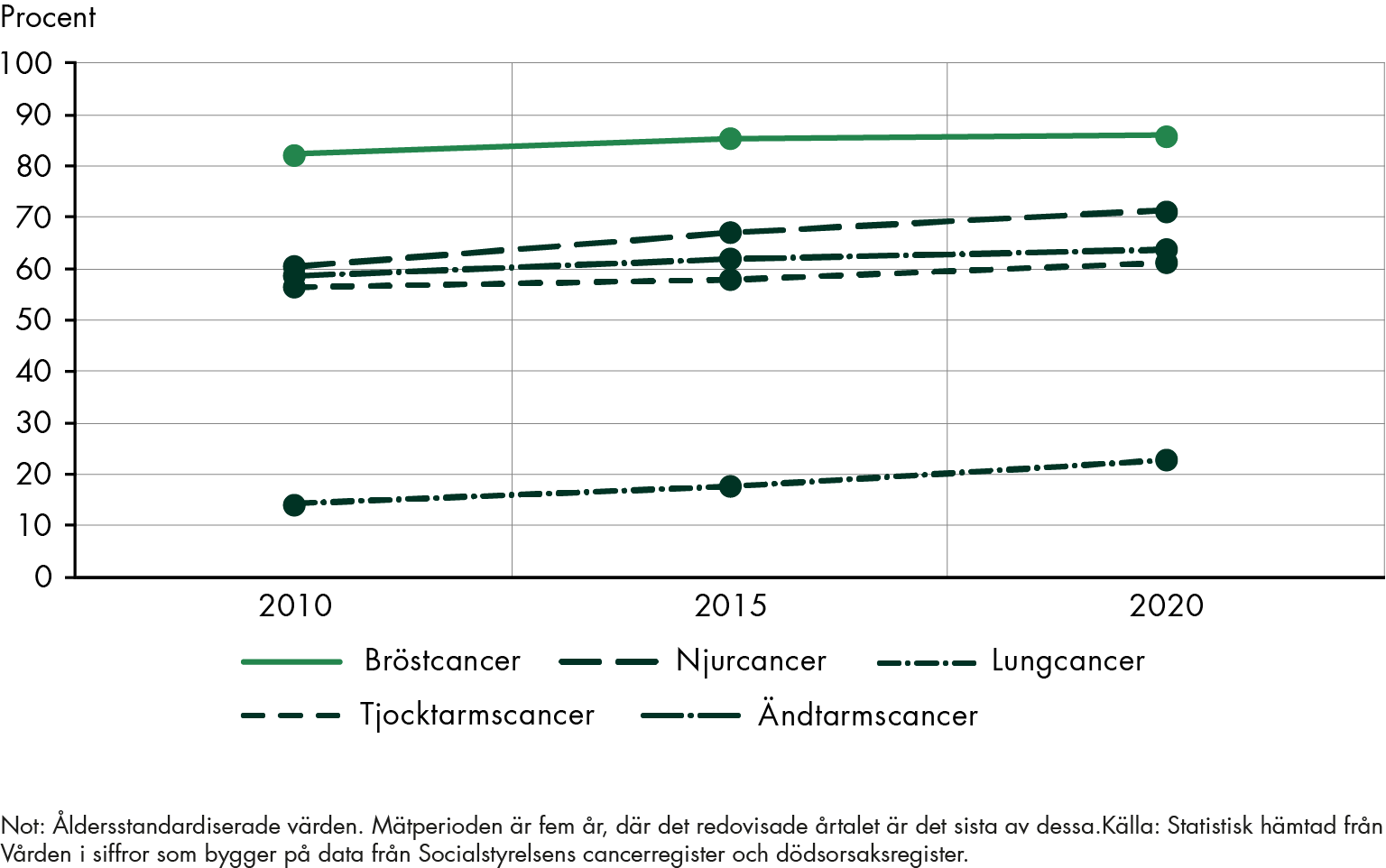
Vi saknar underlag för att bedöma hur livskvaliteten för personer med cancerdiagnos utvecklats sammantaget. Däremot pekar kvalitetsindikatorer inom palliativ vård mot en positiv utveckling (Palliativregistret). Patientorganisationer har i vår undersökning lyft fram att det skulle behövas en bredare förståelse av begreppet livskvalitet än vad som ofta är fallet idag. De lyfter fram faktorer som ekonomisk trygghet och att kunna arbeta, vilket aktualiserar frågor som är bredare än bara vården.
3.3.2 Tidig upptäckt i primärvården har inte varit i fokus
Tidig upptäckt av cancer är centralt för att förbättra möjligheterna att öka överlevnaden bland dem som får cancer. Merparten av alla cancerfall upptäcks i primärvården.
Förutsättningarna för tidig upptäckt i primärvården har varit föremål för jämförelsevis få insatser i den nationella styrningen. Ett initiativ som skett med fokus på primärvårdens roll är etableringen av en nationellt gemensam definition av kriterier för ”välgrundad misstanke om cancer”, som är kriterier för att inkludera patienter i de standardiserade vårdförloppen. RCC har en arbetsgrupp för tidig upptäckt av cancer med fokus på primärvårdens arbete (RCC i samverkan 2023d). Överenskommelserna i slutet av perioden beskriver också att RCC ska stödja hälso- och sjukvården i att öka kunskapen om symtom och fynd som kan innebära förhöjd cancerrisk.
Välgrundad misstanke har underlättat remitteringsprocessen, men förutsättningarna brister
Idag upptäcks 7 av 10 cancerfall i primärvården. Vi saknar underlag på om det har förändrats över tid. Däremot pekar uppföljningar på bristande förutsättningar för primärvården att upptäcka cancer tidigt, vilket tyder på att det finns en förbättringspotential (Gralén 2022; Socialstyrelsen 2023a). I vår intervjustudie betonar några primärvårdens roll i tidig upptäckt, och att största delen av cancerfallen upptäcks där och inte genom screening. Men enligt Cancerfondens analys har utvecklingen av tidig upptäckt av cancer i princip stått stilla.
Socialstyrelsens uppföljning av SVF visade på smidigare remittering efter att vård- förloppen införts, och att definitionen av välgrundad misstanke uppfattades ha underlättat för primärvården (Socialstyrelsen 2019b). Cancerfonden (2020a) betonar dock att vårdförloppen inte är utformade för att öka primärvårdens förmåga att upptäcka cancer tidigt, utan inriktade på att förbättra processen efter att symptom upptäckts, och att det inte har gjorts någon uppföljning av ifall de påverkat primärvårdens förmåga till tidig upptäckt.
Insatserna har fokuserat på kunskap – inte organisatoriska förutsättningar
Insatserna kring tidig upptäckt i primärvården som ingått i nationella styrningen inom ramen för cancerstrategin har handlat om kunskap. Samtidigt framkom i en intervjustudie med primärvårdsläkare (Gralén 2022) att de inte uppfattade bristande kunskap som ett centralt problem, utan att det var andra faktorer som försvårade tidig upptäckt. De viktigaste försvårande faktorerna var enligt läkarna tidsbrist och bristande kontinuitet. Även bristfälliga journalsystem som gör det svårare att på en helhetsbild och brist på beslutsstöd lyftes fram. Även Socialstyrelsen och Cancerfonden har pekat på bristande organisatoriska och resursmässiga förutsättningar för primärvården att upptäcka cancer tidigt (Socialstyrelsen 2023a; Cancerfonden 2020b). Cancerfonden (2020a) menar bland annat att stuprörsorganisation och bristande kontinuitet försvårar tidig upptäckt. I våra intervjuer lyfter flera fram behovet av ökad forskning och fortbildning, bättre verktyg samt mer tid och resurser för primärvården för att göra bättre bedömningar av avvikelser och symtom. Socialstyrelsen (2023a) har pekat på att de arbetssätt som används i primärvården är framtagna för specialistvården, eftersom det saknas verktyg framtagna utifrån primärvårdens behov. En bidragande orsak är att det är ont om forskning utifrån primärvårdens behov (Cancerfonden 2020a).
Att inkludera, samarbeta med och nå ut till primärvården har också varit en generell svårighet för RCC (se 2.3.3) (Socialstyrelsen 2019b, 2023a).
3.3.3 Nivåstrukturering av cancervården
Utredningen om en cancerstrategi beskrev att allt större mängder ny kunskap behövde spridas och omsättas i praktik genom en sammanhållen struktur och en medveten nivåstrukturering av cancervården. Det handlade om att centralisera delar av vården för att möjliggöra specialisering och knyta vård och forskning närmare varandra, samt att tydliggöra vilken vård som skulle ske närmare patienten i exempelvis primärvården.
Nivåstrukturering har sedan dess genomförts dels inom sjukvårdsregionerna, dels genom en koncentration av viss vård till en eller ett par nationella vårdenheter.
På sjukvårdsregional nivå har varje regionalt cancercentrum ansvarat för att ta fram en plan för nivåstruktureringen med beslutsunderlag för regionledningarna, inklusive aspekter som primärvårdens roll, patientvolymer, resursmässiga förutsättningar och system för multiprofessionella konferenser. Därefter har de olika RCC arbetat med att stödja genomförandet och följa upp arbetet (Socialdepartementet 2011, Socialstyrelsen 2017).
RCC i samverkan drev arbetet med nivåstrukturering till nationella vårdenheter under 2013-2020. Socialstyrelsen tog därefter över 2020 som del i sitt arbete med nationell högspecialiserad vård (RCC i samverkan 2018, 2023h).
Nivåstrukturering har genomförts men vi känner ännu inte till effekterna
Nivåstruktureringen inom sjukvårdsregionerna har varit ett utmanande område för RCC att arbeta med under perioden (Socialstyrelsen 2015, 2016a, 2016b, 2021d). I uppföljningen från 2021 framkommer att det skiljer sig åt mellan sjukvårdsregioner hur långt man kommit med arbetet (Socialstyrelsen 2021d). I vår undersökning till RCC framkommer att RCC på den regionala nivån idag arbetar med till exempel kartläggningar och utredningar om effekter av nivåstrukturering, ger stöd för dialog och genomför uppföljningar av beslut om nivåstrukturering.
När det gäller den nationella nivåstruktureringen så är avancerad diagnostik och behandling inom 10 diagnosområden nationellt koncentrerade idag (RCC i samverkan 2023h). RCC i samverkan (2020e) bedömer i en uppföljning att samverkan mellan de nationella vårdenheterna fungerar väl, men att samverkan med de remitterande enheterna kan förbättras. De multidisciplinära konferenser som etablerats som en del i nivåstruktureringen uppfattas som en stor tillgång av vårdenheterna.
Vi saknar underlag om hur patienterna påverkats av nivåstruktureringen. År 2018 när RCC i samverkan utvärderade den nationella nivåstruktureringen av peniscancer, som hörde till de första diagnoser att koncentreras nationellt 2015, bedömdes det ännu vara för tidigt att analysera t.ex. påverkan på överlevnad (Socialstyrelsen 2016b; RCC i samverkan 2018).
Gemensamt nationellt arbete har underlättat nivåstruktureringen
Den främsta utmaningen i arbetet med nivåstrukturering inom sjukvårdsregionerna har enligt uppföljning varit att komma överens om hur nivåstruktureringen ska se ut (Socialstyrelsen 2016a, 2017, 2021d). Man har behövt hantera konflikter inom professionen och konkurrens mellan regioner. En annan utmaning har varit oro för risk för negativ påverkan på annan vård.
Socialstyrelsen (2017) har i uppföljning lyft fram det nationella arbetet inom RCC i samverkan. Man bedömer att arbetet inte bara ha bidragit till den nationella nivåstruktureringen, utan också varit en viktig del i nivåstruktureringen inom sjukvårdsregionerna. Detta genom att regionerna fått gemensamma underlag, med förslag till nivåstrukturering och kriterier för bedömning från den nationella nivån. Socialstyrelsen bedömer att det underlättat processerna i sjukvårdsregionerna och förbättrat förutsättningarna för jämlik vård.
3.3.4 Insatser för ökad tillgång till medicinsk teknik och läkemedel
Många insatser som berör olika former av medicinsk teknik och läkemedel har varit inriktade på både förbättrade medicinska resultat och att minska skillnaderna mellan regioner, exempelvis ordnat införande och stöd för precisionsmedicin. Det beskrivs närmare i avsnitt 3.4.2.
Ordnat införande underlättar men osäkerheten ökar
Socialstyrelsen har under perioden bedömt att arbetet med ordnat införande snabbat på introduktionen av nya läkemedel (Socialstyrelsen 2016a). När det gäller utvecklingen av användning beskriver Tandvårds- och läkemedelsförmånsverket (TLV) (2021a) att användning och kostnader är högre än förväntat, samtidigt som osäkerheten vid introduktion av nya läkemedel har ökat.
3.3.5 Multidisciplinär konferens är en del i många insatser
Multidisciplinär konferens (MDK) är ett viktigt inslag i bedömningen och behandlingen av patienter med cancer. Under en MDK diskuterar flera specialiteter och professioner en patients behandlingsalternativ för att få bästa behandlingsresultat. Det varierar mellan cancerformer vilken sammansättning en MDK bör ha och i vilket skede av behandlingen en konferens blir aktuell.
Att främja MDK har varit en del i flera andra insatser som RCC-organisationen arbetat med under perioden, som den nationella och sjukvårdsregionala nivåstruktureringen och införandet av standardiserade vårdförlopp (Socialdepartementet och SKL 2017; Socialstyrelsen 2017). MDK stöds också av de nationella vårdprogrammen, där det anges för vilka patienter som MDK bör hållas. RCC:s arbete har bland annat handlat om att ta fram ett nationellt ramverk för nationell MDK och att praktiskt underlätta, till exempel med tillgång till lokaler med utrustning och stöd till tidsplanering (Socialstyrelsen 2017).
Förbättring över tid trots skillnader mellan cancerformer
Kvalitetsregistren anger målnivåer för andelen patienter som diskuteras vid MDK. Målnivåerna varierar mellan de olika kvalitetsregistren. När vi tittar närmare på njur- cancer, lungcancer, kolorektalcancer och bröstcancer så når man på riksnivå generellt upp till åtminstone den lägre målnivån, i de fall det finns en lägre och en högre målnivå. För lungcancer, kolorektalcancer och bröstcancer når alla eller nästan alla regioner målnivån, medan merparten av de regioner som det finns data för når upp till den lägre målnivån för njurcancer. Förekomsten av MDK tycks ha ökat över tid för samtliga fyra cancerformer, om än i olika utsträckning och från olika utgångslägen (Kvalitetsregistren för respektive cancerform).
3.3.6 Tillgången till rehabilitering tycks variera
Rehabilitering har i relativt liten utsträckning nämnts i exempelvis överenskommelser och myndighetsuppdrag tidigare under perioden, men tycks ha kommit mer i fokus de senaste åren. Varje RCC har också redan från början haft i uppdrag att ta fram en plan för patienters tillgång till rehabilitering och palliativ vård (Socialdepartementet 2011). Det första nationella vårdprogrammet för cancerrehabilitering kom 2014 och var en kunskapsgenomgång och sammanställning av områdets innehåll. En generisk modell för rehabilitering är också framtagen av det nationella programområdet för rehabilitering, habilitering och försäkringsmedicin (SKR 2021b). Under främst slutet av perioden har överenskommelserna på cancerområdet angett en rad insatser för RCC-strukturen inom rehabilitering och uppföljning av patienter efter behandling. Arbetet har varit inriktat på att implementera det nationella vårdprogrammet, ta fram utbildningar om bedömning av rehabiliteringsbehov och göra det möjligt att följa upp rehabilitering i de nationella kvalitetsregistren (Socialdepartementet och SKR 2020–2023).
Socialstyrelsen (2022b) har utifrån ett regeringsuppdrag utarbetat förslag till hur cancerrehabiliteringen kan förbättras för patienter och deras närstående samt ge en mer jämlik vård.
Tillgången till rehabilitering är inte känd, men tycks variera
Det är inte känt hur tillgången till rehabilitering ser ut i landet, men Socialstyrelsen arbetar nu med en kartläggning. Socialstyrelsen har hittills bedömt att det nationella vårdprogrammet för cancerrehabilitering är implementerat i olika utsträckning i olika regioner, och det är svårt att få en helhetsbild av hur långt man kommit (Socialstyrelsen 2022b). Det är främst professioner som arbetar inom cancervården som använder sig av vårdprogrammet.
Socialstyrelsen (2022b) bedömer att det varit svårt att gå från kunskap till genomförande inom rehabilitering. Cancerfonden har tillsammans med Bröstcancerförbundet (2021) kartlagt tillgången till rehabilitering för bröstcancerpatienter. Där framkom att trots att det finns tydliga riktlinjer för när en bedömning av rehabiliteringsbehov ska göras, är det är stora skillnader i när en bedömning av rehabiliteringsbehovet görs. Det framkom också att det på flera ställen saknas överblick över tillgängliga resurser med rehabiliteringskompetens. I kartläggningen framkom att det förvisso finns många goda initiativ och att många patienter får sina behov tillgodosedda, men att bedömningen av rehabiliteringsbehovet inte är generellt ordnad utan tycks bli av när patienten själv påtalar det eller när en medarbetare eller enhet på eget initiativ gör behovsbedömningar. I vår intervjustudie lyfter flera fram brister när det gäller rehabilitering, till exempel att många patienter upplever att de lämnas efter sin cancerbehandling, med osäkerhet om vart de ska vända sig med kvarstående problem och där primärvårdens kompetens ifrågasätts. Även patientorganisationer har i vår enkät beskrivit rehabilitering som ett svagt område i cancervården.
Socialstyrelsen (2022b) och patientorganisationer i vår undersökning har särskilt lyft fram att vården ofta förbiser unga vuxnas behov av rehabilitering, som skiljer sig på vissa sätt från äldre patienters. En stor andel av medlemmarna i Ung cancer uppger i en undersökning att deras tillgång till rehabilitering varit otillräcklig (Ung cancer 2023).
RCC och cancerstrategin har bidragit positivt
Både RCC och den nationella cancerstrategin beskrivs tidigt under perioden ha varit viktiga för att uppmärksamma området cancerrehabilitering (Socialstyrelsen 2014a). Eftersom områden som rehabilitering inte alltid stått i fokus var många positiva till att RCC fått uppdraget att samordna regionernas resurser (Socialstyrelsen 2014a).
Många personer med erfarenhet av patient- och närståenderåd inom RCC beskriver att patientföreträdare varit en stark kraft för att öka fokus på och sprida strukturerade arbetssätt för cancerrehabilitering. Man nämner exempelvis tidiga och återkommande behovsbedömningar för att tidigt fånga och åtgärda behov som växlar över tid. Här återkommer ofta att patientföreträdare bidragit till att utveckla och implementera Min vårdplan och kontaktsjuksköterskefunktionen, samt arbete med mötesplatser som Livsgnistan, Ljuspunkten och Kraftens hus (Vård- och omsorgsanalys 2024).
Däremot bedömer Socialstyrelsen (2022b) att det krävs starkare regional och kommunal styrning för att det nationella vårdprogrammet ska få genomslag. En mer kraftfull styrning från nationell nivå efterfrågas i vissa av Socialstyrelsens workshoppar om rehabilitering. Deltagare upplevde dock att det finns ett motstånd mot nationella initiativ.
Samarbetet med regional och kommunal primärvård kan bli bättre
Patientorganisationer pekar på oklar ansvarsfördelning mellan specialist- och primärvård som en orsak till brister i rehabilitering. Att rehabiliteringsområdet involverar flera olika specialiteter, aktörer och nivåer är en komplicerande faktor. Vårdprogram som omfattar flera nivåer bedöms som generellt svårare att implementera (Socialstyrelsen 2022b). I dag bedömer Socialstyrelsen att information och utbildning om cancerrehabilitering behöver nå fler delar av vården, och att materialet i högre grad behöver riktas till olika målgrupper, exempelvis regional och kommunal primärvård (Socialstyrelsen 2022b).
Kontaksjuksköterskan viktig för rehabiliteringen
Kontaksjuksköterskorna har en central roll för rehabilitering eftersom de har till uppgift att ta fram en rehabiliteringsplan för patienten (Cancerfonden och Bröstcancerförbundet 2021). Patientorganisationer pekar på brist på kontaktsjuksköterskor som ett hinder för god rehabilitering. I undersökningen av rehabilitering för bröstcancerpatienter beskriver intervjupersoner också att en faktor som kan bidra till variationen i implementering av vårdprogrammet är skillnader i vilka förutsättningar kontaktsjuksköterskan har att göra sitt jobb (Cancerfonden och Bröstcancerförbundet 2021).
Bristande uppföljningsmöjligheter försvårar
En svårighet i implementeringen av vårdprogrammet är att det inte går att följa nationellt vilka rehabiliteringsåtgärder som ges (Socialstyrelsen 2022b). Idag saknas det data om cancerrehabilitering på samhällsnivå, eftersom besök och åtgärder inte registreras systematiskt på ett sådant sätt att det går att följa upp. En stor del av de yrkesgrupper som arbetar med rehabilitering omfattas inte av uppgiftsskyldigheten till nationella hälsodataregistret (patientregistret på Socialstyrelsen), vilket innebär att majoriteten av den rehabilitering som utförs inte rapporteras till nationella hälsodataregistret trots att många åtgärdskoder finns. Detta innebär att det inte är möjligt att överblicka och utvärdera olika rehabiliteringsinsatser (SOU 2019:29).
3.3.7 Den palliativa vården tycks ha förbättrats, men mycket finns kvar att göra
Utredningen om en cancerstrategi lyfte fram den palliativa vården som resursmässigt eftersatt med brister i tillgänglighet och kvalitet och stora geografiska skillnader.
Insatserna inom palliativ vård i överenskommelserna är koncentrerade till slutet av perioden, men att arbeta med palliativ vård ingår också som en del i RCC:s uppdrag sedan start. År 2009 fick Socialstyrelsen i uppdrag att ta fram ett nationellt kunskapsstöd (Socialdepartementet och SKR 2011; Socialstyrelsen 2013), och RCC publicerade 2012 ett nationellt vårdprogram. Vårdprogrammet för palliativ vård omfattar till skillnad från de övriga vårdprogram som tagits fram inom RCC inte bara cancerområdet utan patienter oavsett diagnos. År 2022 tillkom ett vårdförlopp för palliativ vård.
Arbetet har varit inriktat på implementeringen av det nationella vårdprogrammet. RCC har även haft i uppdrag att stödja samverkan om palliativa insatser inom den nära vården. Kopplade till RCC finns idag palliativa processledare och en nationell arbetsgrupp för dem (RCC i samverkan 2023e). Den nationella arbetsgruppen för palliativ vård, som bland annat arbetar med att främja implementering av kunskapsstöd, ligger däremot under programområdet äldres hälsa.
Kvaliteten tycks ha utvecklats positivt
Vi har undersökt kvaliteten i sex olika dimensioner av palliativ vård specifikt för cancerpatienter. För de flesta syns en positiv utveckling över tid, även om nuläget jämfört med de nationella målnivåerna varierar mellan diagnoser. Sammantaget ser det bättre ut för indikatorerna för dokumenterat brytpunktssamtal, injektion mot oro/ångest och opiod vid smärtgenombrott, men sämre för trycksår, smärtskattning under sista veckan och dokumenterad munhälsobedömning (Palliativregistret).
Resultaten bör tolkas med försiktighet eftersom statistiken är hämtad från dödsfallsenkäten i palliativregistret, vars täckningsgrad inte är fullständig och som varierar mellan olika vårdformer (Ledningsgruppen för svenska palliativregistret 2022).
I vår intervjustudie lyfter vissa fram att resultatutvecklingen inom den palliativa vården är starkare för patienter med cancer än för andra diagnosgrupper, troligen eftersom cancerstrategin lyft fram den gruppen av patienter. Intervjupersoner har också uttryckt farhågor om att ett för starkt fokus på cancerpatienter riskerar att tränga undan andra diagnosgrupper.
RCC och cancerstrategin har bidragit, men roller och samarbete kan utvecklas
I likhet med rehabilitering beskrivs både RCC och den nationella cancerstrategin tidigt under perioden ha varit viktiga för att uppmärksamma området (Socialstyrelsen 2014a). Den stora mängden aktörer inom palliativ vård ställer samtidigt stora krav på samverkan och avgränsningar. Socialstyrelsen (2021d) bedömer att det finns en viss otydlighet i roller och ansvar på området, och menar att RCC:s samarbete med primärvården, inklusive kommunerna, behöver utvecklas.
Den bilden bekräftas i vår intervjustudie. Vissa beskriver ett otydligt ansvar på nationell nivå när det gäller palliativ vård. Det handlar till exempel om att området har en något undanskymd roll i kunskapsstyrningsorganisationen. Det beskrivs som svårt att få regioner och verksamsamheter att prioritera att implementera kunskapsstyrning inom området. En försvårande faktor är att det är så många olika typer av verksamheter som kunskapsstöden behöver nå ut till. Intervjupersoner menar också som att det saknas en struktur för implementering både på nationell och regional nivå.
Den palliativa vården beskrivs som ett litet område, där personalen ofta hör till andra enheter, och där god samverkan beror på insatser från ”eldsjälar” eller initiativ från enstaka personer på ledningsnivå. Det beskrivs att förankringen hos huvudmännen är svag och att det finns en utveckling mot att verksamheter prioriterar bort palliativ vård till förmån för vad de anser är sin kärnverksamhet. Hur väl samverkan på verksamhetsnivå fungerar beror också på andra faktorer. Till exempel försvårar en mångfald av privata aktörer inom primärvården en mer strukturerad samverkan.
3.4 Minska regionala skillnader i överlevnadstid efter en cancerdiagnos
Utredningen En nationell cancerstrategi beskrev att den decentraliserade vården fört med sig omotiverade regionala skillnader i praxis och utfall. Bland annat såg utredningen betydande skillnader i vilka läkemedel som ordineras på rekvisition.
Många insatser som skett på cancerområdet sedan cancerstrategin togs fram har haft minskade regionala skillnader som ett av sina mål, och insatserna överlappar därför med flera andra mål. I det här avsnittet tar vi upp insatser för jämlik tillgång till medicinsk teknik och läkemedel samt samordning av screeningprogram.
Arbetet med regional jämlikhet har förutom överlevnad även fokuserat på skillnader i omhändertagande och områden som berör patienters livskvalitet. Utvecklingen inom de områdena beskriver vi sist i avsnittet.
3.4.1 Regionala skillnader i överlevnad har minskat
Generellt har de regionala skillnaderna i överlevnad minskat sedan 2009. För de fem diagnoser vi tittat närmare på har variationen mellan regioner i 5-årsöverlevnad minskat i fyra fall (Vården i siffror). Socialstyrelsen har funnit att det sammantaget kvarstår regionala skillnader, till exempel har regioner med universitetssjukhus bättre resultat (Socialstyrelsen 2021a).
Gemensam struktur en tillgång, men varierande genomslag för insatser
Socialstyrelsen bedömer att uppbyggnaden av RCC-strukturen och dess aktiviteter över lag förbättrat förutsättningarna för jämlik vård (Socialstyrelsen 2023). Samtidigt varierar genomslaget för olika insatser mellan regioner. I våra intervjuer pekar aktörer på varierande genomslag för vårdprogrammen mellan regioner.
I vår närmade analys av fyra cancerformer ser vi till exempel att tillgången till multidisciplinär konferens (MDK) skiljer sig åt både mellan diagnos och mellan regioner. Skillnaderna mellan regioner är små inom bröstcancer och kolorektalcancer, men däremot stora inom lung- och njurcancer. Det ser samtidigt ut som om skillnaderna i förekomsten av MDK mellan regioner har minskat för de diagnoserna. För kolorektalcancer har skillnaderna mellan regioner minskat påtagligt sedan 2009, liksom inom bröstcancer. För njurcancer är dataunderlaget otillräckligt, men den data som finns tyder på att skillnaderna mellan regionerna minskat även om de fortsatt är stora (Kvalitetsregister för respektive cancerform).
3.4.2 Insatser för jämlik tillgång till medicinsk teknologi och läkemedel
Ett område där det skett arbete för minskade regionala skillnader är införande och uppföljning av nya läkemedel. Modellen ”ordnat införande” har medfört ett mer strukturerat sätt att samverka om introduktionen av nya läkemedel och medicinteknik, men det finns fortfarande regionala skillnader i användningen av flera läkemedel.
RCC i samverkan har haft i uppdrag att göra analyser kring precisionsmedicin och att stödja implementering av precisionsdiagnostik på ett jämlikt och effektivt sätt över landet. En annan insats som RCC-strukturen arbetat med är en gemensam nomenklatur och ett standardiserat innehåll för cytostatikakurer, samt ett nationellt regimbibliotek. Insatserna har bland annat omfattat att upprätta gemensamma styrdokument och en nationell databas varifrån man kan exportera till lokala system (Socialdepartementet och SKL/SKR 2011-2012, 2020-2023). Läkemedelsverket och framförallt Tandvårds- och läkemedelsförmånsverket (TLV) har under perioden haft en rad uppdrag kring hälsoekonomiska bedömningar och uppföljning av nya cancerläkemedel.
Cancerstrategin har utvecklat införandet av nya läkemedel
I betänkandet från 2009 lades flera förslag fram som syftade till att utveckla införandet och uppföljningen av nya läkemedel. Förslagen handlade bland annat om att sjukvårdshuvudmännen skulle etablera en samordning för ett strukturerat införande av nya läkemedel och ny teknik. Syftet var att patienter skulle få en snabbare tillgång till bättre behandlingar, oavsett var i landet de bor (SOU 2009:11).
Genom förslagen i den nationella cancerstrategin samt kompletterande initiativ i den nationella läkemedelstrategin har en modell för nationellt ordnat införande av nya läkemedel etablerats. Ordnat införande innebär att regionerna samverkar med läkemedelsföretagen och myndigheter som TLV och Läkemedelsverket om introduktionen av nya läkemedel. Modellen omfattar flera funktioner: kartläggning av nya läkemedel, hälsoekonomisk bedömning, beslut, avtal med läkemedelsindustrin, rekommendationer samt uppföljning. I ordnat införande ingår nu både receptbelagda läkemedel inom förmånen och rekvisitionsläkemedel (Regionernas samverkansmodell för läkemedel 2023a). Sedan 2020 omfattar ordnat införande även medicintekniska produkter. Hittills har rekommendationer för tio medicintekniska produkter lämnats, varav fyra har avsett diagnostik eller behandling av cancer (Regeringen 2011; Regionernas samverkansmodell för medicinteknik 2023).
Vård- och omsorgsanalys utvärderade under 2015–2016 ordnat införande av nya läkemedel. Vi har inte gjort någon förnyad utvärdering, men vår övergripande slutsats då var att modellen bidrog till en mer jämlik läkemedelsanvändning genom nationella rekommendationer och avtal. Men vi såg också exempel på att introduktionen i regionerna drog ut på tiden och att regionala skillnader kvarstod trots ordnat införande (Vård- och omsorgsanalys 2016). Att det finns regionala skillnader i användningen av cancerläkemedel visar även en analys som tar tagits fram inom ramen för regionernas samverkansmodell. Analysen bygger på försäljningsdata från E-hälsomyndigheten och visar att användningen av immunterapier, så kallade PD(L)-hämmare, är större i de sydöstra och västra regionerna, än i de norra och mellersta regionerna samt i Stockholm (Regionernas samverkansmodell för läkemedel 2023b; Lif 2023). En slutsats av vår analys av ordnat införande är att den nationella nivån till viss del kan styra mot en mer jämlik användning, men att regionala och lokala faktorer kan ha stor betydelse för introduktionen av nya läkemedel. Det handlar exempelvis om finansieringsmodeller och införandeprocesser samt tillgång till avancerad diagnostik och kompetens inom regionen (Vård- och omsorgsanalys 2016). I våra intervjuer lyfter flera fram kvarstående regionala skillnader i läkemedelsanvändningen som problematiskt ur jämlikhetssynpunkt.
3.4.3 Samordningen av screening uppfattas som otillräcklig
Att minska regionala skillnader i införande och deltagande i screeningprogram skulle kunna påverka regionala skillnader i överlevnad genom mer jämn tidigare upptäckt av cancer. Det har skett en rad insatser under perioden för mer samordnad screening med mindre regionala skillnader. RCC har bland annat arbetat med ökad nationell samordning mellan de befintliga screeningprogrammen och generiska kallelsesystem (Socialdepartementet och SKL/SKR 2011, 2020, 2021, 2022, 2023). Socialstyrelsen (2022c) har i slutet av perioden haft i uppdrag att arbeta för en mer nationellt samordnad screening.
Screening för livmoderhalscancer och kolorektalcancer varierar stort mellan regioner
I vår intervjustudie framhåller intervjupersoner det positiva med att Sverige har offentligt finansierade screeningprogram, med ett högt deltagande. Samtidigt menar de också att införandet av de nationella screeningprogrammen har gått långsamt och att de regionala skillnaderna är problematiska.
Screeningprogrammet för bröstcancer har relativt små regionala skillnader, bortsett från att Region Stockholm har ett lägre deltagande (70 procent jämfört med rikssnittet 80 procent) (Cancerfonden 2021). Täckningsgraden för screeningprogrammet för livmoderhalscancer varierar däremot med omkring 20 procentenheter mellan regioner (Socialstyrelsen 2020). Övergången till det nya screeningprogrammet för livmoderhalscancer, som inleddes 2015, skedde i olika takt i olika regioner. År 2019 hade till exempel hälften av regionerna gått över till det nya programmet (Socialstyrelsen 2019c). Cancerfonden (2021) menar att den ojämna övergången bland annat berodde på brister i samordningen.
När det gäller screening för kolorektalcancer finns mycket stora regionala skillnader, eftersom alla regioner ännu inte infört programmet. Socialstyrelsen rekommenderar sedan 2014 alla regioner att införa programmet, men först 2022 började screeningprogrammet införas i samtliga regioner. En del i att införandet tog lång tid var att man ville invänta resultatet av SCREESCO-studien, där 18 regioner deltog, och olika metoder för screening för kolektoralcancer jämfördes. Studien avslutades dock 2019, och införandet har alltså dröjt ytterligare sedan dess (Cancerfonden 2021). Socialstyrelsen pekar i våra intervjuer på att Sveriges införande av screening för kolektoralcancer varit sent i ett internationellt perspektiv.
Mer samordning och nationella register efterfrågas
Vi har inte så mycket underlag om hur väl insatserna som initierats inom ramen för cancerstrategin har fungerat, men det framkommer några generella lärdomar om vad som fungerat bättre och sämre i arbetet med screening.
Mer samordning kring screeningprogram har efterfrågats i Socialstyrelsens uppföljningar (Socialstyrelsen 2019c, 2022c). Socialstyrelsen (2019c) har funnit att det finns en god dialog och struktur inom de enskilda screeningprogrammen, men att det behövs en bättre nationell dialog mellan screeningprogrammen, regionerna och myndigheter. Ett dialogforum har därför nyligen inrättats (Socialstyrelsen 2022c).
Flera aktörer bedömer att det behövs tydligare nationell styrning för snabbare och jämnare införande av screening (Socialstyrelsen 2019c; Cancerfonden 2021). I vår undersökning till de olika RCC framkommer uppfattningen att den nationella styrningen borde vara tydligare och överordnas den regionala. En tydligare nationell styrning nämns som ett exempel på en lyckad nationell samordning i ett av screeningprogrammen, vilket bedömts vara resurseffektivt och jämlikt. För övriga screeningprogram finns regionala lösningar som enligt informanterna varit mer resurskrävande och inte gett samma vinster i form av jämlikhet och likvärdig uppföljning.
En svårighet i arbetet har varit att det fortfarande saknas nationella register som möjliggör en systematisk nationell uppföljning av screeningprogrammen (Socialstyrelsen 2023a). Yttre faktorer som material- och kompetensbrist, samt pandemin, har också påverkat screeningen (Socialstyrelsen 2022c).
3.4.4 Insatser för minskade regionala skillnader har även gällt livskvalitet och omhändertagande
Cancerstrategins mål om minskade regionala skillnader omfattar enbart skillnader i överlevnad. Samtidigt pekar utredningen ut andra skillnader mellan regioner som problematiska, till exempel omotiverade skillnader i väntetider (SOU 2009:11). Även i våra intervjuer pekar aktörer på regionala skillnader i omhändertagande och förutsättningarna för god livskvalitet efter en cancerdiagnos, och menar att även de områdena är viktiga för en jämlik vård.
Regionala skillnader i rehabilitering och palliativ vård
Under perioden har det skett en rad insatser för att minska skillnaderna mellan regioner när det gäller omhändertagandet inklusive väntetider, samt i rehabilitering och palliativ vård. Minskade regionala skillnader har till exempel varit en del i syftet med nationella vårdprogram för rehabilitering och palliativ vård.
Socialstyrelsen bedömer att det finns skillnader i tillgång till rehabilitering och implementering av nationella vårdprogrammet för rehabilitering både inom och mellan regioner (Socialstyrelsen 2022b). Även i våra intervjuer beskriver aktörer att utbudet av rehabilitering är ojämlikt fördelat över landet.
I intervjustudien betonas också att tillgången till palliativ vård är mycket ojämlik över landet. Vi ser i vår närmare analys av fyra cancerformer att de regionala skillnaderna tycks ha minskat över tid för vissa kvalitetsindikatorer inom palliativ vård, men att stora skillnader kvarstår för vissa indikatorer. Spridningen mellan regioner minskade mellan 2011 och 2022 för förekomsten av trycksår och injektion mot oro/ångest vid behov. Spridningen minskade också mellan 2018 och 2022 för dokumenterat brytpunktssamtal. När det gäller injektion av opiod vid smärtgenombrott var spridningen relativt liten både 2011 och 2022. För smärtskattning sista veckan och dokumenterad munhälsobedömning var spridningen mellan regioner däremot stor både 2011 och 2022 (Palliativregistret).
Regionala skillnader i omhändertagande tycks ha minskat men är ibland stora
Flera insatser som initierats på nationell nivå har syftat till att minska skillnaderna mellan regioner när det gäller omhändertagandet av patienter.
Skillnaderna mellan regioner är relativt små när det gäller patienters upplevelser av omhändertagandet, enligt de patientenkäter som genomförs (Åkesson och Tufvesson Stiller 2019). Däremot finns tydliga skillnader om man ser till vissa processmått över förutsättningarna för ett gott omhändertagande.
Ett av målen med de standardiserade vårdförloppen var ökad jämlikhet, bland annat att minska de stora skillnaderna i väntetider mellan regioner. Riksrevisionen (2023) har funnit att genomslaget för vårdförloppen varierar mellan regioner. Skillnaderna i väntetider har minskat något över tid, men påtagliga skillnader kvarstår också (Socialstyrelsen 2019a; Riksrevisionen 2023). Andelen patienter som utreddes inom ledtiden varierade till exempel 2022 mellan 31 och 58 procent i olika regioner (Socialstyrelsen 2022a).
När det gäller omhändertagande har vi bara kunnat undersöka förekomsten av kontaktsjuksköterskor och individuella vårdplaner för patienter med njurcancer och bröstcancer. För de cancerformerna syns en positiv utveckling i minskade regionala skillnader jämfört med 2014 respektive 2015, framförallt inom njurcancer där skillnaderna var större i utgångsläget (Kvalitetsregistret för respektive cancerform).
3.5 Minska skillnader mellan befolkningsgrupper i insjuknande och överlevnadstid
I betänkandet En nationell cancerstrategi för framtiden (SOU 2009:11) beskrevs tecken på sociala skillnader i risken för en rad olika cancerformer, och även på att prognosen vid många cancerformer skiljde sig åt utifrån socioekonomi. Att minska dessa skillnader skulle förutom ökad jämlikhet enligt utredningen även kunna minska den totala sjukligheten och dödligheten i cancer.
Vi ser att skillnaderna i insjuknande mellan socioekonomiska grupper tycks vara större idag än när cancerstrategin togs fram. Målet har inte varit i fokus i exempelvis överenskommelser under perioden, även om det ingår i RCC:s uppdrag. Frågan bedöms ha varit svår att arbeta med och det tycks ha saknats ett gemensamt nationellt grepp.
Skillnader i hälsa är dock ett problem som omfattar både vården och samhället i bredare bemärkelse. Kommissionen för jämlik hälsa (SOU 2017:4; SOU 2017:47) bedömde 2017 att hälsoskillnaderna generellt inte hade minskat sedan det tidigare folkhälsopolitiska ramverket utvecklades 2002–2003. Kommissionen menade att utvecklingen delvis berodde på orsaker bortom det folkhälsopolitiska arbetet, men att brister i det folkhälsopolitiska ramverket också bidragit till att det inte fått genomslag.
3.5.1 Skillnaderna i insjuknande tycks ha ökat
Vi har undersökt hur skillnaderna i insjuknande mellan befolkningsgrupper utvecklats. Vi har däremot inte kunnat göra någon egen analys av om skillnaderna mellan socio- ekonomiska grupper i överlevnad minskat under perioden, eftersom det inte rymts inom det här relativt begränsade uppdraget. Analyser från Socialstyrelsen och Cancerfonden tyder på att ojämlikhet i både insjuknande och överlevnad kvarstår, och på vissa punkter har försämrats (Socialstyrelsen 2021a, 2023; Cancerfonden 2018, 2020a). Även patientorganisationer har framfört att de ser ökande socioekonomiska skillnader inom vården, och beskriver det som en svaghet i svensk cancervård. Socialstyrelsen (2023a) bedömer att regionerna har kommit olika långt i arbetet med socioekonomiska skillnader. När det gäller insjuknande syns det generellt en ökad skillnad mellan utbildningsgrupper inom de cancerformer vi undersökt närmare (njurcancer, lungcancer, kolorektalcancer och bröstcancer). Skillnaderna i insjuknande mellan utbildningsgrupper varierar mellan cancerformer och kön. För njur- lung- och kolorektalcancer är insjuknandet lägre bland personer med längre utbildning. Inom dessa cancerformer har skillnaden i insjuknande mellan utbildningsgrupper ökat under perioden 2009–2021, förutom när det gäller lungcancer bland kvinnor där skillnaden minskat. För bröstcancer, där insjuknandet är högre bland personer med längre utbildning, har skillnaden utifrån utbildning inte förändrats (Aggregerade data från Socialstyrelsen).
Analysen av dessa cancerformer tyder på att skillnaderna i insjuknande idag är mindre inom kolorektalcancer, något större inom bröstcancer, större inom njurcancer och i synnerhet större inom lungcancer.
En faktor som kopplats till skillnader mellan socioekonomiska grupper i överlevnad är deltagande i screeningprogram. Här har vissa insatser initierats i den nationella styrningen. Vi saknar underlag för att bedöma hur skillnaderna utvecklats över tid, men det framkommer att skillnader kvarstår. I en underlagsrapport till Cancerfondsrapporten visade exempelvis Institutet för hälso-och sjukvårdsekonomi (IHE) på skillnader i deltagargrad beroende på inkomstnivå, där stadsdelar med lägre inkomstnivå hade lägre deltagande i bröstcancerscreening och stadsdelar med högre inkomstnivå hade högre deltagande (Institutet för Hälso- och Sjukvårdsekonomi 2021). Personer med kortare utbildning deltar även i lägre utsträckning i livmoderhalscancerscreeningen (Socialstyrelsen 2020a). Cancerfonden (2021) har efterfrågat mer fokus på grupper och områden med lågt deltagande i screening för att öka täckningsgraden.
En annan aspekt av skillnader mellan grupper i befolkningen framkommer i den analys som Socialstyrelsen (2023a) har gjort av skillnader mellan kvinnor med bröstcancer med och utan psykisk funktionsnedsättning. Analysen visar på att kvinnor med en psykisk funktionsnedsättning hade längre framskriden tumör vid diagnosticering, och tydligt lägre 5-årsöverlevnad.
3.5.2 Litet fokus på skillnader mellan grupper i den nationella styrningen
I den nationella styrningen framkommer mycket få insatser där minskade skillnader mellan befolkningsgrupper är det huvudsakliga målet, och det tycks inte ha tagits några mer systematiska grepp nationellt. De insatser som beskrivs i överenskommelser handlar främst om att nå ett mer jämlikt deltagande i screening. I RCC:s uppdrag från 2011 ingick också att ta fram och implementera en långsiktig plan för sjukvårdsregionens arbete med prevention och tidig upptäckt, där särskilda åtgärder för ökad jämlikhet skulle ingå. Även i RCC:s mål för sitt arbete framöver ingår minskade skillnader mellan befolkningsgrupper som en del i att arbeta med screening (RCC i samverkan 2023d). I uppföljningen framgår att det skett olika lokala initiativ på området, och att regionerna arbetar på olika sätt. Socialstyrelsen (2023a) beskriver att det pågår flera projekt inom olika RCC och i olika regioner, men att det behövs mer samarbete på nationell nivå. Ett medskick från patientorganisationer är att fler aktörer, som företag och civilsamhälle inklusive patient- och närståendeorganisationer, behöver involveras i arbetet och att man behöver ha ett helhetsperspektiv.
3.5.3 RCC har en otydlig roll i att minska skillnader mellan grupper
Socialstyrelsen bedömer att jämlikhet mellan befolkningsgrupper varit ett av de svårare områdena för RCC att arbeta med (Socialstyrelsen 2021d). RCC:s kartläggningar bedömdes 2016 som en bra grund för det fortsatta arbetet (Socialstyrelsen 2016b). Samtidigt menade Socialstyrelsen också att RCC:s roll behövde bli tydligare och uppmanade RCC att ta en mer aktiv roll (Socialstyrelsen 2016b). Socialstyrelsen (2021d) betonar att mycket arbete återstår när det gäller jämlikhet. Även om det strukturerade arbetet med kvalitetsregister, standardiserade vårdförlopp och regimbibliotek enligt Socialstyrelsen (2021d) förbättrat förutsättningarna för att arbeta med jämlik vård, pekar Socialstyrelsen (2023a) också på att det råder osäkerhet inom flera RCC om hur man kan arbeta mot skillnader mellan befolkningsgrupper. Socialstyrelsen (2023a) menar att RCC:s arbete inom jämlikhet behöver fokuseras, och att utökat samarbete mellan de olika RCC skulle vara en del i det.
3.6 Insatser som berör samtliga mål
Många av de insatser som skett inom ramen för genomförandet av cancerstrategin syftar till att uppnå flera av strategins mål, eller att skapa förutsättningar för samtliga mål. Uppbyggnaden av en struktur för kunskapsstyrning och implementering av cancerstrategin genom RCC, förutsättningarna för uppföljning av cancervården och forskning, samt kompetensförsörjning, är områden som berör samtliga mål i cancerstrategin.
3.6.1 Inrättandet av RCC uppfattas som viktigt och framgångsrikt
Syftet med att inrätta RCC var bland annat att stödja kunskapsutveckling och kunskaps- spridning. RCC har en central roll i kunskapsstyrningen på cancerområdet och arbetar med alla cancerstrategins mål.
I betänkandet syftar ”cancercentrum” på centrum som bedriver både kunskapsstyrning, vård och forskning, det vill säga både det som RCC idag gör och det som universitetssjukhus eller CCC:er gör. I samband med inrättandet valde man att istället att ge RCC en mer renodlad roll inriktad på kunskapsstyrning.
RCCstrukturen har varit en stor tillgång
Socialstyrelsen finner i sina uppföljningar att RCC-strukturen över lag upplevs som välfungerande. Under implementeringsprocessen har Socialstyrelsen lyft fram att RCC-strukturen medfört nytta jämfört med tidigare struktur genom att mer arbete sker sjukvårdsregionalt eller nationellt i stället för separat i de olika regionerna, och bedömt att modellen skulle kunna fungera som förlaga för kunskapsstyrningen på andra områden (Socialstyrelsen 2016a, 2021d). Socialstyrelsen (2016a) bedömer att den modell för kunskapsstyrning som utvecklats inom RCC är genomtänkt och hänger samman.
I vår intervjustudie nämns RCC av flera som en styrka i cancervården. Det lyfts fram att RCC har bidragit till att ge cancervården en stark struktur jämfört med andra vård- områden. RCC bedöms ha bidragit till kunskapsproduktionen, kunskapsspridningen och kunskapsstyrningen på cancerområdet, med till exempel tydliga flöden för olika cancergrupper genom t.ex. standardiserade vårdförlopp, processledare som håller i arbetet, nationella vårdprogram, stöd till kvalitetsregister och tillgång till data. Intervjupersoner lyfter också att RCC bidragit till god samverkan inom cancerområdet och är en bra ingång för patientorganisationerna.
En framgångsfaktor har varit att RCC har strategin att luta sig mot, med ett tydligt uppdrag och resurser. En viktig del i organisationen har bedömts vara rollen som länk mellan staten och dess satsningar och regionerna och det har setts som en styrka att RCC är en fristående part i dialogen med andra aktörer som staten, regionerna och kommunerna.
3.6.2 Nationella vårdprogram uppfattas ha bidragit till flera mål
Framtagande och implementering av nationella vårdprogram har upptagit mycket fokus i överenskommelserna på cancerområdet under perioden. Vårdprogrammen syftar både till att nå målen om ökad överlevnad, bättre omhändertagande och minskade skillnader mellan regioner och befolkningsgrupper (RCC i samverkan 2023j). De tas fram av de nationella vårdprogramsgrupperna med stöd av RCC i samverkan.
Idag finns ett femtiotal nationella vårdprogram på cancerområdet. De flesta är diagnosspecifika, men det finns även diagnosgemensamma vårdprogram för till exempel palliativ vård, långtidsuppföljning efter barncancer och cancer under graviditet (RCC i samverkan 2023k).
Vårdprogrammen uppfattas som välfungerande, men effekterna för patienterna är ännu okända
Baserat på den utvärdering som RCC i samverkan genomförde 2016 uppfattas införandet av vårdprogrammen ha fungerat väl, även om det är svårt att bedöma effekter för patienter utifrån registerdata (RCC i samverkan 2016b).
Enligt de läkare som deltagit i utvärderingen har vårdprogrammen främst medfört mer enhetligt handläggande av patienter med mer stöd till patienter och närstående. I vissa fall uppfattas samordning och kontinuitet ha påverkats positivt. Den medicinska förändringen bedöms däremot variera mellan de olika vårdprogrammen. Vårdprogrammen bedöms ha befäst och skyndat på pågående processer. De uppfattas ha stöttat sådant som patientinformation, dokumentation, användande av vårdplan, kontaksjuksköterskor och multidisciplinär konferens.
RCC i samverkan (2016b) bedömer utifrån sin personalenkät att vårdprogrammen är viktiga i det dagliga arbetet för läkare, medan kontaksjuksköterskor använder vårdprogrammen i varierande grad beroende på arbetsuppgifter. Vårdprogrammen uppfattas som särskilt viktiga när verksamheten har hög personalomsättning. Vårdprogrammen uppfattas inte ha medfört större organisationsförändringar. Nya vårdprogram bedöms däremot ofta innebära kostnader för regioner. Det beskrivs också att vårdprogrammen har kunnat fungera som hävstång i diskussioner om resurser för att skapa politisk vilja till förändring. Flera i vår intervjustudie anser att det är en generell styrka hos cancerstrategin att det nu finns vårdprogram på nästan alla områden, vilket saknades 2009. En styrka är också att vårdprogrammen uppdateras löpande, vilket innebär att vården hela tiden kan arbeta utifrån en uppdaterad kunskap om behandlingar.
Men implementeringen ses som en svårighet; till exempel att vårdprogrammen anpassas i respektive region, vilket skapar en tröghet i systemet. Det framkommer också ett behov av att verksamhetscheferna i högre grad stödjer implementering av vårdprogrammen och andra kunskapsstöd. Intervjupersoner och informanter beskriver det finns en upplevelse i vården av att det lokala ledningsstödet som krävs för implementering inte finns.
Medicinsk kvalitet och systematik i införandet viktigt
RCC i samverkan (2016b) bedömer att två styrkor i införandet av vårdprogrammen är att de varit väl förankrade och hållit hög medicinsk kvalitet. Däremot hade införandet enligt deras intervjupersoner kunnat vara mer systematiskt. Något som efterfrågats är bättre konsekvensanalys på förhand, med kostnadsberäkning och bedömning av lokal tillämplighet. Även en mer systematisk och utvecklad uppföljning har efterfrågats. Det har ibland setts som respektive verksamhets ansvar.
3.6.3 Cancerforskning
På grund av uppdragets omfattning har vi inte haft möjlighet att grundligt kartlägga cancerforskningens förutsättningar. Här beskriver vi bara de bedömningar som aktörer gjort i uppföljningar och i våra intervjuer. Avsnittet bör därför ses som en inledning på en mer omfattande analys av cancerforskningens förutsättningar och möjliga utvecklingsvägar.
Vissa forskningsområden uppfattas som underprioriterade
Flera av de områden som pekades ut som angelägna att satsa på inom cancerforskningen i betänkandet En nationell cancerstrategi för framtiden kvarstår som utmaningar idag. I vår intervjustudie uttrycks särskilt behovet av fler kliniska studier. Flera beskriver att utvecklingen gått i fel riktning när det gäller kliniska studier, att det går långsammare i Sverige eller att Sverige halkat efter andra länder på området. Även Cancerfonden (2023) har pekat på att den kliniska forskningen minskar i omfattning. Flera patientorganisationer lyfter i våra intervjuer fram vikten av ökade och jämlika möjligheter att delta i kliniska studier samt att ny kunskap införs snabbare. De menar också att det är svårt för patienter att delta i studier i övriga Norden och EU.
Barncancerområdet ligger enligt våra intervjuer långt fram när det gäller forskning, och beskrivs som en forskningsintensiv verksamhet med många internationella studier och goda möjligheter till forskningsanslag. Jämlik tillgång till kliniska studier i olika delar av landet beskrivs dock som en svårighet även inom barncancer.
Vissa intervjupersoner och andra informanter menar att det sker felaktiga prioriteringar mellan grundforskning och klinisk forskning. De beskriver att det är lättare att få medel till grundforskning, samtidigt som det finns särskilt goda förutsättningar för klinisk forskning i Sverige som inte nyttjas tillräckligt.
Flera av våra intervjupersoner och informanter lyfter också fram att olika status på forskningsområden försvårar, och att det läggs mer resurser på områden som är nya och har hög status trots att det inte nödvändigtvis motsvarar de största behoven. De menar att det behövs mer forskning inom områden utanför diagnos och behandling. Det handlar om primärprevention, omvårdnadsforskning, livskvalitet, uppföljning och rehabilitering, palliativ vård, tidig upptäckt i primärvården samt kostnadsfrågor och prioriteringar. Intervjupersonerna och informanterna menar att det läggs mindre resurser på forskning inom dessa områden än vad som är motiverat.
Uppföljningar har särskilt betonat behovet av mer forskning ur primärvårdsperspektiv. Primärvården har enligt Cancerfonden (2023) en alltför begränsad roll i forskningen, och det saknas i hög grad forskning med utgångspunkt i primärvårdens behov, till exempel tidig upptäckt (Socialstyrelsen 2023a). Även patientorganisationer menar i vår enkät att det råder brist på primärvårdsforskning.
Insatser för att främja cancerforskning
Vi har inte gjort någon fullständig kartläggning av insatserna för att främja cancerforskning. Här beskriver vi insatser som lyfts fram kopplat till implementeringen av cancerstrategin. Flera statliga myndigheter har haft uppdrag som syftat till att främja forskning på cancerområdet. Vinnova har exempelvis haft en rad uppdrag med koppling till forskning och innovation på cancerområdet, bland annat med fokus på precisionsmedicin (Vinnova 2018a, 2018b, 2021a, 2021b, 2022, 2023).
Det har även skett en rad olika typer av insatser inom ramen för RCC för att på olika sätt främja forskning. I RCC:s uppdrag ingår att stärka den kliniska forskningen i sin sjukvårdsregion (Socialdepartementet 2011), och RCC och RCC i samverkan har under senare delen av perioden haft särskilda uppdrag kring att stödja deltagande i kliniska studier (Socialdepartementet och SKL/SKR 2018–2023). RCC har också under hela perioden arbetat med de nationella kvalitetsregistren och RCC i samverkan har arbetat med att utveckla registerforskningen (Socialdepartementet 2011; Socialdepartementet och SKL/SKR; Socialstyrelsen 2016a).
Socialstyrelsen har i sin uppföljning pekat på att RCC har drivit på utvecklingen i regionerna med t.ex. forskningssjuksköterskor, biobanking och kliniska prövningsenheter. RCC:s stödarbete har också uppfattats bidra till större fokus på jämlikhetsaspekter i forskningen (Socialstyrelsen 2016b). Vad vi känner till har inte resultatet av RCC:s arbete för att stödja forskningen utvärderats och det är inte ett område vi fångat i våra intervjuer. I våra intervjuer menar flera att den nationella samordningen av forskningsresurser behöver bli bättre. Decentraliserad styrning beskrivs återkommande i våra intervjuer som en svårighet, där processer sker separat i de olika regionerna. Intervjupersoner lyfter även att det behövs samordning av forskningsdata. De beskriver att det saknas tillräckligt samlat grepp, och att området därför blir komplext och fragmentiserat. Vissa menar också att det saknas kompetens hos finansiärer och att styrningen inte är tillräckligt långsiktig.
Utvecklingen mot CCC ses som positiv för integration av forskning och vård
Flera av våra intervjupersoner beskriver att det saknas en incitamentsstruktur för att kombinera vård och forskning och att det är ont om tjänster där vård och forskning kombineras. Även Cancerfonden (2023) menar att det saknas incitament att kombinera arbete med vård och forskning. Både Cancerfonden (2023) och flera av våra intervjupersoner bedömer samtidigt att det sker en positiv utveckling när det gäller att koppla vård och forskning starkare samman i och med utvecklingen av Comprehensive Cancer Centres (CCC). Intervjupersoner menar till exempel att ackreditering som CCC medför bättre incitament att forska, och att CCC kan bidra med noder ut dit forskningen har svårt att nå idag.
Bristande tillgång till data försvårar för klinisk forskning
Tillgången till data har pekats ut som en svårighet för den kliniska forskningen, men det pågår insatser på området. Utredningen om sekundäranvändning av hälsodata (SOU 2023:76) konstaterar att det kan vara en betungande uppgift att få tillgång till de uppgifter som behövs för att bedriva klinisk forskning. Utredningen pekar bland annat på att utlämning av personuppgifter till klinisk forskning ofta innebär en omfattande och tidskrävande manuell sammanställning, och att personal som både forskar och erbjuder vård till samma individer måste begära ut uppgifter för forskningsändamål även när de i praktiken har tillgång till uppgifterna i egenskap av vårdgivare. Intervjupersoner i vår undersökning bekräftar den bilden. En ny lag om vidareanvändning av personuppgifter för klinisk forskning föreslås av utredningen för att lösa problemet och underlätta klinisk forskning (SOU 2023:76).
3.6.4 Förutsättningarna att följa upp cancervården har förbättrats
Insatser inom RCC-organisationen och genom myndigheter har gett möjlighet att följa upp aspekter som tidigare saknades, som patientupplevelser och väntetider. Däremot pekar inventeringar på att trots stora mängder data så brister möjligheterna att använda dem för analys på nationell nivå. De brister som pekats ut i uppföljningar har kopplats till svårigheter i genomförandet av cancerstrategin på olika områden, exempelvis väntetider, nya läkemedel, jämlikhet och screening. Bristande förutsättningar för uppföljning kopplas även till svårigheter att lära om vilka insatser som fungerar.
RCC och RCC i samverkans arbete med kvalitetsregister
RCC och RCC i samverkan har tidigt under perioden bland annat arbetat med att inkludera fler patientrapporterade mått i kvalitetsregistren (Socialdepartementet och SKL 2010, 2011, 2012). Under senare delen av perioden har RCC och RCC i samverkan bland annat arbetat med att inkludera uppföljning av rehabilitering och att öka samverkan mellan vårdprogram och kvalitetsregister (Socialdepartementet och SKL/SKR 2018, 2020, 2021, 2022). I överenskommelserna med regeringen har också ingått att löpande stötta regionerna genom kvalitetsregistren. I 2023 års överenskommelse får RCC i samverkan i uppdrag att genomföra insatser för att underlätta automatisk överföring av strukturerade data mellan olika system och register. Av uppföljningen framgår också att RCC tidigare genomfört insatser för att underlätta överföring av information genom individuell patientöversikt och Min vårdplan (Socialstyrelsen 2021d).
Positiv utveckling av kvalitetsregistren, men tillgänglighet och kompatibilitet är förbättringsområden
År 2013 rapporterade SKR att det fanns 16 kvalitetsregister inom cancer (SKR 2013d). Idag finns 35 nationella kvalitetsregister inom cancerområdet (RCC i samverkan 2021c). Varje register drivs och förvaltas av en sjukvårdsregion med stöd av RCC och innehåller individbaserade uppgifter om diagnoser och behandlingar, samt uppgifter om väntetider (Socialstyrelsen 2021b).
Kvalitetsregistren inom cancer har hög täckningsgrad (Socialstyrelsen 2021b) även om rapporteringen sker med fördröjning (RCC i samverkan 2021c). I Socialstyrelsens uppföljningar har RCC:s arbete med kvalitetsregistren lyfts fram som positivt för möjligheterna att följa upp cancervården, och även för registerforskningen (Socialstyrelsen 2016b, 2016a). I vår intervjustudie tar vissa upp kvalitetsregistrens potential att användas för forskning, exempelvis registerbaserade randomiserade studier. Samtidigt menar de att registren i dag inte är tillräckligt snabba på att inkludera den information som behövs för att de ska kunna användas för forskning.
Intervjupersoner uttrycker också att det finns behov av regiongemensamma system för användning av registerdata samt gemensamma strukturer för ledning och uppföljning av forskning.
Socialstyrelsen (2016b) beskrev 2016 också kvalitetsregistren som en viktig länk vid uppföljningen av de nationella vårdprogrammen. I den analys av möjligheterna att följa upp vårdprogrammen genom kvalitetsregister som RCC i samverkan genomförde 2021 bedöms att vårdprogrammens kvalitetsindikatorer i viss mån kan följas upp genom kvalitetsregistren. Arbetet med att samordna vårdprogram och kvalitetsregister pågår. RCC i samverkans undersökning tyder på att kvalitetsregistren ofta används för uppföljning och utveckling i verksamheterna, men att bristande koppling mellan indikatorerna och verksamhetens behov, samt brist på tid, upplevs försvåra användandet (RCC i samverkan 2021c). Flera verksamhetsföreträdare som intervjuats av RCC i samverkan efterfrågar fler indikatorer som är gemensamma och jämförbara för alla diagnoser. Idag är ett flertal indikatorer närliggande, men definierade på olika sätt i olika register.
Processer för redovisning och utlämning av data från kvalitetsregister var tidigt uppe som förbättringsområden (Socialstyrelsen 2013). Verksamhetsrepresentanter uttrycker i RCC i samverkans (2021c) uppföljning att de rapporter som regelbundet skickas till verksamheterna underlättar, medan det är tidskrävande att själva ta fram data.
Insatser för bättre uppföljning av patientupplevelser
Socialstyrelsen (2010) fick i uppdrag att genomföra en förstudie om patientrapporterade mått inom cancervården. Initiativ för att inkludera patientrapporterade mått i kvalitetsregistren ingick som en del i överenskommelserna mellan regeringen och SKR under början av perioden (Socialdepartementet och SKL 2010, 2011, 2012). Det ingår också i RCC:s uppdrag att löpande arbeta för att patientrapporterade uppgifter samlas in och används i arbetet med att utveckla cancervården (Socialdepartementet 2011). RCC arbetar också för ökad samordning mellan olika mätningar (RCC 2023f).
Som en del i införandet av standardiserade vårdförlopp tog SKR och RCC fram en patientenkät med PREM-mått som började användas 2016. Att använda PREM-enkäten var ett villkor för att regionerna skulle få ta del av de ekonomiska medlen i överenskommelsen (Socialdepartementet och SKL 2016). Både patienter som fått ett cancerbesked och de som avslutat SVF av någon annan orsak får enkäten. Enkäten avser att fånga upp patienternas erfarenhet av respektive SVF utifrån sju dimensioner (RCC i samverkan 2023l):
- helhetsintryck
- emotionellt stöd
- delaktighet och involvering
- respekt och bemötande
- kontinuitet och koordinering
- information och kunskap
- tillgänglighet.
Förutsättningarna att följa upp patientupplevelser har förbättrats
Patientupplevelser följs upp i betydligt högre grad idag än när cancerstrategin togs fram. När cancerstrategin togs fram 2009 saknades systematiska uppföljningar av patientupplevd kvalitet i cancervården, och i en tidig inventering fann SKR att få av de dåvarande kvalitetsregistren inkluderade patientupplevelser (SKL 2013d). År 2021 samlade över 85 procent av de nationella kvalitetsregistren in patientrapporterade mått, även om antalet mått varierar (Nationella kvalitetsregister 2021). PREM-enkäten tillämpas för samtliga standardiserade vårdförlopp. Införandet av SVF med tillhörande enkät för patientupplevelser bedöms ha medfört att patientupplevelser uppmärksammats mer i regionerna (Socialstyrelsen 2019b).
Flera insatser för att möjliggöra uppföljning av väntetider
Socialstyrelsen fick tidigt under perioden i uppdrag att kartlägga väntetider och ta fram ett förslag till modell för att mäta väntetider (Socialstyrelsen 2010). Att varje år redovisa väntetider inom cancervården ingick också i ett bredare uppdrag om nationell uppföljning av hälso- och sjukvårdens tillgänglighet (S2014/4157/FS) (Socialstyrelsen 2015b).
Från 2014 inleddes ett arbete med att definiera och mäta väntetider som en del i införandet av standardiserade vårdförlopp (Socialdepartementet och SKR 2015-2019).
Som en del i Socialstyrelsens uppdrag om att utveckla den statligt nationella samordningen och uppföljningen av cancervården ingår att ta fram ett koncept för insamling och analys av individuppgifter om väntetider, med en bred ansats för att även kunna inbegripa andra vårdområden än cancer (Socialstyrelsen 2021b; S2020/09801).
Förutsättningarna att följa upp väntetider har blivit bättre men är fortfarande otillräckliga
Socialstyrelsen (2010) konstaterade i början av perioden att det samlades in mängder med uppgifter om tidpunkter för olika moment i vårdkedjan i olika register, men att det saknades en gemensam uppfattning om vilka väntetider som ska mätas och hur. Eftersom det saknades individbaserade uppgifter om datum för att följa vårdförlopp i de nationella registren kunde man inte göra någon samlad redovisning av aktuella väntetider.
Införandet av SVF med nationella gemensamma mätningar av ledtider bedömer Socialstyrelsen har medfört bättre förutsättningar för uppföljning (Socialstyrelsen 2019b, 2021e). Samtidigt bedömer man (2021b) att uppgifter om väntetider behöver samlas in på ett förändrat sätt. Det saknas idag ett system för att samköra registerdata om väntetider eftersom väntetidsmåtten i olika kvalitetsregister skiljer sig åt, och väntetidsdatabasen saknar individdata (Socialstyrelsen 2021b). Uppföljningen av SVF är en egen modell med annan struktur än i övriga register, vilket inte möjliggör jämförelser väntetid mellan datakällor och patientgrupper (Socialstyrelsen 2021b). Att datan saknar id-uppgift gör att patienters väg genom vården inte kan analyseras, och försvårar kvalitetskontrollen (Socialstyrelsen 2023a). Datan har också brister i kvalitet som gör att den inte kan användas som önskat (Socialstyrelsen 2023a). Anvisningarna för kodningen tolkas olika och Socialstyrelsen (2021e) menar att RCC behöver förbättra och stärka sitt stödjande arbete med enhetlig kodning och registrering.
Viktigt men svårt att se till att rapportering ger värde för verksamheterna
Ett tema i rapporter om uppföljningsmöjligheter är att uppföljningen av cancervården behöver svara mot flera olika aktörers behov. Detta tycks försvåras av att automatöverföring inte fungerar idag, så att rapporteringen blir tidskrävande för verksamheterna.
En lärdom från Socialstyrelsens arbete med standardiserad dokumentation är att det är viktigt att ha kunskap om verksamheternas behov, samt att profession och verksamhet måste uppleva nytta. I det arbetet har det dock varit en svårighet att involvera verksamhetsexperter med kompetens inom informatik och strukturering (Socialstyrelsen 2020b). Uppföljning av arbetet med att samordna vårdprogram och kvalitetsregister visar också på liknande problem, där det upplevts svårt att inkludera verksamhetsföreträdare i processerna eftersom de har svårt att få tid till utvecklingsarbetet. Verksamhetsföreträdare uttrycker samtidigt att kvalitetsindikatorerna har påverkats mycket av forskningens behov och inte tillräckligt av verksamheternas behov. De bedömer att värdet som indikatorerna tillför verksamheterna inte motsvarar de stora resurser som går åt till inrapportering. Samtidigt betonar representanter för kvalitetsregistren i samma studie att det även behövs indikatorer i forskningssyfte som inte används av verksamheterna (RCC i samverkan 2021c). Något som återkommer i de flesta uppföljningar av uppföljningen är behovet av automatiserad överföring till register (Socialstyrelsen 2021b; RCC i samverkan 2021c).
3.6.5 Kompetensförsörjning är centralt men svårt att påverka genom cancerstrategin
Kompetensförsörjningen pekas ut i strategin som en nyckelfråga, och återkommer också som en nyckelfaktor för förutsättningarna att genomföra cancerstrategin. Kompetensförsörjning är både ett område för insatser inom ramen för cancerstrategin och central förutsättning för att genomföra andra delar av cancerstrategin.
RCC:s arbete med kompetensförsörjning
Varje RCC har som en del i sitt uppdrag tagit fram en kompetensförsörjningsplan inom sin sjukvårdsregion. RCC i samverkan har stöttat arbetet genom en nationell övergripande plan för kompetensförsörjning inom cancervården, samt en plan för kompetensförsörjning inom patologin (Socialstyrelsen 2016a). RCC-organisationen har också bland annat arbetat med utbildningar (Socialstyrelsen 2016a; RCC i samverkan 2021b).
Kompetensförsörjning är en svår fråga för RCC att påverka
Kompetensförsörjningen har enligt uppföljningen varit en av de svårare frågorna för RCC att arbeta med (Socialstyrelsen 2016a). Även i vår intervjustudie menar intervjupersoner att bristen på olika professioner och specialiteter inte är en fråga som RCC har mandat att påverka.
Svårigheterna kopplas bland annat till att RCC som separat kunskapsorganisation inom ett begränsat område inte har ansvar för kompetensförsörjning, och har begränsade möjligheter att påverka i frågan. Därför har RCC:s uppdrag att arbeta med kompetensförsörjning ibland ifrågasatts (Socialstyrelsen 2016a). Ansvaret för kompetensförsörjningen ligger hos regionen, även om RCC stödjer med underlag. Regionernas planering måste också utgå från ett helhetsperspektiv på vården, där cancerområdet bara är en del (Socialstyrelsen 2014, 2016a, 2021d).
Socialstyrelsen (2021d) finner att RCC:s insatser inom kompetensutveckling och utbildning uppfattas som positiva. Samtidigt är kompetensförsörjningsfrågan också bredare än vårdens linjeorganisation. Samverkan med aktörer utanför vården, som högskolor och universitet, har varit en utmaning (Socialstyrelsen 2017). Tidigt under perioden har representanter för RCC och sjukvårdsregioner också pekat på att kompetensförsörjningen är en nationellt gemensam utmaning, och efterfrågat mer nationella och statliga initiativ kring kompetensförsörjning (Socialstyrelsen 2014a).
Regeringen har nyligen tagit initiativ till ökat statligt stöd i kompetensförsörjningen genom att ge Socialstyrelsen i uppdrag att ta fram ett förslag till en nationell plan för att förbättra hälso- och sjukvårdens kompetensförsörjning. I uppdraget ingår att göra en nationell kartläggning av dels behovet av hälso- och sjukvårdspersonal nu och framöver, dels ansvarsfördelningen mellan vårdhuvudman och staten (Regeringen 2023c).
4 Standardiserade vårdförlopp
Standardiserade vårdförlopp (SVF) började införas 2015 i cancervården. Vårdförloppen är en insats inom ramen för cancerstrategin men har också särskilda mål som anges i överenskommelserna. I vårt uppdrag ingår att särskilt belysa de standardiserade vårdförloppen. I det här kapitlet sammanfattar vi kunskapen om vårdförloppens måluppfyllelse, hur införandet har gått och vilka hinder som finns. Kapitlet baseras främst på rapporter från olika aktörer, forskningsartiklar och vår intervjustudie. Det här är de viktigaste resultaten:
- Inklusionsmålet om att 70 procent av alla patienter som insjuknar i cancer inom de aktuella diagnoserna ska utredas i ett SVF har uppnåtts. Men det är långt kvar till att nå väntetidsmålet om att 80 procent ska inleda behandling inom De regionala skillnaderna i väntetider har minskat något, men kvarstår i stor utsträckning.
- När det gäller patientnöjdhet och jämlikhet är målen att det ska ske en förbättring. Patientnöjdheten har ökat kontinuerligt sedan 2018.
- Det finns otillräcklig kunskap om SVF:s effekter. Det gäller även faktorer vid sidan av målen, till exempel påverkan på medicinska resultat, prioriteringar och eventuell undanträngning av andra patientgrupper samt arbetsbelastningen i vården.
- Styrkor med SVF är att de bedöms ha bidragit till bättre vårdprocesser och förbättrad samverkan. Uppföljningen av ledtider inom SVF har möjliggjort jämförelser och beskrivs ha skapat incitament för förbättring av väntetider.
- Svagheter som pekats ut med SVF är framförallt att ledtiderna av vissa uppfattas som för ambitiösa och att ledtider som inte är medicinskt motiverade bedöms kunna bidra till felaktiga prioriteringar i vården.
- Genomslaget för SVF i regionerna är ojämnt. Framgångsfaktorer för genomslag är bland annat tydliga strukturer och mandat, god förankring i verksamheterna och långsiktighet i arbetet. Bristande engagemang från regionledningar, bristande lokalt ledarskap samt svårigheter med kompetensförsörjning har varit hinder.
4.1 Standardisering för att öka tillgänglighet, patientnöjdhet och jämlikhet
Standardiserade vårdförlopp (SVF) infördes i den svenska cancervården främst med en förebild i de standardiserade vårdförlopp som funnits i cancervården i Danmark sedan 2007. Sedan 2015 har SVF varit det huvudsakliga fokusområdet för överenskommelserna på cancerområdet mellan regeringen och SKR, både sett till mängden insatser som man kommit överens om och andelen av de ekonomiska medlen (Socialdepartementet och SKL/SKR 2015–2023). Mellan åren 2015 och 2023 har 32 SVF införts.
SVF innefattar en rad olika element, både innehållet i själva vårdförloppen och andra insatser inom ramen för införandet. Utöver själva vårdförloppen inkluderar initiativet bland annat SVF-koordinatorer, införande av obokade tider hos utredande enheter, en patientenkät, krav på återrapportering, och ökad användning av multidisciplinära konferenser (Socialdepartementet och SKL/SKR 2015–2023).
Från 2019 har standardiserade vårdförlopp införts på andra områden än cancer under beteckningen ”personcentrerade och sammanhållna vårdförlopp”. Dessa vårdförlopp bygger på SVF i cancervården men skiljer sig en del från vårdförloppen på cancerområdet. Bland annat omfattar de fler delar av vårdkedjan och andra typer av vårdkedjor (Vård- och omsorgsanalys 2021).
4.1.1 Vårdförloppens mål
Huvudsyftet med SVF är att uppnå ökad tillgänglighet, patientnöjdhet och jämlikhet. De kortare väntetiderna, samt bättre information till patienter och mer delaktighet, ska leda till nöjdare patienter. Vårdförloppen ska också leda till en mer sammanhållen vårdprocess som upplevs som välorganiserad, helhetsorienterad och professionell (Socialdepartementet och SKL 2015).
I överenskommelsen från 2015 nämns också att man ska nå bättre resultat i cancervården genom att RCC och regionernas linjeorganisationer knyts närmare samman. Satsningen ska utformas så att erfarenheterna kan användas även inom andra områden i vården.
Det finns två fastslagna målnivåer (Socialstyrelsen 2022a):
- Inklusionsmålet innebär att 70 procent av alla patienter som insjuknar i cancer inom de aktuella diagnoserna ska utredas i ett SVF.
- Ledtidsmålet innebär att 80 procent av patienterna inom SVF ska utredas inom de angivna ledtiderna.
4.1.2 Vårdförloppens innehåll
Vårdförloppen listar kriterier för ”välgrundad misstanke” för varje cancerform och beskriver vilka utredningar som ska göras i primär- och specialistvården för de patienter som uppfyller kriterierna.
Vårdförloppen ställer upp ledtider, det vill säga tiden mellan olika steg i vårdprocessen, som ska eftersträvas. Den övergripande ledtiden i vårdförloppen, som följs nationellt, är tiden från välgrundad misstanke till olika utredningsåtgärder samt till påbörjad behandling. För de olika delarna i vårdförloppet specificeras vilken information patienten ska få och vilket samråd som ska ske med patienten. I varje vårdförlopp listas också indikatorer för nationell uppföljning.
De svenska standardiserade vårdförloppen gäller enbart den tidigare delen av vård- processen, från misstanke till start av behandling, vilket skiljer dem från de danska vård- förloppen som även omfattar behandling och uppföljning. RCC i samverkan har undersökt möjligheten att införa ett vårdförlopp för tiden efter behandling, men landade i att det var mer ändamålsenligt att låta en särskild sektion i vårdprogrammen komplettera vårdförloppen.
Med ledtiderna i SVF fastslås vad som är skälig väntetid vid olika cancerformer. Ledtiderna sätts utifrån vad som krävs för ”optimal handläggning och medicinsk behandling”, utan hänsyn till nuvarande organisation och arbetssätt (Regionala cancercentrum i samverkan 2020c). Utgångspunkten är att minimera väntetiden för patienten oavsett om det finns evidens för medicinska effekter av väntetiden, och det varierar mellan olika vårdförlopp i vilken utsträckning ledtiden är medicinskt motiverad (Riksrevisionen 2023).
4.1.3 Framtagandeprocess och implementering
Vårdförloppen har tagits fram av nationella vårdprogramgruppen för respektive diagnos och bygger på de nationella vårdprogrammen. RCC i samverkan fastställer vårdförloppen och ansvarar för publicering. Varje region ansvarar för att anpassa förloppet till sin organisatoriska struktur, en ”lokal beskrivning” som individuella vårdplaner sedan skrivs utifrån. Varje region ansvarar också för att tillhandahålla den organisation och de resurser som krävs för att kunna genomföra vårdförloppen (Socialdepartementet och SKL 2015; Regionala cancercentrum i samverkan 2020c).
I överenskommelserna mellan regeringen och SKR har merparten av de ekonomiska medlen sedan 2015 varit vikta för införandet av standardiserade vårdförlopp.
4.2 Måluppfyllelse och effekter
Vi har sammanställt befintlig kunskap om vårdförloppens måluppfyllelse och effekter. Till att börja med sammanfattar vi kunskapen om effekter på de faktorer som vårdförloppen syftar till att påverka. Därefter sammanfattar vi kunskapen om deras påverkan på andra faktorer som lyfts fram som relevanta i utvärderingar och forskning.
4.2.1 Inklusionsmålet är uppnått, men inte ledtidsmålet
Inklusionsmålet om 70 procent har uppnåtts sett till både det nationella genomsnittet och för samtliga regioner. Under första halvan av 2022 var måluppfyllelsen 80 procent på nationell nivå (Socialstyrelsen 2022a). Väntetidsmålet om att 80 procent ska inleda behandling inom ledtiden har däremot inte uppnåtts under perioden (Riksrevisionen 2023). På nationell nivå var måluppfyllelsen 42 procent 2022 (Socialstyrelsen 2022a).
För patientnöjdhet och jämlikhet har inga mål specificerats utöver förbättring. När det gäller regionala skillnader så har de blivit något mindre, men kvarstår i stor utsträckning. Patientnöjdheten ligger däremot högt och har ökat kontinuerligt sedan 2018 (Riksrevisionen 2023).
4.2 2 Viss positiv påverkan på väntetider men över lag stor osäkerhet kring effekter
Över lag råder stor osäkerhet om de standardiserade vårdförloppens effekter. Det gäller inte bara de svenska SVF utan standardiserade vårdförlopp över lag (Vård- och omsorgsanalys 2021).
Även om det finns studier från olika länder som tyder på att standardiserade vårdförlopp kan föra med sig bland annat ökad följsamhet gentemot kliniska riktlinjer, förbättrad dokumentation och att personalen upplever ett förbättrat samarbete, saknas det studier som kan visa att vårdförlopp lett till förbättringar i medicinska resultat eller patientupplevelser (Vård- och omsorgsanalys 2021).
Ledde till kortare väntetider för vissa diagnoser, men långt kvar till målet
Det mest centrala målet med SVF har varit att korta väntetiderna i cancervården. SVF har också lett till kortare väntetider för vissa diagnoser. Riksrevisionen (2023) har analyserat utvecklingen i väntetid för prostatacancer, bröstcancer, tjock- och ändtarmscancer, urinblåsecancer och njurcancer jämfört med patientgrupper som ännu inte fått ett SVF. De kan belägga att SVF haft positiv effekt på väntetiderna för prostatacancer, urinblåsecancer och njurcancer, men inte däremot för bröstcancer eller tjocktarmscancer.
Förändringarna i väntetider under perioden bedöms sammantaget som positiva, men små och varierande (Socialstyrelsen 2019a och 2019b; Abuhasanein m.fl 2022; Riksrevisionen 2023; Fjällström m.fl 2023). Man befinner sig långt ifrån att nå väntetidsmålet om att 80 procent av SVF-patienterna ska inleda behandling inom ledtiden (Socialstyrelsen 2019a; Riksrevisionen 2023). Måluppfyllelsen är dock högre inom de mer allvarliga cancerformerna (Riksrevisionen 2023). Patientorganisationer lyfter i vår undersökning fram långa väntetider som en brist.
Även om väntetiderna i cancervården i Sverige, Danmark och Norge i olika grad har minskat över tid är det oklart utifrån forskningen i vilken utsträckning förändringen beror på just vårdförloppen. De flesta studier av SVF på cancerområdet i Norden finner att ledtiderna minskat under samma period som man infört standardiserade vårdförlopp (Sjövall m.fl 2020; Jensen m.fl 2015; Toustrup m.fl 2010; Sorensen m.fl 2014; Sandager m.fl 2019; Dyrop m.fl 2013; Fjällström m.dl 2023; Jakobsen och Jensen 2016; Laerum m.fl 2020; Lyhne m.fl 2013; Nilbert m.fl 2018; Lijkendijk och Thind 2010; Abuhasanein m.fl 2022; Villadsen m.fl 2019). Merparten av studierna visar dock bara att ledtider minskat över tid, och kan inte belägga någon koppling till införandet av SVF. Det framgår i flera studier att trenden varit minskande ledtider redan innan SVF infördes (Abuhasanein m.fl 2022; Lijkendijk och Thind 2010). Vissa studier av SVF på cancerområdet i Norden har följt utvecklingen över tid mer i detalj, och kan visa att en minskning i ledtider sammanföll tydligt med införandet av SVF i tid (Sorensen m.fl 2014; Toustrup m.fl 2010; Jensen m.fl 2015). Det kan stödja att förändringen beror på SVF. En av studierna visar dock att den största förbättringen i ledtider skedde redan i början av införandet, när effekten av SVF inte borde märkas så tydligt än. Det tolkar författarna som att det inte är SVF i sin helhet som lett till merparten av minskningen i ledtider (Jensen m.fl 2015).
Bättre förutsättningar för sammanhållen vård, men effekten på patientnöjdhet är okänd
Ökad patientnöjdhet är ett av målen med SVF. Patientupplevelsen med och utan SVF går dock inte att jämföra, eftersom mätningarna av patienters upplevelser infördes i samband med SVF. Vi vet därför inte om SVF påverkat patientnöjdheten. Över lag bedöms andelen nöjda cancerpatienter vara hög (RCC Stockholm Gotland 2019), men det var den även före införandet av SVF (Socialstyrelsen 2015) och nivåerna är över lag stabila över tid (Åkesson och Tufvesson Stiller 2019).
En dansk studie som jämfört patientrapporterad upplevelse av vården mellan cancerpatienter inom SVF och utanför SVF har funnit att patienterna inom SVF rapporterar en mer positiv upplevelse, och att en stor del av skillnaden kan kopplas till att ledtiderna är kortare för de patienterna (Sandager m.fl 2019). En svensk studie finner däremot att patientupplevelsen främst tycks variera utifrån tillgång till kontaktsjuksköterska (Sjövall m.fl 2020). Personal och chefer i verksamheterna uppfattar samtidigt att omhändertagandet av patienter blivit bättre i och med vårdförloppen, och Socialstyrelsen bedömer att förutsättningarna för sammanhållen vård har förbättrats (Socialstyrelsen 2019b; Riksrevisionen 2023).
Bättre förutsättningar för geografisk jämlikhet och för vissa utsatta patientgrupper
Ett mål med SVF är minskade skillnader mellan regioner. Skillnaderna i väntetider mellan regioner har blivit något mindre under perioden, men det är en relativt liten förändring (Socialstyrelsen 2019a; Riksrevisionen 2023). När det gäller patientupplevelser så är de uppmätta skillnaderna över huvud taget små (Åkesson och Tufvesson Stiller 2019). Däremot bedöms förutsättningarna för jämlikhet mellan regioner ha blivit bättre (Socialstyrelsen 2019a).
Olika aspekter av SVF kan ha olika påverkan på olika grupper cancerpatienter. En slutsats ur uppföljningar är att standardförloppet inte är lämpligt för exempelvis många äldre patienter med samsjuklighet och mer komplexa behov, och att dessa patienter behöver en mer sammanhållen och individanpassad vård än vad som anges i de standardiserade vårdförloppen. Socialstyrelsen (2019b) lyfter fram sammanhållna vårdkedjor för äldre personer med komplexa behov och samsjuklighet som ett område i behov av förbättring. Regionerna i Socialstyrelsens utvärdering uttrycker att vårdförloppen har varit särskilt gynnsamma för vissa patientgrupper som tidigare haft svårt att ta sig fram i vårdsystemet, bland annat personer med nedsatt autonomi, missbruk eller funktionsnedsättning. Definitionen av välgrundad misstanke bedömer regionerna har gjort att patienter med återfall och diffusa symtom, som ofta tidigare skickats runt i vårdsystemet, i högre grad tas om hand (Socialstyrelsen 2019b).
Positivt bidrag till utvecklingsarbete och vårdprocesser
Vårdförloppen bedöms ha varit positiva för verksamhetsutveckling och vårdprocesser (Socialstyrelsen 2019b; Riksrevisionen 2023). Socialstyrelsen (2019b), som följt införandeprocessen, drar sammantaget slutsatsen att förutsättningarna att arbeta med verksamhetsövergripande processer har förbättrats genom bland annat synliggörande av brister, gemensamt språk samt ökad förståelse för sina egna och andras roller bland verksamheterna. En journalgranskning visar också på att remitteringsprocesserna blivit smidigare efter införandet av SVF, med exempelvis färre tillbakaremitteringar. SVF uppfattas även ha medfört mer fokus på patientupplevelser och patienters ställning (Delilovic m.fl 2019, Socialstyrelsen 2019b).
Det förändringsarbete som aktualiserats av SVF har dock kommit olika långt i olika regioner och verksamheter, och Riksrevisionen (2023) finner att många verksamheter har kommit igång med förändringsarbetet först nyligen.
Ett centralt bidrag från SVF till förbättringsarbetet är att synliggöra flaskhalsar och möjliggöra jämförelser av väntetider och patientnöjdhet (Socialstyrelsen 2019b). Uppföljningen av SVF är central för det. Riksrevisionen (2023) konstaterar dock sammantaget att ”SVF-statistiken har brister i kvalitet, täckningsgrad och innehåll”. Registreringen har också medfört ökad administrativ belastning (Socialstyrelsen 2019b; Riksrevisionen 2023). Synliggörandet av bristande måluppfyllelse och flaskhalsar har inte heller alltid följts av utvecklingsarbete och åtgärder, vilket bland annat kopplas till bristande resurser (Delilovic m.fl. 2019; Riksrevisionen 2023).
4.2.3 Okänd effekt på medicinska resultat och vissa tecken på undanträngningseffekter
Förutom de områden som SVF syftar till att påverka har även andra konsekvenser lyfts fram i utvärderingar och studier. Det som framför allt varit i fokus är hur vårdförloppen påverkat prioriteringar och om de lett till undanträngning av patienter utanför vårdförloppen. Studier har också undersökt effekter på medicinska resultat. Även vårdförloppens påverkan på arbetsbelastning har undersökts.
Vissa tecken på undanträngning av andra patientgrupper
Risken för undanträngning, det vill säga att patientgrupper utanför SVF med lika eller större behov prioriteras ner till följd av vårdförloppen, har uppmärksammats mycket under perioden. Undanträngning är dock svårt att undersöka empiriskt och olika analyser har landat i olika slutsatser. Å ena sidan bedöms SVF ha synliggjort undanträngning snarare än att skapa den (Socialstyrelsen 2019b), vilket skulle kunna vara en sammantaget positiv påverkan. Å andra sidan har vissa patientgrupper med lika eller större behov fått längre väntetider i samband med införandet av SVF, vilket tyder på att vårdförloppen kan ha orsakat undanträngning (Delilovic, Andersson och Hasson 2020; Olsson 2020; Riksrevisionen 2023).
Intervjustudier med vårdpersonal har visat att SVF fungerar som ett snabbspår och att personal uppfattar att SVF-patienter prioriteras högre (Delilovic m.fl. 2019; Wells m.fl. 2020). Det framkommer i en studie att primärvårdsläkare ibland gör avvägningar kring risken att överbelasta sjukhusvården när de väljer om patienter ska remitteras enligt SVF (Wells m.fl. 2020). Socialstyrelsen har analyserat frågan utifrån regionernas rapportering, intervjuer och kvantitativa analyser på regionnivå. Man bedömer att medvetenheten om risken för undanträngning har varit stor under införandet och att de flesta förändringar som skett varit förbättringar eller korrekta prioriteringar. Sammantaget bedömer Socialstyrelsen att även om det finns tecken på att vårdförloppen medfört lägre prioritering av vissa andra patientgrupper, har de troligen inte lett till omfattande undanträngning. Man bedömer att prioriteringarna även har förbättrats till följd av införandet.
Två senare studier har undersökt utvecklingen av väntetider för lika eller högre prioriterade patientgrupper som har behov av samma resurser som patienterna inom SVF. De visar att väntetiderna hos vissa av de undersökta grupperna, som inte utreds för cancer, har ökat i samband med införandet av SVF. Det tyder på att undanträngning kan ha skett (Delilovic, Andersson och Hasson 2020; Riksrevisionen 2023). Däremot finner Riksrevisionen (2023) inte några tydliga tecken på att det skett undanträngning av cancerpatienter med större behov, av patienter med samma cancerdiagnos som inte utreds inom ett SVF, av cancerpatienter inom diagnoser utan SVF eller beroende på patienters bakgrund.
Oklar påverkan på medicinska resultat
Vårdförloppens syfte är inte att förbättra de medicinska resultaten, men det skulle potentiellt kunna vara en positiv bieffekt. De medicinska effekterna av vårdförloppen är dock inte kända. Forskare som undersökt vårdförloppens effekter på medicinska resultat har inte funnit tecken på att faktorer som tumörstadium och prognos är bättre för patienter som ingår i ett SVF (Andersson m.fl. 2021; Abuhasanein m.fl. 2022). Bland de studier av SVF på cancerområdet i Norden som tittat på utvecklingen i överlevnad finns flera som finner en förbättring över tid (Jensen och Maina 2015; Jensen, Torring och Vedsted 2017), men det kan handla om en utveckling utan samband med SVF.
Arbetsbelastning tycks främst ha påverkats negativt
Det finns beskrivningar av hur SVF kan medföra både minskad och ökad arbetsbelastning. Smidigare remittering beskrivs av vissa primärvårdsläkare minska belastningen (Wells m.fl. 2020), men personal uppger i flera studier att SVF ökat arbetsbelastningen genom ökad administration och fler undersökningar (Socialstyrelsen 2019b; Wells m.fl. 2020; Riksrevisionen 2023).
4.3 Vårdförloppen har fört med sig ett förbättrat samarbete, men ledtiderna ifrågasätts
De standardiserade vårdförloppen har flera komponenter. En del är standardisering, med begrepp som ”välgrundad misstanke om cancer” och gemensamma beskrivningar av vårdprocesser. En annan del är att de tar ett samlat grepp om flera delar av vårdkedjan, vilket kräver ett verksamhetsövergripande arbete med vårdprocesser. En tredje komponent är definitionen och uppföljningen av ledtider. Uppföljningar av vårdförloppen visar på att dessa olika komponenter haft olika för- och nackdelar.
Uppföljning har också pekat på faktorer som underlättat och försvårat i implementeringen av SVF. Flera av dessa, som ansvariga aktörer med mandat och strukturella faktorer, känns igen från andra insatser inom cancerstrategin.
4.3.1 Positivt med gemensamma definitioner och ökad tydlighet
Den relativt höga detaljnivån i SVF-initiativet har både uppfattats som en fördel och en nackdel. Den detaljerade styrningen har inneburit tydlighet, men samtidigt har den väckt viss kritik närmare verksamheterna (Socialstyrelsen 2019b).
I analyser av vad SVF bidragit med återkommer tydlighet och synliggörande. Det handlar bland annat om att ha en standard med gemensamma begrepp, en verksamhetsövergripande beskrivning av patientens vårdprocess och statistik över väntetider och patientupplevelser (Socialstyrelsen 2019b; Riksrevisionen 2023). En viktig del i införandet har varit att skapa ett gemensamt språk och en nationell samsyn. Kommunikation, till exempel att återkommande presentera en gemensam definition av undanträngning, har varit en del i det (Socialstyrelsen 2019b). När dessa delar varit otydliga har det uppfattats som ett problem. Utvärderingar pekar till exempel på olika tolkningar av kriterierna för ”välgrundad misstanke” (Socialstyrelsen 2019b) och att olika tolkningar av hur rapporteringen ska ske lett till brister i datakvaliteten (Riksrevisionen 2023).
Begreppet ”välgrundad misstanke om cancer”, med tydliga gemensamma kriterier, lyfts fram som ett viktigt bidrag, bland annat för att skapa bättre samarbete mellan primärvård och sjukhusvård (Socialstyrelsen 2019b). Även remissmallarna bedöms ha bidragit till smidigare remitteringsprocesser (Socialstyrelsen 2019b). Inklusionskriterierna har samtidigt kritiserats för att i vissa fall vara alltför breda, vilket kan leda till ineffektiv utredning och undanträngning (Socialstyrelsen 2019b; Riksrevisionen 2023). Andelen SVF-patienter i Sverige som visar sig ha cancer är högre än i Danmark men lägre än i Norge, och det är inte känt vad skillnaden mellan länderna beror på (Cancerfonden 2020a). Nackdelen med tydliga och standardiserade beskrivningar av vårdprocessen är att det blir en linjär beskrivning av vårdprocesser som i verkligheten ofta är komplexa. Det är särskilt viktigt för de många multisjuka äldre cancerpatienterna (Socialstyrelsen 2019b).
4.3.2 Svårt men viktigt arbete med vårdprocesser
En viktig del i SVF är att de knyter ihop flera delar av vårdkedjan i ett sammanhållet vårdflöde. Att arbeta enligt vårdförloppen kräver ett starkt samarbete mellan verksamheter för att skapa sammanhållna och välfungerande vårdprocesser, och den egna verksamhetens resultat är beroende av vad andra verksamheter gör. Att de standardiserade vårdförloppen och uppföljningen av dem är verksamhetsövergripande har varit utmanande att hantera (Delilovic m.fl. 2019; Socialstyrelsen 2019b). Dominerande kulturer, fragmentisering och samverkansproblem över lag inom vården har enligt Socialstyrelsens (2019b) och Riksrevisionens (2023) analys försvårat införandet av SVF, och det är svårigheter man behöver arbeta med även efter införandet av SVF. Men den verksamhetsövergripande karaktären framstår som en central del i SVF, eftersom det drivit på förbättringar i samarbete och vårdprocesser (Delilovic m.fl. 2019; Socialstyrelsen 2019b, Riksrevisionen 2023).
Vissa komponenter i SVF har pekats ut som särskilt viktiga för att underlätta arbetet med vårdprocesser. En framgångsfaktor som framhålls i flera uppföljningar är vårdförloppskoordinatorerna. De har bidragit till smidigare processer, samordning och bättre registrering (Delilovic 2019; Socialstyrelsen 2019a; Riksrevisionen 2023). Även förbokade tider hos utredande enheter har varit en viktig del (Socialstyrelsen 2018).
4.3.3 Ledtiderna är en central men kritiserad del i SVF
Ledtiderna och uppföljningen av dem är en central del i SVF, som möjliggör jämförelse och ger incitament för förbättring av väntetider (Socialstyrelsen 2019b; Riksrevisionen 2023). Samtidigt har de också beskrivits som alltför ambitiösa och omöjliga att nå (Socialstyrelsen 2019b; Riksrevisionen 2023) och ibland även för korta utifrån ett patientperspektiv (Socialstyrelsen 2023).
Vårdförloppens fokus på ledtider från upptäckt till behandlingsstart kommenteras också av flera i vår intervjustudie. De menar att det är positivt att följa upp ledtider men att det finns också begränsningar i den nuvarande utformningen. Vissa menar att vårdförloppen har ett snävt fokus på ledtider och inte tar hänsyn till andra kvalitetsdimensioner som kan vara viktiga. Andra menar att det skulle behövas tydligare incitament för att klara målnivåerna och påföljder när man inte når målen.
Medicinsk förankring av vårdförloppen återkommer som en viktig fråga för deras legitimitet. I Socialstyrelsens intervjuer beskriver nyckelaktörer att den medicinska förankringen varit en framgångsfaktor, och pekar bland annat på att vårdförloppen är kopplade till de nationella vårdprogrammen och att professionen fastställt ledtiderna (Socialstyrelsen 2019b). Samtidigt finner Riksrevisionen (2023) att ledtider som inte bygger på evidens har lett till motstånd inom professionen. Riksrevisionen bedömer också att det tvådelat formulerade ledtidsmålet och sättet att rapportera måluppfyllelsen försvårar analys och kommunikation, och enligt verksamhetsföreträdare kan det även minska motivationen bland personal.
Ledtiderna och ledtidsmålet är inte alltid satta utifrån vad som är medicinskt motiverat, men vården ska samtidigt prioritera utifrån medicinska behov. Flera i vår intervjustudie menar att bristande medicinskt stöd för ledtider kan bidra till felaktiga prioriteringar i vården, en risk som även Socialstyrelsen (2023a) har pekat på. Riksrevisionen (2023) menar att prioriteringar försvåras av att det inte finns någon struktur för horisontella prioriteringar i framtagandet av vårdförloppen, utan att fokus och expertis i arbetsgrupperna är begränsat till det specifika diagnosområdet.
4.3.4 Förankring och processledare har underlättat införandet
Sammantaget bedöms det finnas ett utbrett stöd för SVF i vården, inklusive primärvården (Socialstyrelsen 2019b; Delilovic 2019; Backman, Johansson och Hellgren 2021; Riksrevisionen 2023). En viktig framgångsfaktor för förankringen är att professionen är aktiv i framtagandet (Riksrevisionen 2023) och att SVF är ett nationellt initiativ (Delilovic m.fl. 2019). Det fanns dessutom en gemensam bild i verksamheterna före införandet av att det behövdes en förändring (Delilovic m.fl. 2019; Socialstyrelsen 2019b).
En ytterligare framgångsfaktor är att någon är tydligt ansvarig för att driva arbetet med SVF, både mer övergripande och i verksamheterna. Riksrevisionen (2023) menar att lokala processledare med tydligt mandat och stöd från verksamhetsledningar varit viktiga för ett framgångsrikt införande. RCC har också varit en central aktör och fungerat som motor i arbetet (Riksrevisionen 2023).
RCC:s tidigare arbete och stödet från nationell nivå har underlättat
En underlättande faktor för implementeringen av SVF var att det utgjorde en fortsättning på RCC:s redan påbörjade arbete med verksamhetsövergripande vårdprocesser, och att RCC fanns som en etablerad struktur för kunskapsstyrning som kunde föra ut vårdförloppen (Socialstyrelsen 2019b).
Sammanhållna insatser med kontinuitet och enhetlig kommunikation har underlättat lärande i införandeprocessen (Socialstyrelsen 2019b). Stödet från nationell nivå, inklusive det ekonomiska stödet, lyfts fram som viktigt, men bättre framförhållning i stödet hade varit önskvärt (Socialstyrelsen 2019b; Åkesson och Tufvesson Stiller 2019; Riksrevisionen 2023). Arenor för dialog och erfarenhetsutbyte på olika nivåer har bidragit till att skapa engagemang och lärande (Socialstyrelsen 2019b). Införandeprocessen uppfattas dock i vissa delar ha gått för snabbt (Socialstyrelsen 2019b; Åkesson och Tufvesson Stiller 2019).
Särskilda insatser nödvändiga för att nå primärvården
Införandet i primärvården har varit ett område med särskilda utmaningar. Det har varit svårt att inkludera primärvården i införandeprocessen och särskilda insatser har behövts för att nå ut i primärvården (Socialstyrelsen 2019b). I våra intervjuer framkommer att det behövs kontinuerliga insatser för att informera om SVF i primärvården även efter införandet.
En intervjustudie med personal som arbetar med SVF visar att de uppfattar att primärvårdens kunskap om SVF har brister (Delilovic m.fl. 2019). En enkätundersökning bland läkare visar att läkare både inom primärvården och sjukhusvården upplever att de saknar tillräcklig kunskap om SVF, och att de svarande läkarna överlag också har låg kunskap om SVF. Däremot är kunskapen om SVF större bland allmänläkarna än bland övriga läkare i studien (Backman, Johansson och Hellgren 2021).
4.3.5 Brister i ledarskap och kompetensförsörjning har varit utmaningar för implementeringen
En faktor som lyfts fram kopplat till skillnaderna mellan regioner är vikten av tydliga strukturer där det finns roller med ansvar för SVF och mandat (Socialstyrelsen 2019b; Riksrevisionen 2023). RCC:s svaga mandat pekas i Riksrevisionens (2023) uppföljning ut som ett hinder för implementeringen av vårdförloppen. Eftersom RCC inte själva kan styra blir regionledningens förhållningssätt centralt för de standardiserade vårdförloppens genomslag. Det har därför varit viktigt med samsyn mellan RCC och den politiska ledningen i regionerna. Engagemang från regionledning och politisk nivå uppfattas ha underlättat implementeringen i vissa regioner medan bristande intresse beskrivs som ett hinder i andra (Riksrevisionen 2023). Att inte ha processledare med ansvar för att driva arbetet i de olika SVF har i vissa regioner försvårat samverkan och innebär att ingen har ansvar för hela vårdförloppet. Även de lokala processledarna har dock ett svagt formellt mandat och är beroende av att ha verksamhetsledningen med sig (Riksrevisionen 2023). Verksamhetsföreträdare som intervjuats av Socialstyrelsen (2019a) har även pekat ut kompetens och ledarskap hos chefer som den viktigaste faktorn för hur man lyckats med väntetidsarbetet.
En annan central faktor som identifierats är it-stöd (Socialstyrelsen 2019b). Ett hinder i införandet var att det saknades en fungerande it-lösning, vilket bidrog till den administrativa belastningen (Delilovic m.fl. 2019; Riksrevisionen 2023). Införandet av SVF-INCA-plattformen för registrering beskrivs ha underlättat (Delilovic m.fl. 2019).
Resurser, i synnerhet bemanning, återkommer i uppföljningsrapporter som en central förutsättning för att kunna införa och nå målen med SVF (Socialstyrelsen 2019a, 2019b).
En stabil bemanning bedöms ha underlättat, medan bristande personkontinuitet och kompetensbrist i verksamheterna bedöms ha varit ett viktigt skäl till att man inte nått målen (Socialstyrelsen 2019a, 2019b). Resursbristen och den höga personalomsättningen i primärvården lyfts särskilt fram som en försvårande faktor (Socialstyrelsen 2019b; Riksrevisionen 2023). Ansträngda resurser inom de utredande verksamheterna kopplas särskilt till risken för undanträngning, vilket kan förvärras av att den medicinska utvecklingen leder till ett ökat behov av avancerade undersökningar (Riksrevisionen 2023).
5 Barncancer
Barncancer tycks inte från början ha ingått i cancerstrategin, sett till de insatser som genomfördes, utan tillkom efter regeringens avsiktsförklaring om cancervården 2018. I betänkandet En nationell cancerstrategi för framtiden beskrevs barncancerområdet som välfungerande, men det betonades också att behovet av uppföljning och stöd vid sena komplikationer förväntades öka kraftigt i takt med att allt fler barn och unga, som överlevt efter en cancerdiagnos, når vuxen ålder. I vårt uppdrag ingår att ge en lägesbild över styrkor och utvecklingsbehov inom barncancervården. I det här kapitlet gör vi en analys av barncancerområdet, baserat på främst rapporter från andra aktörer och vår intervjustudie. Det här är de viktigaste resultaten:
- Resultaten på barncancerområdet utifrån cancerstrategins mål liknar i viss mån cancervården för vuxna. Som starka områden framkommer även i barncancervården kvaliteten i omhändertagandet, de medicinska resultaten och den geografiska jämlikheten. Men det framkommer också att stödet till en förbättrad livskvalitet varierar, till exempel rehabilitering.
- Sedan barncancer blev en tydligare del av cancerstrategin har flera insatser genomförts, bland annat för att stärka den nationella samordningen inom RCC, förbättra omhändertagandet av patienter, genom till exempel kontaktsjuksköterskor och förbättrad samordning mellan barn- och vuxenvården, stärkt långtidsuppföljning, samt stärkt palliativ vård för barn.
- Styrkor i barncancervården är starka strukturer för vården samt det nationella samarbetet inom ramen för RCC och i professionsnätverk. Området ligger också långt fram vad gäller tillämpningen av precisionsmedicin.
- Flera svårigheter inom barncancerområdet handlar om särskilda utmaningar kopplade till att det är ett så litet område. Särskilda svårigheter är kompetensförsörjning och finansiering, samt tillgång till läkemedel och kliniska studier.
- Ett särskilt område som aktualiseras för barn och unga vuxna är övergången mellan barncancervården och vuxencancervården. Det finns särskilda mottagningar som erbjuder stöd men unga vuxna cancerpatienter upplever ändå ensamhet, bristande informationsöverföring mellan vårdaktörer, brist på psykosocialt stöd och annat stöd kopplat till övergången till vuxenlivet, till exempel vad gäller fertilitet, studier och etablering på arbetsmarknaden.
5.1 Barncancer blev sent en del i arbetet med cancerstrategin
Under de första tio åren av cancerstrategin vidtogs vissa insatser, exempelvis den kompetens- försörjningsplan för barncancerområdet som togs fram 2016 (Socialdepartementet och SKL 2016). Sedan 2016 finns också ett nationellt vårdprogram för långtidsuppföljning efter barncancer (RCC i samverkan 2016a). Arbetet initierades av arbetsgruppen för långtidsuppföljning (SALUB) som kom med sina första rekommendationer redan 2007, och arbetet med att utveckla vårdprogrammet har sedan gjorts tillsammans med RCC i samverkan och SKR.
I övrigt har insatser för barncancer blivit en del i arbetet med cancerstrategin efter regeringens avsiktsförklaring om cancervården (Regeringen 2018). En stärkt cancervård för barn och unga anges också som ett av de områden som RCC:s arbete i framtiden bör vara inriktat på (Regeringen 2018; se till exempel RCC i samverkan 2023d).
Insatserna har bland annat haft fokus på kunskaps- och erfarenhetsutbyte om långtidsuppföljning, samt på införandet av ett vårdprogram för palliativ vård för barn. Flera av de insatser som skett inom barncancerområdet inom ramen för överenskommelserna mellan regeringen och SKR har syftat till att förbättra omhändertagandet av patienter, genom till exempel kontaktsjuksköterskor och förbättrad samordning mellan barn- och vuxenvården.
En nationell samordningsgrupp inom RCC i samverkan har haft i uppdrag att arbeta för att stärka och öka kvaliteten inom barncancer utifrån en handlingsplan från 2020, och respektive RCC har haft i uppdrag att ge stöd till regionerna i samma frågor.
5.1.1 Vårdprogrammet för långtidsuppföljning efter barncancer
Syftet med vårdprogrammet för långtidsuppföljning efter barncancer är att få en nationell samsyn inom alla delar av vården och en regional samverkan för långtidsuppföljning efter barncancer. Målet är också att öka kompetensen och medvetenheten om patientgruppen. Programmet inkluderar alla som har fått cancerbehandling som barn och fram till 18 års ålder. Det omfattar långtidsuppföljning både för de som nu är barn och ungdomar och de som är vuxna.
För att underlätta övergången från barn- till vuxenvården pågår ett arbete med att bygga upp en struktur med så kallade nyckelmottagningar på alla barncancercentrum. En nyckelmottagning består i att de läkare och sjuksköterskor som patienten mött under behandlingen regelbundet träffar patienten och följer upp patientens behov efter behandlingen. Målet är att alla tonåringar som avslutat sin cancerbehandling ska erbjudas två till tre nyckelbesök på en nyckelmottagning vid ett barncancercentrum.
Vid det avslutande besöket får patienten en sammanfattning av behandlingen, eventuella komplikationer samt potentiella risker för sena komplikationer (så kallat ”survivorship passport”). Vid besöket får också patienten en remiss till en uppföljningsmottagning för vuxna efter barncancer där de planeras att gå med viss regelbundenhet. Uppföljnings- mottagningar finns idag i alla sex sjukvårdsregioner: Umeå, Uppsala, Stockholm, Linköping, Göteborg och Lund. Som stöd för uppföljningsmottagningarna finns det nationella vårdprogrammet för långtidsuppföljning efter barncancer. Mottagningarna samarbetar också i det nationella nätverket UFM Sverige, med syfte att organisera och strukturera långtidsuppföljning efter behandling för barncancer. Nätverket håller för närvarande på att permanentas inom ramen för RCC i samverkan (Petersen, Óskarsson, Jarfelt och Hjorth 2023).
5.2 Styrkor och svagheter i barncancervården idag
De styrkor och svagheter i cancervården för barn och unga som lyfts fram i uppföljningsrapporter och i våra intervjuer är delvis gemensamma med cancervården för vuxna. Även patienter inom barncancer har haft en positiv utveckling inom bland annat överlevnad, medan tillgången till rehabilitering och god palliativ vård är svagare områden. Styrkor och svagheter inom barncancer skiljer sig dock delvis från vuxenvården. För barn och unga finns exempelvis inte problem med långa väntetider till behandling, men det finns istället särskilda svårigheter med bland annat tillgång till nya läkemedel.
5.2.1 Positiv utveckling i överlevnad och gott omhändertagande under behandling
Den analys som bland annat nationella arbetsgruppen för barncancer gjort visar på att barncancerområdet har goda medicinska resultat. En positiv utveckling syns i ökande överlevnad (RCC i samverkan 2020d). Barncancerområdet ligger också enligt våra intervjupersoner långt fram när det gäller precisionsmedicin i och med att gensekvensering börjar bli klinisk rutin, vilket få förväntas stor betydelse för behandling och uppföljning. Ytterligare en styrka som lyfts fram i våra intervjuer är den regionala jämlikheten när det gäller behandling, som beskrivs som mycket god inom barncancer.
Våra intervjupersoner beskriver att omhändertagandet inom barncancer är en styrka, med hög personkontinuitet. Det har även skett en positiv utveckling av till exempel tillgång till kontaktsjuksköterska (RCC i samverkan 2022d), vilket också lyfts fram i våra intervjuer.
5.2.2 Vårdprogrammet för långtidsuppföljning är till nytta
Nationella arbetsgruppen för barncancer gjorde under 2019 en utvärdering av det nationella vårdprogrammet för långtidsuppföljning för att utvärdera de första årens arbete med vårdprogrammet (RCC i samverkan 2022d). Sammanfattningsvis visade resultaten från intervjuer med vårdpersonal och patienter bland annat att vårdprogrammet används och är till nytta framför allt när det gäller att få ökad kunskap samt kontrollera vad som rekommenderas för utredning, behandling och uppföljning.
I våra intervjuer lyfts nyckelmottagningarna fram som en positiv utveckling, där man har hög kontinuitet och erfarenhet bland personal. Det finns nyckelmottagningar i alla sex sjukvårdsregioner, även om det skiljer hur långt de olika mottagningarna kommit i etableringsgrad (RCC i samverkan 2022c).
Alla barncancercentrum uppger i en enkät att de har förutsättningar att genomföra uppföljning av patienter enligt vårdprogrammet för långtidsuppföljning (RCC 2021a). Uppföljningsmottagningarna för vuxna efter barncancer har dock olika förutsättningar eftersom det finns regionala skillnader i deras resurser (RCC 2019b).
5.2.3 Tillgången till läkemedel, psykosocialt stöd, hemsjukvård och palliativ vård brister
En svårighet är att nya läkemedel inte görs tillgängliga för barn i samma utsträckning som för vuxna, eftersom intresset från läkemedelsföretag är lägre (RCC 2019b). Våra intervjupersoner beskriver att eftersom barn inte ingår i läkemedelsutvecklingen på samma sätt som vuxna blir läkemedelsbehandlingen inte evidensbaserad i lika hög grad utan måste baseras främst på tidigare erfarenhet. Den nationella arbetsgruppen har också pekat på en begränsad och ojämlik tillgång till hemsjukvård och palliativ för barn (RCC 2019b).
Det psykosociala stödet till patienter och familjer under och efter behandling upplevs också som otillräckligt, och arbete pågår med att ta fram en gemensam basrekommendation för psykosocialt stöd (SKL 2016, RCC i samverkan 2019, RCC i samverkan 2022b). Aktörer som vi intervjuat pekar också på att syskon inte inkluderas i begreppet närstående i dag.
5.2.4 Tillgången till rehabilitering och övergången till vuxenvården är svagheter i långtidsuppföljningen
Utvärderingen av det nationella vårdprogrammet för långtidsuppföljning visar att det som saknades i vårdprogrammet var omvårdnadsaspekter och kognitiva besvär (RCC i samverkan 2022d). Det framfördes också att programmet i första hand vänder sig till de som arbetar med långtidsuppföljning varje dag och att det på mindre sjukhus kan vara svårt att se vad som är viktigt.
Våra intervjupersoner beskriver att stödet till en förbättrad livskvalitet – eftervården, det psykosociala omhändertagandet, rehabiliteringen och uppföljningen – varierar lika mycket mellan olika regioner som i vuxencancervården. Nyckelmottagningen kan ta initiativ till stöd, men stödet måste ges av en rad andra aktörer. Det lyfts fram att det i dag inte finns något som heter ”cancerrehabilitering för barn”, och att det saknas struktur och samordning i form av exempelvis multidisciplinära team för att tillgodose patienternas behov av rehabilitering.
En svaghet i långtidsuppföljningen är brister i övergången till vuxenvården för fortsatt uppföljning (RCC i samverkan 2019). Unga vuxna är en grupp med särskilda utmaningar som ofta faller mellan stolarna (RCC i samverkan 2019b; Socialstyrelsen 2022b). Våra intervjupersoner beskriver att vanliga problem för unga vuxna cancerpatienter är bristande informationsöverföring mellan vårdaktörer och upplevelser av ensamhet, brist på psykosocialt stöd och annat stöd kopplat till övergången till vuxenlivet, till exempel vad gäller fertilitet, studier och etablering på arbetsmarknaden.
5.2.5 Kompetensförsörjningen är ett problem som riskerar att förvärras
Kompetensförsörjningen har pekats ut som en särskilt central utmaning. Det råder brist på framförallt specialistsjuksköterskor i dag, och under kommande år beräknas det bli brist på barnonkologer. Tillgången till många andra yrkesgrupper som deltar i barncancervården beskrivs också som otillräcklig. Kompetensförsörjningssituationen har inte förbättrats sedan den första kartläggningen gjordes 2016 (SKR 2016a, RCC 2022b).
5.3 Lärdomar och utvecklingsbehov
Flera av de lärdomar och utvecklingsbehov som framkommer i uppföljningen av barncancerområdet anknyter till att det är ett jämförelsevis litet område, som i hög grad varit separat från cancerområdet i övrigt. I våra intervjuer beskrivs att barncancervården byggt upp strukturer och samverkan oberoende av de strukturer som skapats inom ramen för cancerstrategin. Dessa strukturer bedöms ge goda förutsättningar. Samtidigt återkommer i uppföljning och i våra intervjuer att det finns utvecklingsbehov. Bland annat lyfts det fram som problematiskt att barncancerområdet i så hög grad förlitar sig på stöd från Barncancerfonden när det gäller kompetensutveckling, stöd till närstående och genomförande av uppföljning.
5.3.1 Nationellt samarbete är centralt
Ett centralt tema i uppföljning av barncancervården är vikten av samarbete nationellt. Det gemensamma nationella arbete som idag bedrivs inom ramen för RCC bedöms bidra positivt och Socialstyrelsen (2021e) bedömer att det är positivt att den nationella handlingsplanen för barncancer är gemensam för alla regioner. Även de nationella nätverken för professionen bedöms som mycket värdefulla för kunskapsutvecklingen inom barncancer (RCC i samverkan 2022b). En utmaning i arbetet med att arbeta tillsammans nationellt med kompetensförsörjningsfrågan har dock varit att skillnaderna mellan regionerna i vissa fall gör det svårt att jämföra data (RCC i samverkan 2022b).
5.3.2 Att vara ett litet område medför särskilda utmaningar
Flera svårigheter inom barncancerområdet handlar om särskilda utmaningar kopplade till att det är ett så litet område. Den nationella arbetsgruppen beskriver att barncancerområdet i och med sin storlek blir mer känsligt för de generella trenderna inom vården, till exempel problem med kompetensförsörjning och att kompetenser blir alltmer nischade (RCC i samverkan 2022b).
Den nationella arbetsgruppen lyfter också fram särskilda dilemman för barncancer- området kopplade till tillgång till kliniska studier med nya läkemedel. Å ena sidan, beskriver man, finns behov av centralisering av studier, eftersom det är svårt att upprätthålla tillräcklig kompetens på mindre enheter. Å andra sidan är det både praktiskt och etiskt problematiskt att skicka barncancerpatienter långt hemifrån för att delta. Att betala för vården på annan ort är också en stor ekonomisk påfrestning för hemförvaltningen (RCC i samverkan 2019).
5.3.3 Medicinska framsteg bedöms öka behovet av gemensam finansiering
Den medicinska utvecklingen för inte bara med sig ökad överlevnad utan även utmaningar med resurser. Den ökade behandlingsintensiteten och den ökade efterfrågan på genetisk analys (som finansierats genom forskningsmedel men kommer att övergå till ordinarie budget) medför ökade behov av ekonomiska och personella resurser. Den nationella arbetsgruppen föreslår mer gemensamt arbete för att möta utmaningarna (RCC i samverkan 2019). En svaghet de pekar ut i dagens struktur är till exempel att varje barncancercentrum finansierar sina egna läkemedel. Eftersom det handlar om få patienter med en sporadisk användning av nya läkemedel, blir det svårt för förvaltningarna att rusta sig inför de stora kostnader som ett nytt läkemedel kan innebära. Arbetsgruppen föreslår därför att man övergår till gemensam finansiering på nationell nivå, och utökar den nationella samordningen inom de multidisciplinära nätverken.
5.3.4 Arbetsförhållanden, attraktivitet och kompetensutveckling är viktigt för kompetensförsörjningen
När det gäller kompetensförsörjningen är en försvårande faktor för barncancervården att de fåtaliga erfarna barnonkologerna också håller i de flesta ST-utbildningar och utbildningar för andra läkare, vilket medför stor arbetsbelastning (RCC i samverkan 2022b).
SKR (2016) har tidigare lyft fram bristande arbetsförhållanden och attraktivitet för sjuksköterskor som viktiga förklaringar bakom problemen med kompetensförsörjning. En styrka för barncancervården när det gäller kompetensförsörjning är däremot att man kan erbjuda kompetensutveckling (RCC i samverkan 2022b).
5.3.5 Viktiga aktiviteter på barncancerområdet finansieras av Barncancerfonden
En faktor som problematiserades i kartläggningen 2016 och återkommer i senare rapporter och i våra intervjuer är att Barncancerfonden finansierar en stor del av kompetens- utvecklingen inom barncancer (RCC i samverkan 2022c). I 2016 års kartläggning föreslogs att utbildningen till barnonkologisjuksköterska (som idag är professionsdriven och finansieras av Barncancerfonden) skulle formaliseras, vilket ännu inte skett (RCC i samverkan 2022b). Barncancerfonden finansierar också rapporteringen till kvalitetsregister (RCC i samverkan 2019).
6 Cancerstrategin i förhållande till omvärldsfaktorer
Under perioden efter att den ursprungliga nationella cancerstrategin togs fram har det skett flera förändringar som har betydelse för cancerområdet.
Den snabba utveckling inom diagnostik och behandling som beskrevs i betänkandet 2009 har fortsatt. Utvecklingen mot centralisering av cancervård till cancercentrum med både vård och forskning har skett i form av framväxten av Comprehensive Cancer Centres (CCC). Samtidigt berörs cancervården också av omställningen av hälso- och sjukvårdssystemet mot en mer nära vård, med en starkare primärvård i centrum. Slutligen har en rad initiativ skett på EU-nivå, något som inte skett inom hälso- och sjukvårdsområdet tidigare.
En reviderad cancerstrategi behöver förhålla sig till dessa omvärldsfaktorer.
6.1 Initiativ på EU-nivå
En utveckling som skett sedan den svenska cancerstrategin togs fram 2009 är att det tillkommit initiativ på EU-nivå. På EU-nivå finns sedan 2021 två större initiativ som berör cancerområdet: EU:s cancerplan (EU:s Beating Cancer Plan) och Cancermissionen (Mission on Cancer). Båda initiativen ligger under EU-kommissionen. Dessutom berörs cancerområdet av en rad andra aktiviteter på EU-nivå.
Det är nytt att EU så tydligt ger sig in på ett område inom hälso- och sjukvård. EU saknar mandat (s.k. kompetens) inom hälso- och sjukvårdsområdet, så de flesta av initiativen är inte tvingande. Däremot bedömer våra intervjupersoner och andra informanter att cancerområdet i Sverige kommer att påverkas av det som sker på EU-nivå. De menar att det finns flera skäl att ta en aktiv roll inom EU-initiativen. Till exempel är det möjligt att ta del av stöd i form av ekonomiska medel och kunskapsutbyten samt till samverkan om frågor som rör vårdkedjans olika delar, från prevention och screening till precisionsdiagnostik och palliativ vård. Initiativ finns inom områden som forskning, innovation, nya tekniker och ökade möjligheter att dela hälsodata.
6.1.1 EU:s cancerplan (2021)
EU:s cancerplan (Europeiska kommissionen 2021a) är ett insatsområde inom EU:s hälsoprogram, Eu4Health, som ska komplettera medlemsstaternas politik för att förbättra människors hälsa i hela unionen (Europeiska kommissionen u.å.c).
Mål för EU:s hälsoprogram EU4Health:
- förbättra och främja hälsan i unionen för att minska bördan av smittsamma och icke- smittsamma sjukdomar genom att stödja hälsofrämjande och sjukdomsförebyggande åtgärder, minska ojämlikhet i hälsa, främja en hälsosam livsstil och främja tillgång till hälso- och sjukvård.
- skydda människor i unionen mot allvarliga gränsöverskridande hot mot människors hälsa, stärka hälso- och sjukvårdssystemens förmåga att reagera på dessa hot och förbättra samordningen mellan medlemsstaterna när det gäller att hantera allvarliga gränsöverskridande hot mot människors hälsa.
- förbättra tillgången på och åtkomsten till ekonomiskt överkomliga läkemedel och medicintekniska produkter och krisnödvändiga produkter i unionen samt stödja innovation när det gäller sådana produkter.
- stärka hälso- och sjukvårdssystemen genom att förbättra deras resiliens och resurseffektivitet, särskilt genom att
- stödja ett integrerat och samordnat arbete mellan medlemsstaterna,
- främja genomförandet av bästa praxis och främja utbyte av uppgifter,
- förstärka hälso- och sjukvårdspersonalen,
- hantera konsekvenserna av demografiska utmaningar, och
- föra den digitala omvandlingen framåt.
EU:s cancerplan anges i EU4Health som en av tre brådskande prioriteringar som ska bana väg för en europeisk hälsounion. Förutom cancerplanen prioriterar man en läkedelsstrategi för EU samt insatser mot covid-19 och förstärkningar av EU:s motståndskraft mot internationella hälsohot.
Motivet till EU:s cancerplan är enligt EU-kommissionen (2021a) att det behövs mer gemensamt ansvarstagande för cancer bland EU:s medlemsländer. Det handlar till att börja med om att cancer är ett ökande problem, som beräknas bli den vanligaste dödsorsaken i EU om cirka ett decennium. Dessutom finns stora skillnader i prevention och vård mellan och inom länder. Man pekar också på stora kostnader för cancerläkemedel och stor variation i kostnader inom EU. Dessutom finns det ökande problem med brist på cancerläkemedel. För att möta dessa problem presenteras åtgärder inom prevention, tidig upptäckt, diagnostik och behandling samt cancerpatienters och canceröverlevares livskvalitet.
En viktig form för genomförandet är så kallade Joint Actions, där länder kan välja att delta i processen att specificera och implementera initiativen i cancerplanen och även få ekonomiskt stöd i genomförandet. Aktörer kan delta i Joint Actions som ”behörig myndighet” (Competent Authority). Det innebär att man som landets formella representant ansvarar för att insatserna som man åtagit sig genomförs, och mottar och fördelar de ekonomiska medlen. Det är upp till varje land att närmare bestämma hur detta ska ske. I den mån implementeringen till exempel kräver insatser från de svenska regionerna behöver de besluta om dem, och kan då ta del av medlen från den behöriga myndigheten. En aktör kan också delta i arbetet som Affiliated Entity och representerar då den egna organisationen (Socialstyrelsen 2023c).
Åtgärdsområden i EU:s cancerplan
I EU:s cancerplan anges fyra åtgärdsområden:
- förebyggande insatser
- tidig upptäckt
- diagnos och behandling
- cancerpatienters och canceröverlevares
Figur 3. EU:s cancerplan.
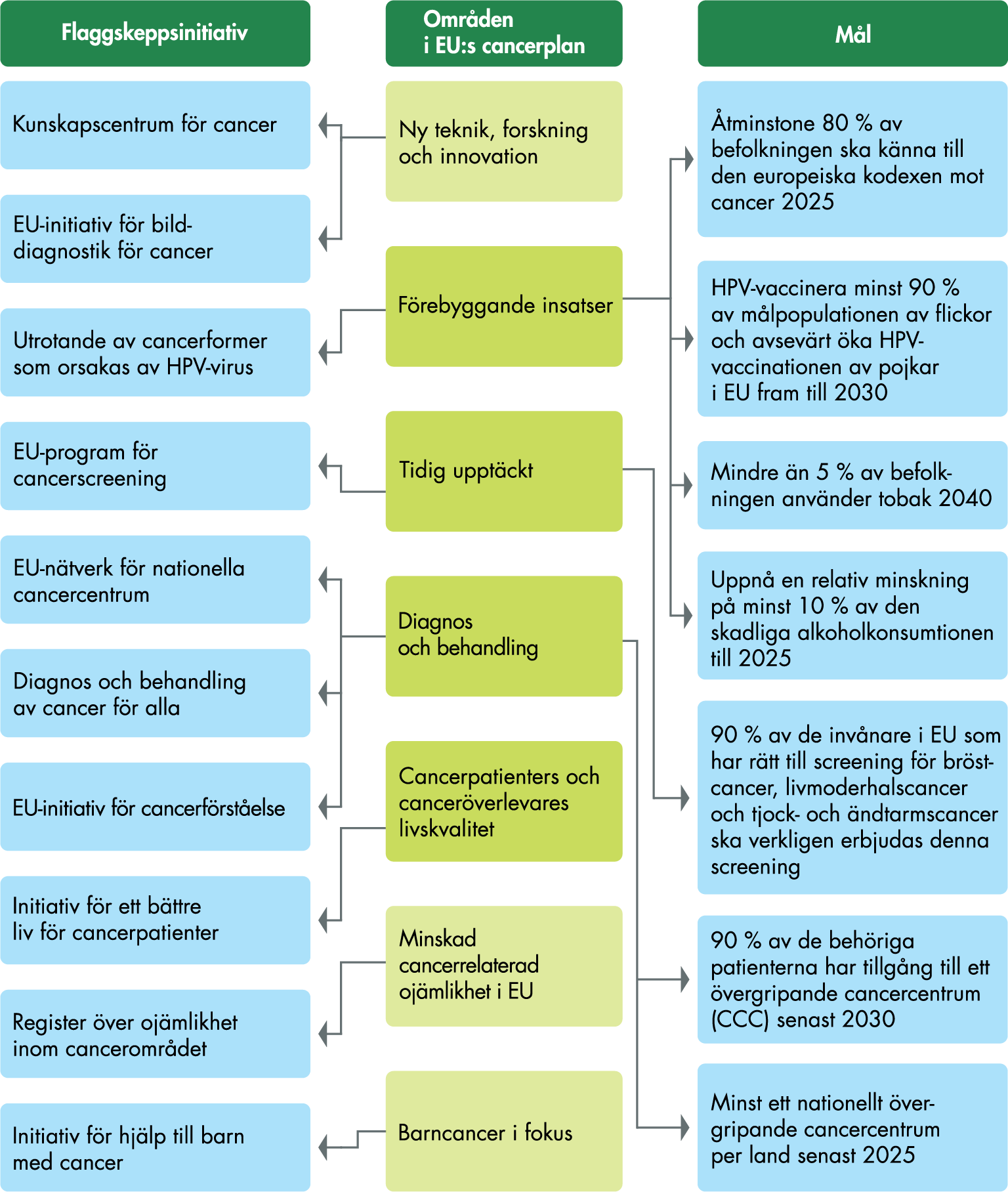
Kopplat till åtgärdsområdena finns 7 mål kopplat till prevention, tidig upptäckt samt diagnos och behandling:
- Prevention:
- Vaccinera minst 90 procent av målpopulationen av flickor mot HPV och avsevärt öka vaccinationen av pojkar i EU fram till 2030.
- Åtminstone 80 procent av befolkningen ska känna till europeiska kodexen mot cancer 2025.
- Mindre än 5 procent av befolkningen använder tobak 2040.
- En relativ minskning på minst 10 procent av den skadliga alkoholkonsumtionen till 2025 (refererar till målen i FN:s hållbara utvecklingsmål).
- Tidig upptäckt:
- År 2025 ska 90 procent av de invånare i EU som har rätt till screening för bröstcancer, livmoderhalscancer och kolorektalcancer verkligen erbjudas denna screening.
- Diagnos och behandling:
- 90 procent av de behöriga patienterna har tillgång till ett CCC senast 2030.
- Det ska finnas minst ett nationellt övergripande cancercentrum per land senast 2025.
Under respektive åtgärdsområde anges även ”flaggskeppsinitiativ”, som kan ses som storskaliga och långsiktiga initiativ som ska bidra till ambitiösa visioner inom EU (figur 3).
Utöver de fyra åtgärdsområdena finns tre områden som inte anges som åtgärdsområden, men som ändå har flaggskeppsinitiativ kopplade till sig:
- Ny teknik, forskning och innovation.
- Minska cancerrelaterad ojämlikhet i EU.
- Sätta barncancer i fokus.
Inom området ny teknik, forskning och innovation ingår till exempel inrätta nya test- och experimentanläggningar med högpresterande datorsystem och AI.
EU:s cancerplan innehåller flera initiativ för utbyte av och tillgång till patientinformation, hälsodata och genetiska data över landsgränserna inom EU. Det handlar till exempel om att skapa det europeiska hälsodataområdet, som ska vara ett ekosystem för hälsodata bestående i gemensamma regler, standarder, infrastruktur och ramverk för styrning (Europeiska kommissionen a.å.a). På det följer det europeiska initiativet för bilddiagnostik av cancer, som ska tillgängliggöra anonymiserade cancerrelaterade bilder till en mängd olika parter inom sjukhusvärlden.
Det pågår också ett arbete med att bygga upp strukturer på EU-nivå för kunskapsstyrning, kunskapsutveckling och kunskapsspridning. Bland annat har ett kunskapscentrum för cancer inrättats under EU-kommissionen (Europeiska kommissionen 2020b). Kunskapscentret ska stödja insatser inom cancerplanen, Cancermissionen samt EU- kommissionens övriga initiativ på cancerområdet genom vetenskapligt baserad kunskap, och ta fram riktlinjer och kvalitetssäkringsprogram. Ett EU-nätverk för erkända nationella CCC:er ska inrättas. Ett register över cancerrelaterad ojämlikhet ska möjliggöra jämförelser mellan olika medlemsstater och regioner (Europeiska kommissionen u.å.b).
Betydelse för den svenska cancerstrategin
På en övergripande nivå överlappar åtgärdsområdena i EU:s cancerplan i hög grad med den svenska cancerstrategins inriktning.
En skillnad är att det finns tydligare mål kopplade till vissa av åtgärdsområdena i EU:s cancerplan, framför allt på preventionsområdet. Till skillnad från de svenska målen är de kvantifierade och tidsatta. Mot bakgrund av de önskemål som framförts i våra intervjuer om mer konkreta mål i den svenska cancerstrategin skulle en väg kunna vara att inkorporera EU-målen i en svensk cancerstrategi. Det behöver dock bygga på en konsekvensanalys och en bedömning av om målen är relevanta för ett svenskt sammanhang.
En annan skillnad mellan EU-nivån och arbetet på cancerområdet i Sverige är att CCC:er har en mer central roll i EU:s cancerplan. Utvecklingen av fler CCC:er och ett nätverk mellan CCC:er ska bland annat främja kunskapsspridning och minska skillnader i tillgång till vård (Innovative partnership for action against cancer 2021; Europeiska kommissionen 2021b). Strukturen för kunskapsstyrning genom en separat RCC-organisationen är däremot unik för Sverige. Våra intervjupersoner menar att man framöver behöver avgöra hur det svenska systemet för kunskapsstyrning ska kopplas samman med strukturer på EU-nivå.
6.1.2 Cancermissionen
Cancermissionen är en av fem missioner i Horisont Europa, EU:s ramprogram för forskning och innovation 2021–2027. Cancermissionen ska bidra till genomförandet av EU:s cancerplan. Programmet är huvudsakligen inriktat på att stödja kunskapsutveckling och spridning av kunskap (Europeiska kommissionen 2020a; Europeiska kommissionen 2021b).
De planerade aktiviteterna är inriktade mot kunskapsutveckling, prevention, diagnostik och behandling samt cancerpatienters och canceröverlevares livskvalitet. Det handlar bland annat om ekonomiskt stöd till forskning och innovation. Förutsättningarna för kunskapsutveckling ska också stärkas genom det europeiska initiativet för att förstå cancer, en digital plattform där forskare från hela världen ska få tillgång till högkvalitativa forskningsdata. Cancermissionen omfattar också skapandet av ett virtuellt europeiskt digitalt centrum för cancerpatienter, som ska länka samman nationella datakällor med patientkontrollerade data samt regionala och nationella cancerregister över lands- gränserna. Aktiviteter inom cancermissionen ska också ge stöd till medlemsländer och CCC:er samt bidra med analys och uppföljning (Europeiska kommissionen 2020a; Europeiska kommissionen 2021b).
Medel från Horisont Europa betalas ut direkt till forskare, innovatörer och forskningsinstitutioner. Fördelningen mellan olika länder är inte bestämd på förhand. Urvalet baseras huvudsakligen på öppna utlysningar. År 2023 utlystes totalt omkring 110 miljoner euro inom ramen för Cancermissionen (Europeiska kommissionen 2023a). Förutom de ekonomiska medel som finns inom Horisont Europa förväntas initiativ inom Cancermissionen även delfinansieras genom medel från medlemsländer, privat sektor och synergier med andra EU-initiativ, till exempel Europeiska atomenergigemenskapen EURATOM-programmet.
6.1.3 Fler initiativ inom EU har betydelse för cancerområdet
Utöver cancerplanen och Cancermissionen sker fler initiativ på EU-nivå som har betydelse för cancerområdet. Det gäller till exempel Agendan för Artificiell Intelligens, Läkemedelsstrategin och Digitala Agendan (Europeiska kommissionen 2021a, 2023a).
Den kommande HTA-förordningen innebär att det ska ske gemensamma utvärderingar på EU-nivå för läkemedel mot sällsynta cancerformer. Att alla länder får rapporter samtidigt ska möjliggöra en mer jämlik introduktion av läkemedel i alla länder (Europeiska kommissionen 2023b).
6.1.4 Sveriges deltagande i EU-initiativen
Flera av våra intervjupersoner lyfter fram att det är viktigt att Sverige deltar aktivt i arbetet på EU-nivå dels för att vi har en bra cancervård och förväntas kunna bidra med kunskap, dels för att kunna få nytta av de europeiska satsningarna.
Den snabba utvecklingen inom EU ställer enligt intervjupersonerna krav på samordning, och på ett strategiskt samarbete mellan olika aktörer och de myndigheter i Sverige som ansvarar för olika EU-program (t.ex. Socialstyrelsen, Folkhälsomyndigheten, Vinnova och DIGG).
På övergripande nivå har Socialstyrelsen uppdraget att samordna det nationella arbetet med att genomföra EU:s cancerplan, medan Vinnova har det nationella ansvaret för Horisont Europa och Cancermissionen. Folkhälsomyndigheten är nationell kontaktpunkt för EU:s hälsoprogram (EU4Health). En mängd andra aktörer inom cancerområdet i Sverige deltar också på olika sätt i de initiativ och grupperingar som skapats inom EU.
Socialstyrelsen håller samman arbetet med EU:s cancerplan
I Socialstyrelsens uppdrag om att samordna arbetet med cancerplanen ingår bland annat att verka för att Sverige är representerat i relevanta arbets- och expertgrupper. Socialstyrelsen ska också informera relevanta aktörer om det pågående arbetet, informera om möjligheter till finansiering genom cancerplanen och stötta aktörer i ansökningsprocessen (Socialstyrelsen 2023c). En utmaning enligt våra intervjuer är komplexiteten i det stora antalet olika program på EU-nivå med ekonomiska medel från flera olika källor inom EU, tillsammans med det decentraliserade systemet i Sverige där olika myndigheter också ansvarar för olika satsningar. Det gör det angeläget att samordna och skapa en gemensam riktning. Som en del i det arbetet har Socialstyrelsen inrättat samverkans- och referensgrupper som samlar aktörer på cancerområdet, vilket vissa av våra intervjupersoner lyfter fram som värdefullt.
Socialstyrelsen bedömer att man är en lämplig aktör för den samordnande rollen, och att man har ett tydligt mandat för rollen.
Det finns idag sex Joint Actions kopplade till genomförandet av EU:s cancerplan. I tre av dem deltar Socialstyrelsen som behörig myndighet från Sverige. Dessa Joint Actions arbetar med screening, ett register över cancerrelaterad ojämlikhet samt ett EU-nätverk för erkända nationella övergripande cancercentrum (CCC). Folkhälsomyndigheten är behörig myndighet i en Joint Action för prevention och Läkemedelsverket i en Joint Action inriktad på kärnteknik och radiologisk teknik. I en sjätte Joint Action, om ett EU-nätverk för expertis inom cancer, saknas en svensk behörig myndighet (Socialstyrelsen 2023c).
Även RCC deltar i arbetet med EU-initiativ
I 2023 års överenskommelse mellan regeringen och SKR om cancervården anges att RCC i samverkan ska samarbeta med övriga nationella aktörer på cancerområdet, så att det svenska bidraget till EU hålls samman och att erfarenheter från det europeiska samarbetet återförs till svensk cancervård. RCC verkar även för att innehållet i den europeiska kodexen mot cancer blir mer känt inom RCC, bland hälso- och sjukvårdspersonal, patienter och närstående samt bland befolkningen som helhet (RCC i samverkan 2020a). RCC i samverkan deltar också som Affiliated Entity i Joint Action om ett register över cancerrelaterad ojämlikhet (Socialstyrelsen 2023c) och RCC planerar medverka som Affiliated Entity i flera av de kommande Joint Actions.
6.1.5 Den svenska cancerstrategin behöver förhålla sig till EU-initiativen
Aktörer på cancerområdet som vi intervjuat menar att initiativen på EU-nivå kommer att vara viktiga för cancerområdet i Sverige framöver, och att en reviderad cancerstrategi behöver förhålla sig till EU-initiativen. En reviderad strategi, menar flera, behöver också ta ställning till hur strukturen i Sverige ska samverka med EU-nivån.
I nästa avsnitt beskriver vi några områden bland EU:s initiativ inom cancer som vi bedömer att en reviderad svensk cancerstrategi särskilt behöver förhålla sig till. Det ska inte ses som en uttömmande lista, utan är de medskick som kommit fram i våra intervjuer.
Den svenska strategin behöver förhålla sig till målen i EU:s cancerplan
I en reviderad cancerstrategi behöver man ta ställning till hur man ska förhålla sig till EU:s cancerplan och de 7 konkreta mål som ingår i den. Flera intervjupersoner pekar på EU:s cancerplan som en inspiration för att ställa upp konkreta mål för en reviderad cancerstrategi. Ingen i våra intervjuer föreslår däremot att EU:s mål i sin helhet bör ingå i en svensk cancerstrategi. Om man bedömer det som ändamålsenligt att inkludera målen i en svensk strategi så behöver det ske efter en konsekvensanalys.
Behov av samordning och tydlighet om representation
Genom EU:s cancerplan finns goda möjligheter för svenska aktörer att ansöka om EU- medel för forskning och utvecklingsarbete. Flera intervjupersoner menar att det finns utrymme för svenska aktörer att bli bättre på att använda sig av dessa möjligheter. Det kan även behövas någon typ av koordinering och stöd för till exempel forskare att söka pengar. Intervjupersonerna pekar också på att information om det som sker på EU-nivå behöver spridas bland relevanta aktörer i Sverige.
EU-initiativen kan ge ökade möjligheter för Sverige att samarbeta med andra länder inom frågor som ovanliga diagnoser, barncancer och nya kostsamma behandlingar. Det kan vara särskilt relevant för ett litet land som Sverige, eftersom det finns få inhemska patienter och därmed ett alltför litet underlag för till exempel kliniska studier.
De strukturer som byggs upp på EU-nivå skapar behov av att tydliggöra vilka aktörer som ska representera Sverige i olika samarbeten, och hur den unika svenska strukturen för kunskapsstyrning ska haka i strukturerna på EU-nivå. Sedan 2022 har Socialstyrelsen i uppdrag att samordna Sveriges insatser i EU:s cancerplan. Socialstyrelsen ser positivt på utvecklingen, men beskriver också att mycket arbete återstår. Socialstyrelsen kan heller inte bestämma vilka roller som olika svenska aktörer ska ha i EU-sammanhang, utan betonar att det behöver diskuteras på högre nivå.
Utveckling mot en enhetlig struktur för hälsodata – nationellt och i EU
Regeringen har inom ramen för Tidöavtalet tagit flera initiativ för att skapa förutsättningar för en mer enhetlig struktur för hälsodata. Utredningen om infrastruktur för hälsodata som nationellt intresse har i uppdrag att ta fram förslag på åtgärder för att åstadkomma en bättre och säkrare informationsförsörjning av hälsodata mellan system och aktörer (SOU 2023:83). E-hälsomyndigheten har ett regeringsuppdrag att påbörja utvecklingen av en nationell digital infrastruktur. Syftet är bland annat att underlätta delning av hälsodata mellan vårdgivare och förbättra informationsförsörjningen av hälsodata till forskning, uppföljning och innovation samt att minska den administrativa bördan för hälso- och sjukvårdens medarbetare genom till exempel automatisk överföring mellan system (Regeringen 2023a).
De här initiativen syftar till att öka möjligheterna att dela hälsodata på ett ändamålsenligt sätt, för att öka genomslaget för nya medicinska metoder och underlätta för forskningen. Det är områden som vi uppfattar är särskilt angelägna inom cancerområdet, eftersom utvecklingen av nya läkemedel ofta riktar sig mot cancer. Det sker också initiativ inom EU som förstärker behovet av att kunna dela data även mellan länder i EU på ett säkert sätt. En viktig förutsättning är då att datadelningen fungerar väl nationellt. Det är särskilt aktuellt för cancerområdet eftersom dessa initiativ berörs i EU:s cancerplan.
EU-kommissionen har tagit fram ett förslag om en förordning för användningen av hälsodata inom EU – European Health Data Space (EHDS) (Europeiska kommissionen 2022). Vi vet ännu inte vad det europeiska hälsodataområdet och andra initiativ inom delning av hälsodata kommer att innebära för Sverige. Enligt delbetänkandet från Utredningen om infrastruktur för hälsodata som nationellt intresse innebär initiativen dock att det blir ännu mer angeläget att åstadkomma en mer enhetlig tolkning av bestämmelserna för delning av hälsodata inom landet (SOU 2023:83). Initiativen skulle även kunna medföra behov av anpassning av svensk lagstiftning. I betänkandet Vidareanvändning av hälsodata för vård och klinisk forskning (SOU 2023:76) framgår att utredningen har förhållit sig till EHDS inriktning och vad den syftar till att åstadkomma samt att utredningens förslag är förenliga med det nuvarande förslaget till EHDS (Europeiska kommissionen 2022). Utredningen lyfter bland annat att bestämmelserna för personuppgiftsbehandlingar och bestämmelser om sekretess behöver ses över.
6.2 Framväxten av Comprehensive Cancer Centres (CCC)
Ackrediterade cancercentrum och integrerade och sammanhållna cancercentrum (CC och CCC, hädanefter CCC) är cancercentrum med både klinisk verksamhet, forskning och utbildning. Skillnaden mellan CC och CCC handlar bland annat om storlek och omfattning på forskningen.
Ackreditering sker sedan 2008 genom Organisation of European Cancer Institutes (OECI), en icke-vinstdrivande icke-statlig organisation som har koppling till EU. För att få ackreditering behöver ett cancercentrum uppfylla europeiska kvalitetsstandarder som innefattar områden som ledningsstruktur, vårdkvalitet, tillgänglighet, multidisciplinär samverkan, patient- och närståendesamverkan, klinisk-translationell forskning samt grund- och vidareutbildning (RCC i samverkan 2023b; OECI 2023). Ackrediteringsprocessen beskrivs i våra intervjuer som en process för verksamhetsutveckling som börjar med att man kartlägger sin verksamhet inom flera områden. Därefter deltar man i ackrediterings- processen som ett granskningsobjekt, vilken ger möjlighet att få goda råd om hur man ska komma vidare i sin förbättringsprocess. Efter ackrediteringen sker regelbunden återackreditering, när centrumets utvecklingsplan följs upp genom fackgranskning (peer review).
6.2.1 Behov av ökad specialisering och klinisk forskning driver utvecklingen
Bakgrunden till framväxten av CCC är utvecklingen inom diagnos och behandling, där man ser behov av ökad specialisering, större patientunderlag för studier och närmare koppling mellan forskning och klinisk verksamhet (SOU 2009:11; Europeiska kommissionen 2021a). Utredningen En nationell cancerstrategi (SOU 2009:11) beskriver att cancervården behöver organiseras om i riktning mot ökad specialisering och närmare band mellan forskning och vård. De nya regionala cancercentrumen föreslogs i betänkandet från 2009 bli cancercentrum som både bedrev vård, forskning och kunskapsstyrning, och utredningen argumenterade för att ett eller två RCC på sikt borde bli ackrediterade CCC (SOU 2009:11). När RCC inrättades gavs de dock en mer begränsad roll, med ansvar för kunskapsstyrning och stöd till verksamheter och forskning men där RCC inte själva bedriver vård eller forskning. Nivåstrukturering av cancervården har istället varit ett separat område för insatser, som främst innefattat en tydligare ansvarsfördelning inom varje sjukvårdsregion samt nationell koncentration av den mest högspecialiserade vården (Socialdepartementet 2011).
Över tid har flera universitetssjukhus valt att söka ackreditering som CCC. Idag finns tre CCC i Sverige: Karolinska CCC (Karolinska universitetssjukhuset i samarbete med Karolinska Institutet), Skåne University Hospital Comprehensive Cancer Center (SUHCCC) (Skånes universitetssjukhus i samverkan med Lunds universitet) och Sahlgrenska CCC (Sahlgrenska universitetssjukhuset i samverkan med Sahlgrenska Akademin). Fler universitetssjukhus förväntas bli ackrediterade i framtiden. Enligt våra intervjuer är Uppsala och Linköping de som kommit längst, men det tycks finnas ett intresse även i Umeå och Örebro.
Framväxten av CCC:er främjas av initiativ på EU-nivå och framöver förväntas fler cancercentrum i Europa bli CCC. Som en del i EU:s cancerplan inrättas ett eget EU-ackrediteringsprogram för cancercentrum, som ska länkas samman i initiativet EU-nätverk för nationella cancercentrum. Nätverket ska organisatoriskt ligga under EU- kommissionen. Kriterierna för ackreditering och formerna för nätverket är inte fastslagna, men tanken är att CCC:erna ska ha en central roll i utvecklingen på cancerområdet i Europa. Målsättningarna i den europeiska cancerplanen är att det ska finnas minst ett CCC i varje land senast 2025, och att 90 procent av de berättigade patienterna ska ha tillgång till ett CCC senast 2030 (Europeiska kommissionen 2021a).
6.2.2 Aktörer uppfattar att CCC förändrar styrstrukturen på cancerområdet
Det framkommer i vår undersökning att många aktörer ser framväxten av CCC:er som en viktig förändring på cancerområdet. De har dock olika bilder av hur exempelvis strukturen för kunskapsstyrning påverkas.
Flera i vår intervjustudie och undersökning till RCC framhåller att det är tydligt att RCC och CCC har olika uppdrag som kompletterar varandra. RCC har ett brett och samlat uppdrag att arbeta med alla delar av cancervården, från prevention till palliativ vård, och har en organisatorisk struktur med nationell samverkan som täcker in alla landets regioner. RCC ansvarar också för den grundläggande kunskapsstyrningen. CCC är däremot en tidsbegränsad ackreditering som är inriktad mot högspecialiserad cancervård och forskning, och finns just nu också bara vid tre sjukhus i landet. CCC beskrivs ha en viktig roll i spetsforskning med koppling till universiteteten och står för den mest högkvalificerade vården. Intervjupersonerna och informanterna menar att CCC ansvarar för implementering och genomförande av kunskapsstöden som kommer från RCC. Socialstyrelsen bedömer däremot att det i beskrivningen av vad ett CCC ska uppfylla finns många ansvarsområden som idag ligger på RCC.
I vår undersökning till RCC nämner flera informanter möjligheterna till ett gott samarbete mellan RCC och CCC om bland annat processer och uppföljning, och att det kan ge förutsättningar för en positiv utveckling av cancervården. En synergi är att det kvalitetsarbete och de arbetsprocesser som behöver upprättas under OECI:s ackreditering och re-ackreditering av CCC kan byggas för de nationella kunskapsstöden på cancerområdet som RCC ansvarar för att ta fram. I stort sett alla områden som lyfts av OECI för en ackreditering, är områden som RCC har jobbat med och kan därmed få draghjälp i genomförandet av CCC.
Samtidigt lyfter flera i vår intervjustudie och undersökning till RCC fram att det finns en risk för oklarheter mellan RCC och CCC som behöver hanteras. Samarbetet ser idag olika ut i olika sjukvårdsregioner och det skulle behövas en tydligare roll- och mandatfördelning och mer gemensamma ramar för samarbetet. Om det inte finns en nära samverkan finns en risk för att de kunskapsunderlag RCC tar fram inte införs, att RCC upplevs försöka styra CCC:s verksamheter eller att det uppstår parallella strukturer. Det kan leda till konkurrens samt ineffektivitet på grund av dubbelarbete och att konflikter och konflikterande styrsignaler tar upp tid.
6.2.3 Rollfördelningen behöver förtydligas i ny cancerstrategi
Den nuvarande cancerstrategin ger ingen vägledning om hur rollfördelningen mellan CCC och RCC ska se ut, men det är viktigt att uppmärksamma i en reviderad strategi. Våra intervjupersoner och informanter har olika bild av hur rollfördelningen bör se ut, men är överens om att det finns ett behov av att se över och tydliggöra rollfördelningen. Sedan 2009 har det tillkommit fler aktörer och flertalet EU-initiativ där det behöver tydliggöras vilken aktör som representerar Sverige i olika sammanhang. Det behöver vara aktörer som har rätt kompetens och mandat att påverka inom EU, men även att besluta hur EU:s arbete ska implementeras i Sverige. I dagsläget uppfattas rollfördelningen som något oklar, inte minst mot bakgrund av att myndigheter minskat sitt arbete inom cancerområdet när ansvaret förts över till RCC. Det är också viktigt att säkerställa att det finns någon aktör med ett nationellt perspektiv på cancerområdet.
Eftersom de svenska strukturerna i dagsläget inte matchar EU:s strukturer, till exempel med ett nationellt CCC, blir det enligt intervjupersoner också en uppgift för Sverige att se till att strukturen för kunskapsstyrning kan fungera bra med resten av Europa (se även 6.1). I övrigt råder det delade meningar i vår intervjustudie och undersökning till RCC om hur rollfördelningen bör se ut. Några menar att RCC:s uppdrag med tiden blivit för brett och att det finns anledning att pröva om vissa delar i uppdraget behöver förtydligas eller flyttas till andra aktörer. Vissa RCC-representanter menar att RCC bör ansvara för kunskapsstöd och vidareutbildning, medan CCC bör ansvara för mer specialiserad vård och forskning. De pekar på att det samtidigt bör finnas en samverkan. Vidare menar några i vår intervjustudie att RCC bör inordnas under CCC eller främst få rollen att stötta CCC. Det mest centrala budskapet från våra intervjupersoner och informanter är dock att det är viktigt att regeringen i cancerstrategin tydliggör de olika aktörernas roller och hur de ska förhålla sig till varandra.
I ett pågående arbete inom EU där både CCC, RCC och Socialstyrelsen deltar, arbetar man nu med en europeisk definition av CCC (som kan skilja sig från OECI:s definition). Man talar också om övergripande cancerinfrastrukturer (CCI:er), nätverk av nationella eller regionala infrastrukturer som ska länka samman kompetensen hos CCC:er över landsgränser. Utöver vård och forskning kommer troligen även ansvar för att ta fram styrdokument och riktlinjer att ligga hos CCC enligt EU-definitionen. Sverige behöver även förhålla sig till detta, eftersom vår nuvarande struktur för kunskapsstyrning utgår från RCC.
6.3 Medicinsk utveckling
Inom cancerområdet pågår en utveckling mot nya avancerade diagnostiska metoder och behandlingsalternativ. De gör det möjligt att tidigare upptäcka cancer, öka överlevnaden och skapa bättre livskvalitet för cancerpatienter.
Precisionsmedicin innebär att man väljer behandling utifrån specifik information om en individ, till exempel från individens genuppsättning (för en närmare definition se Vård- och omsorgsanalys 2021a). Precisionsmedicin medför en ökad träffsäkerhet vid val av behandlingsalternativ och sjukvården får allt bättre möjligheter att sätta in behandlingar som kan ge god effekt. Genterapi och så kallad CAR T-behandling har idag potential att bota patienter vid vissa svåra cancersjukdomar. Det är positivt att patienter får tillgång till nya effektiva läkemedel, men det medför också ökade kostnader och behov av horisontella prioriteringar. Införandet av precisionsmedicin skapar utmaningar kopplat till finansiering, införande och uppföljning och aktualiserar behovet av att utveckla vårdens infrastruktur.
Även om ordnat införande (se avsnitt 3.4.2) idag är en etablerad och central del av införandet av nya cancerläkemedel, och i viss utsträckning för medicinteknik, kan vi konstatera det finns fortsatta utmaningar att hantera. Det gäller bland annat behovet av att utveckla hälsoekonomiska bedömningar av precisionsläkemedel, kombinations- behandlingar och medicintekniska produkter. Det handlar även om att stärka uppföljningen och att säkerställa en jämlik användning av cancerläkemedel. Vi återkommer till de frågorna senare i avsnittet.
6.3.1 Ökade kostnader för cancerläkemedel enligt Socialstyrelsen prognos för 2023–2026
Mycket talar för att den snabba utvecklingen av cancerläkemedel kommer fortsätta även framöver med en introduktion av ett stort antal nya läkemedel. Den här utvecklingen medför samtidigt ökade kostnader. Socialstyrelsens prognos visar på en kostnadsökning från cirka 4,5 miljarder kronor under 2022 till 5,2 miljarder kronor 2025 för cancerläkemedel inom förmånen. Även kostnaderna för rekvisitionsläkemedel har ökat under de senaste åren. Den här utvecklingen antas fortsätta under prognosperioden. Flera faktorer driver på mot ökade kostnader. Antalet cancerfall har ökat över tid, vilket till stor del kan förklaras av en åldrande befolkning där fler insjuknar i cancer, lever längre och behandlas under en längre tid. De nya avancerade läkemedlen medför även en högre kostnad än tidigare. Faktorer som dämpar kostnadsutvecklingen är patentutgångar, omprövningar av subventionsbeslut samt avtal om återbäring mellan regionerna och läkemedelsföretagen (Socialstyrelsen 2023d).
6.3.2 Precisionsläkemedel kan ge bättre möjligheter till behandling men ställer krav på finansiering och infrastruktur
Flera i vår intervjustudie menar att cancerstrategin inte är utformad för att svara upp mot den snabba utvecklingen av precisionsmedicin. De menar att strategin behöver utvecklas för att kunna stötta nödvändiga förändringar i hälso- och sjukvården exempelvis gällande diagnostik, personal- och kompetensförsörjning samt patientdata.
Under 2020–2021 analyserade Vård- och omsorgsanalys på regeringens uppdrag hur utvecklingen av precisionsmedicin har påverkat och kommer att påverka hälso- och sjukvården i rapporten Genvägen till ökad precision – en framåtblickande analys av precisionsmedicin i hälso- och sjukvården. Vår analys visar att användningen av precisionsmedicin kommer att öka under de kommande åren. Under 2021 fanns 70 godkända behandlingar som vi karaktäriserade som precisionsmedicin, men vår bedömning i rapporten var att mellan 300 och 400 nya immunterapier, målriktade läkemedel och tumöragnostiska läkemedel kan vara godkända inom en tioårsperiod. Det är främst inom cancervården som precisionsmedicin bedöms växa. Företrädare för den nationella arbetsgruppen för barncancerområdet och Barncancerfonden pekar samtidigt på vikten av att säkerställa att barn får tillgång till precisionsmedicin. Det förutsätter att kliniska studier där barn ingår blir fler, vilket i sin tur kräver en utvecklad infrastruktur för läkemedelsprövningar.
Utvecklingen av precisionsmedicin inom områden som cancer, sällsynta diagnoser och infektionssjukdomar kommer att påverka stora delar av hälso- och sjukvården i framtiden, även om prognoserna är osäkra. Vår rapport om precisionsmedicin visar att det kommer ställas krav på att utveckla vårdens infrastruktur, till exempel it-system, organisering och personalförsörjning. Särskilt kraftfulla behandlingar och behandlingar med osäkra långtidseffekter kommer innebära att stora delar av hälso- och sjukvården berörs av eftervård och uppföljning under lång tid. När fler patienter får ta del av precisionsmedicin i sjukvården kommer också fler i personalen behöva kompetens att genomföra genetisk diagnostik, precisionsbehandlingar och uppföljning (Vård- och omsorgsanalys 2021a).
Flera som vi har intervjuat, bland annat företrädare för LIF, TLV och CCC, lyfter fram att diagnoskapaciteten kommer behöva byggas ut. För att kunna genomföra avancerad diagnostik i större skala kommer det krävas personal med rätt kompetens, exempelvis laboratorietekniker/biomedicinska analytiker och it-informatiker. Det är bristyrken på många håll i landet och trots att antalet antagna på utbildningarna ökat under många år har antalet examinerade inte ökat i samma takt (Nationella vårdkompetensrådet 2021). En företrädare för CCC menar att möjligheterna till diagnostik och sättet vi screenar cancer kan förändras helt, exempelvis genom användning av blodprov. Det handlar om mycket kostsamma analyser, i både utrustning och kompetens. Flera intervjupersoner och informanter pekar på vikten av att patienten får rätt diagnos redan från början, eftersom den påverkar val av behandling, biverkningar och rehabilitering.
I takt med att diagnostik och behandling av cancer blir mer alltmer avancerad är vår bedömning att precisionsmedicinen till stor del kommer behöva utföras på ett fåtal ställen i vården med nationell upptagning. Regionerna kommer i allt högre utsträckning vara för små för att på ett effektivt sätt kunna erbjuda vård med hög kvalitet. Vissa av de åtgärder vi anser behöver genomföras kan och bör ske på regional nivå, men andra åtgärder kräver nationell samordning och koordination för att patienter ska få del av en jämlik och kostnadseffektiv precisionsmedicin. I våra intervjuer menar flera att en nivåstrukturering kommer att vara nödvändig. Några lyfter samtidigt fram att det är ett dilemma att kompetensen försvinner på mindre sjukhus om allt blir högspecialiserat. De menar att det då blir viktigt att mindre sjukhus kan specialisera sig på delar i vårdkedjan som inte är högspecialiserade och på så sätt avlasta den högspecialiserade vården.
Precisionsmedicin bygger delvis på att stora mängder information om individer samlas in, struktureras och tillgängliggörs för olika aktörer. I regel handlar det om information av personlig och ofta känslig natur. Med hänsyn till den snabba kunskapstillväxten är det dessutom svårt att överblicka och förutse vad informationen i framtiden kommer att kunna användas till. Detta medför att kraven på skyddet av självbestämmandet och den personliga integriteten blir särskilt viktig. Den här utvecklingen innebär att patienter behöver involveras på ett tydligare sätt i beslutsfattande på både systemnivå och individnivå, samt att informationsöverföringen behöver vara adekvat.
Precisionsmedicin har än så länge inte föranlett någon större strukturomvandling i vården. Vi ser dock att vården, i vid bemärkelse, inte är förberedd eller än så länge har de förutsättningar som krävs för ett brett och jämlikt införande av precisionsmedicin. Vår analys av precisionsmedicin visade att det under 2020 genomfördes ungefär 20 000 gensekvenseringar. Det sker i huvudsak inom ramen för befintliga strukturer i hälso- och sjukvården och det är ett relativt litet antal som hittills har behandlats med avancerade gen- och cellterapier i rutinvården. Införandet av dessa terapier har visserligen varit en ansträngning för enskilda verksamheter, vilket föranlett initiativ för nationell samordning, men inte påverkat hälso- och sjukvården i stort. Men på sikt kommer hälso- och sjukvårdssystemet att ställas inför prioriteringar när möjligheterna att tillämpa precisionsmedicin ökar.
För att Sverige ska vara ett föregångsland i att införa precisionsmedicin och fullt ut nå den potential som finns, krävs insatser inom flera områden. Åtgärder krävs av både regeringen och regionerna – enskilt och i samverkan. Ansvarsfördelningen är i vissa delar tydlig, men behöver i andra delar förtydligas, för att inte hindra utvecklingen av precisionsmedicin i vården. Vi identifierade flera områden som behöver hanteras för att potentialen med precisionsmedicin ska kunna tas tillvara, och som en reviderad cancerstrategi behöver ta hänsyn till. I vår rapport om precisionsmedicin (Vård- och omsorgsanalys 2021a) lämnar vi rekommendationer till regeringen och regionerna. Det handlar om att säkerställa
- ett ändamålsenligt tillgängliggörande av hälsodata och vävnadsprover
- att precisionsmedicin skapar värde för patienter och medborgare
- att etik vägleder utvecklingen inom precisionsmedicin
- patienters delaktighet i systemen för precisionsmedicin
- jämlikhet vid införandet av precisionsmedicin
- kompetensförsörjning och kunskapsutveckling
- ändamålsenlig kapacitet i systemen för nationellt ordnat införande samt för nationell kunskapsstyrning
- fler kliniska studier i Sverige.
6.3.3 Nya avancerade behandlingar kräver att hälsoekonomiska bedömningar utvecklas
I den ursprungliga nationella cancerstrategin fanns förslag som syftar till att utveckla nationella hälsoekonomiska bedömningar av rekvisitionsläkemedel. Utgångspunkten var att rekvisitionsläkemedel skulle genomgå samma bedömning av kostnadseffektiviteten som receptbelagda läkemedel inom förmånen (SOU 2009:11). Idag hanteras rekvisitions- läkemedel i den nationella processen för ordnat införande, där TLV genomför en kostnadseffektivitetsanalys och NT-rådet lämnar rekommendationer (Regionernas samverkansmodell för läkemedel 2023a). En utmaning som lyftes fram i En nationell cancerstrategi för framtiden (SOU 2009:11) och som är minst lika aktuell i dag är att nya läkemedel ofta är förknippade med höga kostnader, hög osäkerhet om klinisk effekt på längre sikt men samtidigt har en hög potentiell nytta. Det innebär att det kan vara svårt för regioner och myndigheter att bedöma om kostnaden är rimlig i förhållande till nyttan. De här utmaningarna är särskilt påtagliga för precisionsläkemedel där patientpopulationerna ofta är små, uppföljningstiderna är korta och det saknas kontrollgrupper (TLV 2021b, 2020a). I tidigare rapporter och i vår intervju bedömer TLV att det är svårt att följa upp nya läkemedel nationellt. Dels eftersom det saknas data om rekvisitionsläkemedel på individnivå som är tillgänglig nationellt, dels eftersom det är tidskrävande att beställa data från många olika aktörer. Möjligheten att följa upp med hjälp av den nationella tjänsteplattformen är beroende av att regionerna prioriterar detta, och kvalitetsregistren går inte att använda systematiskt för TLV. Förutom uppgift om rekvisitionsläkemedel på individnivå skulle man också behöva inkludera laboratoriedata i nationella hälsodataregister. Det skulle dock, betonar TLV, gå att göra mycket med den data som finns idag. Myndigheten behöver få författningsstöd för att hantera uppgifter från hälsodataregister på individnivå. Andra utvecklingsområden som TLV lyfter fram är att vidga patientregistret så att rapporteringen inkluderar vårdbesök i den specialiserade öppenvården från annan yrkeskategori än läkare samt besök i primärvården med alla yrkeskategorier. Se även avsnitt 2.4. (TLV 2021a, 2021b, 2020a).
Det finns förhoppningar om att delar av precisionsmedicinen och andra terapier i framtiden blir kostnadsbesparande, men om det faktiskt blir så vet vi ännu inte. För att säkerställa att skattemedlen genererar så mycket värde som möjligt behöver systemen för utveckling, införande och användning av nya metoder och terapier kunna hantera osäkerhet om effekt, säkerhet och kostnadseffektivitet. Processer och modeller behöver utvecklas av sjukvårdshuvudmännen och av berörda statliga myndigheter. Även läkemedelsföretagen har ett ansvar att prissätta produkterna på ett sätt som möjliggör en så bred användning som möjligt (Vård- och omsorgsanalys 2021a).
TLV har haft flera regeringsuppdrag som syftar till att utveckla hälsoekonomiska bedömningar av avancerade terapiläkemedel och precisionsmedicin. I en rapport som publicerades under 2022 pekar TLV på flera utvecklingsområden. Det handlar bland annat om att se över hur myndigheten på ett tydligare sätt kan kvantifiera och redovisa de osäkerheter som finns i en hälsoekonomisk utvärdering, att vikta sannolikheten för olika utfall av kostnadseffektivitet och att utveckla utfallsbaserade betalningsmodeller som kan minska risken för att betalningen för ett läkemedel blir för hög i förhållande till den nytta som behandlingen ger i klinisk vardag. TLV anser också att det är angeläget att utreda frågan om hur omfattningen av användningen av ett läkemedel bör påverka hur hög kostnad som accepteras (TLV 2022b).
Givet att vi kommer se en snabb utveckling av precisionsläkemedel med många nya indikationer kommer det att finnas ett allt större behov av hälsoekonomiska bedömningar inom cancerområdet. Det kommer att ställa krav på att TLV har kompetens att genomföra fler och allt mer avancerade analyser, vilket kräver att det finns tillräckligt med hälso- ekonomer, medicinska utredare och jurister inom myndigheten. Sverige är ett relativt litet land, vilket talar för att de kommer behövas ett fördjupat samarbete med andra EU-länder. Resonemangen om kostnadseffektivitet väcker också frågan om hur samhället ska hantera kostnadseffektivitet i olika sektorer och för olika behandlingar. Idag är det stort fokus på kostnadseffektivitet hos just läkemedel, medan andra delar av sjukvården inte granskas lika noga med avseende på vilken effekt som uppnås för de medel som investeras. Samma sak gäller för de flesta områden utanför sjukvården. För att systemet ska uppfattas som legitimt bör det ställas liknande krav på kostnadseffektivitet i olika användningsområden.
För nya medicintekniska produkter som introduceras på marknaden är tillgången till data om effekter ofta begränsad och det kan finnas osäkerhet kring hur produkten kommer att användas i klinisk praxis. Det kan därför finnas osäkerheter i bedömningen av en produkts värde och hur kostnaden står i relation till dess nytta. TLV har påtalat behovet av att vidareutveckla tillgången till kliniska studier och effektdata för medicintekniska produkter för att skapa bättre förutsättningar för att bedöma nya produkters kostnadseffektivitet (TLV 2020).
Sammantaget är vår bedömning att en utvecklad cancerstrategi behöver stötta en vidareutveckling av hälsoekonomiska bedömningar som möter de förutsättningar som finns hos allt mer avancerade behandlingar. Det behöver också finnas tillräcklig kapacitet inom TLV och inom regionernas samverkansmodell för ordnat införande för att säkerställa att kostnadseffektivitetsanalyser, avtalsförhandlingar med läkemedelsföretag, rekommendationer och uppföljning kan genomföras i den utsträckning som behövs.
6.3.4 Bristande möjligheter till uppföljning
För att samhällets resurser ska kunna används på bästa sätt och för att patienter ska få tillgång till kostnadseffektiva och säkra läkemedel är det centralt med en fungerande uppföljning av läkemedelsanvändningen. I En nationell cancerstrategi för framtiden (SOU 2009:11) föreslogs att en gemensam modell för att uppnå en nationellt samordnad uppföljning i introduktionsfas för nya tekniker inklusive nya läkemedel skulle skapas.
Trots de förslagen och många andra senare initiativ är möjligheterna att följa upp cancerläkemedlens användning och effekt fortfarande begränsade. I våra intervjuer lyfter många fram en utvecklad uppföljning som en nyckelfråga för cancerstrategin. Flera pekar på att det är problematiskt att det saknas möjligheter till uppföljning på individnivå för rekvisitionsläkemedel. Det innebär att det på nationell nivå inte är möjligt att koppla ihop en patients användning av ett eller flera läkemedel med annan behandling. Avsaknaden av individdata för rekvisitionsläkemedel försvårar uppföljningen av läkemedlens effekt men också utfallet i de avtal som regleras mellan läkemedelsföretag och regionerna (TLV 2020a). Den statliga utredningen Bättre förutsättningar för uppföljning av hälso- och sjukvården (Dir. 2023:48) har uppdraget att analysera bestämmelserna för hälsodataregister och föreslå regler för behandling av personuppgifter som avser rekvisitionsläkemedel samt särskilt bedöma om uppgifterna kan samlas in via registret nationell läkemedelslista. Uppdraget ska redovisas senast den 30 juni 2024.
Regionerna har inom ramen för RCC tagit initiativ till det gemensamma läkemedels- registret Register för nya cancerläkemedel (RCL). RCL omfattar i dag 30 olika cancerläkemedel. Syftet är att få bättre kännedom om hur nya cancerläkemedel introduceras och används runt om i landet (RCC i samverkan 2022f).
En uppföljning som RCC har gjort visar på skillnader i inrapporteringen till RCL mellan regionerna. Även om inrapporteringen till registret successivt har ökat kan data från RCL ännu inte kan användas fullt ut för att jämföra verksamheternas läkemedelsanvändning och upptäcka eventuell under- eller överanvändning av ett specifikt läkemedel i olika regioner (RCC i samverkan 2022f).
En faktor som påverkar benägenheten att registrera data är att professionen upplever en ökad administrativ börda kopplat till inrapporteringen. Rapporteringen sker ofta manuellt och i flera fall måste data dokumenteras i både journalsystem och kvalitetsregister. Om inte professionen ser en koppling mellan det de registrerar och nyttan för den enskilda kliniken minskar incitamenten att rapportera in data (Vård- och omsorgsanalys 2017b). Det finns flera pågående utvecklingsinitiativ både på nationell nivå och inom hälso- och sjukvården som syftar till att utveckla uppföljningen av läkemedel. Det handlar om bland annat flera regeringsuppdrag och det sker en utveckling av kvalitetsregister inom området. Vi ser positivt på att det tas initiativ till att utveckla nya register, men de kan ses som en övergångslösning innan mer avancerade register med automatisk överföring är på plats. En av de övergripande slutsatserna redan i Vård- och omsorgsanalys utvärdering av den nationella kvalitetsregistersatsningen 2012–2016 var att det är nödvändigt att påbörja en förflyttning, från dagens fragmenterade lösning med enskilda kvalitetsregister mot en modell som på ett bättre sätt möter de samlade behoven av information om vårdens kvalitet (Vård- och omsorgsanalys 2017a). Vi ser därför att det är viktigt att framtidens informationssystem som nu kravställs och utvecklas säkerställer fångst av de data som behövs för uppföljningen av cancerområdet. Det behöver ske utan onödig administration.
I det här avsnittet har vi fokuserat på cancerläkemedel, men det är även viktigt att se till helheten. I helheten ingår beröringspunkter mellan cancerläkemedel och andra läkemedel, liksom hur uppföljningen av cancerläkemedel relaterar till andra delar av behandlingskedjan, till exempel kirurgi, strålning och rehabilitering. Vi delar bilden från intervjuerna att utvecklingen av uppföljningen av cancerområdet är en nyckelfråga för cancerstrategin, eftersom den är avgörande för utvecklingen många andra områden, till exempel hälsoekonomiska bedömningar, effektutvärdering och uppföljningen av utfall av avtal. Ytterst handlar behovet av en förstärkt uppföljning om att säkerställa att patienter får tillgång till säkra och effektiva behandlingar till en rimlig kostnad för samhället.
6.4 Omställningen till en god och nära vård
Det pågår en omställning i hälso- och sjukvården till en god och nära vård. Målen med omställningen är bland annat att primärvården ska vara navet i vården och att patienten ska få en god, nära och samordnad vård som stärker hälsan. Omställningen är en av de omvärldsfaktorer som kan påverka inriktningen på en ny cancerstrategi.
6.4.1 Effektivare resursutnyttjande och mer stöd vid långvariga och kroniska tillstånd
Under 2018 lämnade regeringen en proposition till riksdagen med förslag till ett första steg i hälso- och sjukvårdens omställning till en god och nära vård, där primärvården ska bli den tydliga basen och navet i hälso- och sjukvården (prop. 2017/18:83). Regeringen har därefter lämnat ytterligare förslag i propositioner, bland annat med en förtydligad målbild för omställningen (prop. 2019/20:164, 2021/22:72). De övergripande målen med omställningen är att patienten får en god, nära och samordnad vård som stärker hälsan, att patienten är delaktig utifrån sina förutsättningar och preferenser och att hälso- och sjukvårdens resurser används på ett mer effektivt sätt.
Som bakgrund till omställningen lyfte regeringen fram behovet av att gå från ett sjukhustungt system till ett system där primärvården får förutsättningar för att klara uppdraget som första linjens vård. Det behövs en reform för att stärka och utveckla de delar i hälso- och sjukvårdssystemet som har bäst förutsättningar att hantera både närhet till patienten och komplexitet i sjukdomstillstånd. Bättre stöd vid långvariga, kroniska och komplexa tillstånd och ett effektivare resursutnyttjande bör känneteckna en modern hälso- och sjukvård enligt regeringen. Vårdens struktur måste underlätta koordineringen av olika vårdinstanser och aktörer, utifrån varje patients individuella behov. I det sammanhanget betonade regeringen att primärvård är ett ansvar för både regioner och kommuner. Enligt regeringens bedömning har den kommunala hälso- och sjukvården en nyckelroll i utvecklingen till en mer nära vård, inte minst vården av multisjuka och äldre patienter. Samverkan mellan regioner och kommuner och ett ökat fokus på den kommunala hälso- och sjukvården är därför centralt för att uppnå en god och nära vård (prop. 2019/20:164).
Lagreglerat grunduppdrag för primärvården:
Regeringens insatser för att stödja omställningen omfattar lagändringar, stimulansmedel och uppdrag till flera myndigheter (Vård och omsorgsanalys 2023b). En av de centrala lagändringarna gäller primärvårdens grunduppdrag. Enligt 13a kap. 1 § hälso- och sjukvårdslagen (2017:30), ska regioner och kommuner inom ramen för verksamhet som utgör primärvård särskilt:
- tillhandahålla de hälso- och sjukvårdstjänster som krävs för att tillgodose vanligt förekommande vårdbehov,
- se till att vården är lätt tillgänglig,
- tillhandahålla förebyggande insatser utifrån såväl befolkningens behov som patientens individuella behov och förutsättningar,
- tillhandahålla rehabiliterande insatser utifrån patientens individuella behov och förutsättningar,
- samordna olika insatser för patienten i de fall det är mest ändamålsenligt att samordningen sker inom primärvården, och
- möjliggöra medverkan vid genomförande av forskningsarbete.
6.4.2 Primärvården har ännu inte förutsättningar att ta sitt ansvar
I vår pågående utvärdering av omställningen har vi konstaterat att mycket arbete med att genomföra omställningen pågår i regioner och kommuner, både på strategisk nivå och i projektform. Men omställningen är ännu inte på ett påtagligt sätt synlig i verksamheterna, och vi ser få tecken på att förutsättningarna har stärkts för att nå omställningens mål. Vår bild är att det nationella grunduppdraget har tydliggjort förväntningarna på primärvården, men att det i nuläget saknas förutsättningar för att klara uppdraget. Vår utvärdering visar till exempel att både samverkan och förebyggande arbete ses som centrala för att nå omställningens mål, men att det saknas resurser för att kunna prioritera dessa uppdrag tillräckligt (Vård- och omsorgsanalys 2023b).
I vår utvärdering av omställningen har vi också sett en trend mot kostnadsökningar inom den kommunala hälso- och sjukvården. De verkar inte bero på en uttalad strategi mellan regioner och kommuner, utan är snarare ett resultat av att kommunerna tar hand om fler patienter med stora och komplexa vårdbehov. Vi vet ännu inte vilka förutsättningar kommunerna har för att möta den utvecklingen eller vilka prioriteringar den kommunala hälso- och sjukvårdens ökade kostnader innebär (Vård- och omsorgsanalys 2021c).
I vår intervjustudie nämner flera att omställningen till en god och nära vård är en av de faktorer som kan påverka cancervården. De anser också att det finns anledning att tydliggöra vilken roll den nära vården ska ha i cancervården, samt hur samarbetet mellan primärvården och den specialiserade vården ska se ut. I det sammanhanget nämns också att egenmonitorering behöver utvecklas som en del i förflyttningen av vård från sjukhusen till hemmet.
Det finns dock en farhåga om att omställningen kommer ta tid att genomföra. I intervjuerna framkommer olika svårigheter för primärvården att ta sitt ansvar i cancervården. Till exempel nämns primärvårdens bristande kapacitet, bland annat på grund av svårigheter med kompetensförsörjningen. Flera framhåller att primärvården inte har förutsättningar att fullt ut ta sitt ansvar för prevention som rör ohälsosamma levnadsvanor, tidig upptäckt och rehabiliteringsinsatser. De pekar också på att det behövs bättre strukturer för informations- och kunskapsöverföring mellan sekundärvård och primärvård samt bättre kontaktvägar. Även Socialstyrelsen har konstaterat liknande utmaningar med att involvera primärvården i arbetet (Socialstyrelsen 2023a).
I vår intervjustudie reflekterar flera över att cancerstrategin inte har påverkat den kommunala hälso- och sjukvården, samt att kommunerna inte är särskilt närvarande i RCC och kunskapsstyrningen. Det nämns dock att det finns andra områden inom systemet för kunskapsstyrning som har mer samverkan med kommunerna och att cancervården kan lära av dem.
En kommentar handlar om att utformningen av den statliga styrningen med riktade medel har gjort det svårt att balansera cancer mot andra delar av vården, och att primärvården varit särskilt svår att inkludera. Ett annat exempel på det är att särskilda rehabiliteringscentrum skapats för cancer trots att rehabiliteringen har mycket gemensamt med rehabilitering vid andra sjukdomar. En kommentar till det är att cancervården får mycket resurser jämfört med andra sjukdomar, men att det borde vara möjligt att i högre grad använda gemensamma resurser.
I några intervjuer framkommer också att cancer tack vare de medicinska framstegen nu blivit mer av en kronisk sjukdom. Det gör det ännu mer angeläget att sätta cancerstrategin i relation till vården i stort och stärka integreringen med övrig hälso- och sjukvård. Samtidigt har vi i vår utvärdering av omställningen konstaterat att det ännu är oklart vilken roll sjukhusen eller annan specialiserad vård ska spela i omställningen och att regioner och kommuner, i genomförandet av omställningen, behöver beakta hur hälso- och sjukvården som helhet ska struktureras och planeras på kort och lång sikt (Vård- och omsorgsanalys 2023b).
7 Slutsatser
Vi har belyst styrkor och utvecklingsbehov i den nationella cancerstrategin och dess implementering samt beskrivit omvärldstendenser och deras innebörd för cancerstrategin framöver. Vi har också kartlagt styrkor och svagheter inom SVF och barncancer. Lägesbilden har tagits fram utifrån följande tre frågor:
- Vilka är styrkorna och utvecklingsbehoven i styrningen genom cancerstrategin?
- Vilka är styrkorna och utvecklingsbehoven i måluppfyllelsen och implementeringen av insatserna inom ramen för cancerstrategin?
- Vilka omvärldsfaktorer skapar behov av förändringar i cancerstrategin?
Detta är våra övergripande slutsatser:
- Den nationella cancerstrategin ger struktur och riktning men brister i prioritering, implementering och uppföljning.
- Måluppfyllelsen och insatserna skiljer sig åt mellan cancerstrategins olika målområden.
- De standardiserade vårdförloppen har skapat sammanhållna flöden i cancervården men behöver utvecklas.
- Barncancervården har blivit en del i cancerstrategin men utvecklingsbehov kvarstår.
- Medicinteknisk utveckling, EU-initiativ och omställningen till god och nära vård behöver vägas in i en ny strategi.
Utöver dessa slutsatser har vi också identifierat ett antal medskick till regeringen att överväga i arbetet med att revidera cancerstrategin. Uppdraget har genomförts på kort tid och rapporten ger en översiktlig bild av utvecklingen sedan cancerstrategin infördes samt nuläget. Våra slutsatser och medskick bör därför ses som en presentation av olika ingångar att studera vidare innan regeringen landar i en reviderad strategi.
7.1 Strategin ger struktur och riktning men brister i prioritering, implementering och uppföljning
Vår första slutsats är att cancerstrategin som styrmedel har styrkor i form av struktur och riktning men också svagheter i form av brister i prioritering, implementering och uppföljning. Synen på cancerstrategin som styrmedel är över lag positiv bland aktörerna som intervjuats. Cancerstrategin upplevs ha gett en gemensam inriktning för arbetet och skapat en struktur för nationell samverkan på flera områden, och på så sätt blivit en modell för att skapa större enhetlighet i cancervården i Sveriges decentraliserade hälso- och sjukvårdssystem.
Men det finns också utvecklingsbehov. En utmaning i styrningen genom cancerstrategin är att styrdokumenten saknar vägledning för prioriteringar – både mellan olika mål och insatser inom cancervården och mellan cancervården och annan vård. Osäkerhet om vad som bör prioriteras och strukturella utmaningar bidrar till en ofullständig och ojämn implementering. Trots goda intentioner om uppföljning har inte cancerstrategin följts upp på ett systematiskt sätt. Och trots en rad initiativ för att stärka förutsättningarna för uppföljning inom cancervården kvarstår flera utmaningar.
7.1.1 Målen för cancerstrategin är fortfarande relevanta, men kan utvecklas
Cancerstrategins mål uppfattas i hög grad som relevanta och tar sikte på centrala aspekter av hälso- och sjukvårdens mål, samtidigt som de utgår från relevanta utmaningar och tydliga förbättringsbehov.
En svaghet i cancerstrategins övergripande mål är att målen inte konkretiseras i mer mätbara mål, kompletteras med målnivåer eller tidsätts. Det bidrar till brister i uppföljningen och ansvarsutkrävandet och medför en osäkerhet om måluppfyllelsen. Det finns också omvärldsfaktorer som förstärker behovet av att se över målstrukturen. EU:s cancerplan innehåller exempelvis ett antal konkreta mål, framförallt inom prevention.
En annan svaghet är att det är svårt för aktörerna som ska förverkliga cancerstrategins insatser att avgöra vilka mål och insatser som är högst prioriterade och hur insatser inom cancerområdet ska prioriteras gentemot vården i övrigt. Flera efterlyser en mer genomtänkt och tydlig inriktning inom ramen för cancerstrategin, där de högst prioriterade områdena anges.
Trots att inget mål anges som högre prioriterat än de andra, finns det stora skillnader i hur målen konkretiserats i form av insatser. I våra intervjuer lyfter flera fram några områden som de upplever är lägre prioriterade: prevention som rör ohälsosamma levnadsvanor, skillnader mellan grupper samt rehabilitering och palliativ vård. Inom de områdena är insatserna färre och mindre omfattande, även om det ändrats något de senaste åren. Många av de insatser som genomförts inom ramen för cancerstrategin har inriktats mot ökad överlevnad och bättre omhändertagande, främst före och under behandling. Insatser för att stärka personcentreringen i de senare delarna av cancervården har varit mindre framträdande än under behandling.
7.1.2 Strukturen för genomförande kännetecknas av förbättrad samverkan men bristande förutsättningar för implementering
Vår bedömning är att cancerstrategin har skapat en struktur för helhetssyn, samsyn och samverkan mellan olika aktörer, särskilt staten, RCC och regionerna.
Ansvarsfördelningen inom cancerstrategin är i huvudsak tydlig när det gäller RCC och statliga myndigheter. I första hand är det RCC som bland annat har ansvaret för kunskapsstyrning, att utveckla vårdprocesserna samt dialog med regionerna. En av de tydligaste styrkorna bland cancerstrategins alla beståndsdelar är etableringen av RCC och den kunskapsstyrning som RCC har ansvaret för, till exempel vårdprogram och standardiserade vårdförlopp. Myndigheternas uppdrag har huvudsakligen gått ut på att stötta med kompletterande strukturer och uppföljning.
Över lag uppfattas RCC som en aktör med ett brett ansvar som samlar många aktörer och bidrar till samverkan och fungerar som en länk mellan statliga myndigheter, regioner och verksamheter. Av vissa patientorganisationer upplevs RCC som en bra ingång, medan andra har en mer negativ bild.
På många sätt har RCC haft goda förutsättningar att genomföra cancerstrategin – de har haft en långsiktig finansiering och har högt förtroende bland hälso- och sjukvårdens aktörer.
RCC:s möjligheter att svara mot sitt uppdrag begränsas dock av att man är en kunskapsstyrningsorganisation utan beslutsmandat. Ett återkommande tema är att uppdraget ibland inte upplevs motsvara möjligheterna att påverka. De förändringar som drivs av RCC kräver regionala beslut och prioriteringar, men regionernas ansvar är otydligt i överenskommelserna. Tillsammans med de vaga målen leder det till en osäkerhet om vad cancerstrategin faktiskt innebär för vården och för patienterna. Cancerstrategin skapar på så sätt en förväntan på resultat som inte alltid förverkligas. Flera strukturella problem hanteras inte, till exempel bristande kompetensförsörjning och stöd för horisontella prioriteringar. De kopplas inte ihop med planeringen, och har därför försvårat implementeringen. Bristande förankring i vården uppfattas också som ett hinder för implementering.
Sammantaget finns ett missnöje med det bristande genomslaget och de kvarstående regionala skillnaderna. Det skapar en önskan om ett ökat statligt ansvarstagande eller ett tydligare formulerat uppdrag för någon aktör på en rad delområden som rör cancervården. Det handlar i synnerhet om de områden där man upplever att utvecklingen inte har kommit tillräckligt långt, till exempel prevention som rör ohälsosamma levnadsvanor, screening, rehabilitering, palliativ vård och forskning. Flera av de områdena karakteriseras också av att de omfattar fler sjukdomsgrupper än cancer.
7.1.3 Strategin har bidragit till förbättrade uppföljningsmöjligheter, men har inte följts upp systematiskt
Ett utvecklingsbehov är uppföljningen av cancerstrategin i sin helhet. Utredningen som lade grunden för cancerstrategin lämnade flera förslag på hur cancerstrategin borde följas upp. Bland annat föreslog man att målen skulle följas upp löpande, för att ge kunskap om utvecklingsbehoven och kunna justera insatserna. Även om det gjorts vissa punktinsatser i den riktningen, har det saknats en systematisk uppföljning.
Den sammantagna bilden från våra intervjuer är att förbättrad uppföljning kan göra cancerstrategin till ett tydligare och mer effektivt styrinstrument. Det anses önskvärt att någon aktör får i uppdrag att ta fram ett ramverk för uppföljning, definiera centrala indikatorer och löpande följa upp utvecklingen inom de olika målen i cancerstrategin. Det finns också ett behov av att följa upp genomslaget för riktlinjer. Vissa intervjupersoner lyfter även fram att det är viktigt att vidta åtgärder om riktlinjer inte efterlevs. Det kopplar i sin tur an till behovet av välmotiverade och konkreta mål i cancerstrategin.
Uppföljningsmöjligheter saknas på flera områden
Cancerstrategin har bidragit till värdefull utveckling av uppföljningen inom cancervården. Några exempel på det är utvecklingen av uppföljning av patientrapporterade upplevelsemått, väntetidsdata och register för cancerläkemedel.
Kvalitetsregistren på cancerområdet upplevs ha förhållandevis god kvalitet och täckningsgrad, men ur forskningssynpunkt kan det finnas utrymme för förbättringar. Det handlar bland annat om att inkludera nya variabler i takt med den medicinska och medicintekniska utvecklingen. För att möjliggöra uppföljning på nationell nivå skulle det även vara önskvärt med en större enhetlighet, till exempel när det gäller patientrapporterade utfallsmått (PROMs). Cancerläkemedelsregistret bidrar till att möjliggöra uppföljning av rekvisitionsläkemedel i cancervården, men täckningsgraden är fortfarande låg.
Det kvarstår flera utvecklingsbehov när det gäller förutsättningarna för uppföljning, både för nationell uppföljning, verksamhetsutveckling och forskning. Utmaningarna är i regel desamma som finns i hälso- och sjukvården i stort. En sådan utmaning är att det saknas uppgifter om primärvårdens insatser och rekvisitionsläkemedel i nationella hälso- dataregister. En annan utmaning, särskilt för nationell uppföljning och hälsoekonomisk- utvärdering av nya läkemedel, är att strukturen för datakällor är fragmentarisk, att olika källor inte kan kopplas ihop, att kvaliteten brister och att det behövs kommunicerande it- system och automatisk överföring för att minska den administrativa bördan. Det innebär att det är svårt att få tillgång till och koppla ihop nödvändiga data från olika källor, för att kunna analysera måluppfyllelsen och stödja implementeringen av cancerstrategin.
Utvecklingen inom precisionsmedicin och EU-samarbeten aktualiserar förbättringar i informationshanteringen och uppföljningsmöjligheter av t.ex. nya läkemedel. Även EU-initiativ kring delning av hälsodata inom EU skapar behov av ökad nationell samordning av hälsodata.
Ett område som en reviderad cancerstrategi behöver ta ställning till är om uppföljningen ska förbättras genom de nationella initiativen för att skapa en förbättrad infrastruktur för hälsodata eller om det är lämpligast att satsa på att utveckla den uppföljningsstruktur som finns på cancerområdet. Vissa intervjupersoner pekar på att förutsättningarna för uppföljning på cancerområdet är förhållandevis goda och det därför är viktigt att fortsätta med det som fungerar i dag, i väntan på att de mer övergripande initiativen har nått god funktionalitet.
7.2 Måluppfyllelsen och insatserna skiljer sig åt mellan strategins olika målområden
Vår andra slutsats är att det finns en variation i hur långt man kommit inom cancerstrategins fem mål, både vad gäller måluppfyllelse och i vilken mån man initierat insatser inom respektive område. Det finns många insatser kopplade till överlevnad och omhändertagande, och inom de områdena kan vi också se en positiv utveckling. När det gäller risken för insjuknande och jämlikhet mellan grupper är utvecklingen mindre tydlig och det har initierats färre insatser från nationell nivå, sett till hela perioden.
Vår undersökning gör det inte möjligt att avgöra i vilken utsträckning insatserna inom cancerstrategin direkt har påverkat resultatet i relation till strategins mål. Men vår rapport ger en bild av utvecklingen i relation till målen, det vill säga om läget har förbättrats eller försämrats i relation till målen, och hur väl implementeringen av cancerstrategin bedöms ha fungerat inom de olika områdena.
7.2.1 Det har varit lättare att arbeta med frågor som är mer begränsade till cancervården
En stor del av insatserna inom ramen för cancerstrategin handlar om att bygga upp strukturer för kunskapsstyrning och samordning, särskilt inrättandet av RCC. De strukturerna tycks sammantaget ha fungerat bättre när det gäller frågor som lättare kan avgränsas till cancervården, till exempel omhändertagande och medicinsk kvalitet i behandlingen.
Däremot har det varit svårare att arbeta med många av de frågor som är bredare än cancervården och som kräver samverkan med aktörer utanför specialistvården. Utgångsläget har också sett olika ut inom olika områden. Uppföljning pekar mot svårigheter med att åstadkomma förändring inom strukturella frågor, som kompetensförsörjning, inom ramen för en cancerstrategi. Det har samtidigt skett bredare initiativ med exempelvis datatillgång och kompetensförsörjning utanför cancerområdet, men vi kan inte avgöra hur de påverkar cancerområdet.
7.2.2 Överlevnad, personcentrering och strukturer för kunskapsstyrning framstår som starkare områden
Vår kartläggning visar att många insatser har skett riktat mot målet om ökad överlevnad, och över lag har insatserna bedömts vara välfungerande. Överlevnaden efter en cancerdiagnos har också förbättrats sedan cancerstrategin togs fram. De regionala skillnaderna i överlevnad ser även ut att ha minskat något. Den gemensamma strukturen för kunskapsstyrning som byggts upp inom ramen för cancerstrategin uppfattas generellt som framgångsrik och bedöms ge bättre förutsättningar för geografisk jämlikhet. Särskilt uppbyggnaden av RCC-strukturen – som tar sikte på alla målområden – har över lag bedömts som framgångsrik.
Vår sammanställning visar att en mängd insatser har skett riktade mot målet om ökad kvalitet i omhändertagandet ur ett patientperspektiv. Flera av de åtgärder för bättre omhändertagande som föreslogs i betänkandet har genomförts. Patienternas upplevelser av omhändertagandet vid utredning och behandling är över lag goda och tycks ha förbättrats något över tid. Även om vi inte kan följa utvecklingen i patientupplevelser över hela perioden så tycks förutsättningarna för personcentrering och sammanhållen vård vara bättre. Det arbete som RCC bedrivit med kontaktsjuksköterskor, individuella vårdplaner och med verksamhetsövergripande vårdprocesser inom ramen för de standardiserade vårdförloppen har över lag bedömts som framgångsrikt. Det har också skett omfattande insatser inom ramen för de standardiserade vårdförloppen för att korta väntetiderna. Vårdförloppen ledde initialt till kortare väntetider för vissa diagnoser, men förbättringarna har varit relativt små och ojämna och ändamålsenligheten i ledtiderna och ledtidsmålet har ifrågasatts (se avsnitt 7.3).
7.2.3 Prevention som rör ohälsosamma levnadsvanor, livskvalitet och jämlikhet mellan grupper framstår som svagare områden
När det gäller målet att minska risken för insjuknande är det svårt att bedöma hur utvecklingen sett ut sammantaget. För de cancerformer vi undersökt närmare har risken för insjuknande utvecklats i olika riktning, och jämförelser över tid kompliceras av att diagnostiken sannolikt förbättrats. Däremot framkommer att det även framöver finns en stor potential att förebygga insjuknande, eftersom en stor andel av cancerfallen även idag uppskattas vara kopplade till påverkbara faktorer. Utredningen En nationell cancerstrategi betonade särskilt vikten av att prioritera prevention i förhållande till behandling, men utifrån de nationella styrdokumenten tycks inriktningen inte ha varit sådan.
Prevention som rör ohälsosamma levnadsvanor har varit relativt lite i fokus i den nationella styrningen under större delen av perioden. Mer fokus har legat på prevention och tidig upptäckt genom screening. Den ambition som fanns i cancerstrategin om ett starkare och mer strukturerat arbete med cancerprevention kopplat till levnadsvanor tycks inte ha förverkligats förrän i slutet av perioden. Ett mer övergripande arbete i form av en nationell plan för cancerprevention, nationella riktlinjer för prevention och behandling vid ohälsosamma levnadsvanor och ett nationellt programområde (NPO) för levnadsvanor har tagit form under de senaste åren, men det är ännu för tidigt för att se hur det faller ut.
Det är svårare att avgöra hur utvecklingen sett ut i relation till målet om förbättrad livskvalitet, eftersom det saknas sätt att följa upp utfall i livskvalitet på nationell och cancerövergripande nivå. Indikatorer över arbetssätt tyder på att den palliativa vården på flera sätt blivit bättre under perioden. När det gäller rehabilitering saknas underlag om hur tillgång och kvalitet utvecklats. Både palliativ vård och rehabilitering ingår i RCC:s uppdrag, och RCC:s arbete uppfattas ha bidragit till förbättringar. Dessa områden har samtidigt varit i jämförelsevis lite fokus i den nationella styrningen fram tills de senaste åren.
När det gäller målet om minskade skillnader mellan befolkningsgrupper har insatser i stort sett saknats i den nationella styrningen. Även om insatser skett inom RCC så tycks det ha saknats ett samlat grepp om frågan, och uppföljningen tyder på att skillnader mellan befolkningsgrupper varit en svår fråga för RCC att arbeta med. Skillnaderna i insjuknande mellan befolkningsgrupper tycks vara större idag än när cancerstrategin togs fram. Hur skillnader mellan befolkningsgrupper i överlevnad har utvecklats över tid har vi däremot inte kunnat bedöma inom ramen för det här korta uppdraget.
7.3 De standardiserade vårdförloppen har skapat sammanhållna flöden men behöver utvecklas
De standardiserade vårdförloppen ska bidra till ökad tillgänglighet, patientnöjdhet och jämlikhet. Vår tredje slutsats är att vårdförloppen bedöms ha bidragit till bättre vårdflöden och samarbete, men det finns ett behov av att utvärdera vårdförloppens effekter och se över målen för vårdförloppen.
7.3.1 Vårdförloppen bör utvärderas
De standardiserade vårdförloppen har varit i starkt fokus i den nationella styrningen på cancerområdet under en längre tid. Samtidigt saknas i mycket kunskap om effekterna av vårdförloppen.
Viss positiv effekt på väntetider, men långt till måluppfyllelse
Målet om att 70 procent av alla patienter som insjuknar i cancer ska utredas inom ett standardiserat vårdförlopp är uppnått. Däremot ligger samtliga regioner långt ifrån målet om att 80 av patienterna ska genomgå vårdförloppet inom den satta ledtiden. Vårdförloppen ledde till kortare väntetider för vissa diagnoser, men sammantaget är förbättringen i väntetider liten och varierar stort.
Ökat fokus på primärvårdens roll och sammanhållna flöden lyfts fram som styrkor i SVF
Flera av förslagen i betänkandet från för att skapa mer sammanhållen vård och stärka patienternas ställning har genomförts inom ramen för SVF. Kravet på samarbete och att resultat är beroende av flera aktörer i vårdkedjan, framstår som en utmanande del i SVF i och med vårdens fragmentisering. Samtidigt framstår det också som en punkt där SVF bidragit positivt, genom att ge former för verksamhetsövergripande processarbete. Analyser har pekat på att en viktig del av värdet med SVF är det som berör primärvården, med kriterier för välgrundad misstanke och en standardiserad remitteringsprocess. Den delen i de standardiserade vårdförloppen framstår som särskilt viktig utifrån att primärvårdens roll i att upptäcka cancer tidigt annars är ett område som inte varit i fokus i den nationella styrningen. Samtidigt pekar analyser på att primärvårdens förutsättningar att upptäcka cancer tidigt brister.
7.3.2 Flera aktörer lyfter fram att ledtidsmålen behöver ses över
I både våra intervjuer och i tidigare uppföljningar framkommer ett behov av att se över ledtidsmålen och vilken status de bör ha utifrån medicinska behov och i relation till andra sjukdomsgrupper. Det tycks råda en viss oklarhet om ledtidernas syfte och vilka effekter de kan förväntas ha, eftersom olika aktörer gör olika tolkningar.
Utgångspunkten för de standardiserade vårdförloppen, som det uttrycks i styrdokumenten, är de långa och varierande väntetiderna. Frågan kopplas i första hand till patienters ställning, upplevelser och förtroende för vården. Utgångspunkterna är att en välfungerande vårdkedja är av betydelse för cancervårdens utfall och att väntan kan innebära en stor psykisk belastning på patienter. Därför föreslog utredningen En nationell cancerstrategi att tidsgränser för ledtider skulle definieras och inkluderas i kvalitets- register. De uttalade målen för vårdförloppen handlar om nöjdare patienter genom kortare väntetider, men inte förändrade medicinska utfall. Ledtiderna tas också fram för att minimera väntetiden för patienten oavsett om det finns evidens för medicinska effekter.
Medicinsk förankring av ledtiderna uppfattas dock som viktigt för deras legitimitet. I våra intervjuer och tidigare uppföljningar framkommer kritik mot att en del av ledtiderna inte är medicinskt motiverade, och att de uppfattas som en alltför skarp styrsignal samtidigt som det finns risk för missförstånd. Forskning har exempelvis pekat på att vissa aktörer uppfattar att vårdförloppen kan förväntas ha medicinska effekter, och även i våra intervjuer beskriver flera att det finns missförstånd kring det.
Förutom den medicinska förankringen så finns det också olika syn på om det är positivt eller problematiskt att ledtiderna är satta utifrån ideala förhållanden, utan hänsyn till organisatoriska och resursmässiga avvägningar. Mot bakgrund av bristen på stöd för horisontella prioriteringar finns det risk för att alltför ambitiösa ledtidsmål tränger undan andra grupper eller annat förbättringsarbete.
7.4 Styrkor och svagheter i cancervården för barn och unga
Barncancer ingick inte i den ursprungliga cancerstrategin, men har under senare år tydligare inkluderats i överenskommelserna på cancerområdet genom en särskild satsning. Vår slutsats är att cancervården för barn och unga vuxna bör ingå i en reviderad strategi, men att man bör ta hänsyn till deras särskilda behov.
7.4.1 Barncancer bör ingå i en reviderad cancerstrategi
De aktörer vi intervjuat ser ett behov av att inkludera barncancer i en reviderad cancerstrategi. De menar att barncancer behöver vara en integrerad del i cancerstrategins olika områden, men också särskilt synliggöras för att inte tappa bort barncancerperspektivet. Cancerstrategins mål och fokusområden är över lag relevanta även för barncancerområdet. Exempelvis är frågor som kompetensförsörjning och utvecklingen inom precisionsmedicin minst lika angelägna inom barncancer. Men det finns också skillnader mellan barncancerområdet och vuxenvården, till exempel är prevention inte lika relevant inom barncancer.
7.4.2 Goda medicinska resultat och positiv utveckling inom omhändertagande och uppföljning
Barncancervården har goda medicinska resultat och ligger långt fram inom precisionsmedicin när det gäller att ha infört gensekvensering som klinisk norm. Tillgängligheten är hög och det sker en positiv utveckling i exempelvis tillgång till kontaktsjuksköterska.
Det sker också en positiv utveckling inom uppföljningen av barncancerpatienter, med ett vårdprogram för långtidsuppföljning och utbyggnad av nyckelmottagningar.
Barncancerområdet har dessutom väl utbyggda strukturer för nationell samverkan, där arbetet inom RCC och med nationella handlingsplanen bedöms bidra positivt, och även goda förutsättningar för uppföljning genom kvalitetsregistret.
7.4.3 Utmaningar med läkemedelstillgång, kompetensförsörjning och insatser efter behandling
Även om barncancerområdet ligger långt fram med gensekvensering är tillgången till läkemedel sämre än för vuxna, och det finns svårigheter i barncancerpatienters tillgång till kliniska studier. Utvecklingen inom precisionsmedicin medför också svårigheter med den finansieringsmodell man har idag.
Det finns behov av förbättringar i vården efter behandling utöver vårdprogrammet. Bland annat brister tillgången till palliativ vård och strukturerna för rehabilitering av barncancerpatienter har brister. Övergångarna till vuxenvården är också en svaghet och unga vuxna faller ofta mellan stolarna.
När det gäller strukturella förutsättningar så är kompetensförsörjningen problematisk, i ännu högre grad för barncancer eftersom det är litet område. Att Barncancerfonden i dag finansierar viktiga delar som utbildning av specialistsjuksköterskor och uppföljning är något en reviderad cancerstrategi behöver ta ställning till.
7.5 Medicinteknisk utveckling, EU-initiativ och omställningen till en god och nära vård behöver vägas in i en ny strategi
Vår sista slutsats är att det finns ett antal omvärldsfaktorer som en reviderad cancerstrategi behöver förhålla sig till. De faktorer vi särskilt vill lyfta fram är EU:s initiativ på cancer- området, utvecklingen av precisionsmedicin, de pågående förändringarna i organiseringen av cancervården och genomförandet av omställningen till en god och nära vård.
7.5.1 EU:s initiativ på cancerområdet
På EU-nivå pågår flera initiativ som en reviderad svensk cancerstrategi behöver förhålla sig till.
EU:s cancerplan, som syftar till att stärka cancervården i EU, är i stor utsträckning förenlig med den nuvarande cancerstrategin. Men det finns vissa skillnader. Exempelvis innehåller den konkreta mål, framför allt kopplat till prevention och tidig upptäckt. Dessutom innehåller den initiativ för att stärka samarbetet mellan EU-länderna i frågor som standardisering och delning av hälsodata samt kunskapsspridning. Cancermissionen är ytterligare ett EU-initiativ som främst är inriktat på forskning och innovation.
I arbetet med att revidera cancerstrategin är det viktigt att avgöra hur EU:s cancerplan ska avspeglas i den svenska strategin, till exempel hur en reviderad cancerstrategi ska förhålla sig till målen i EU:s cancerplan. EU:s initiativ på cancerområdet aktualiserar också behov av att avgöra på vilket sätt samarbetet på EU-nivå ska tas tillvara. Mångfalden av EU-nätverk och satsningar skapar behov av samordning bland svenska aktörer, för att kunna tillgodogöra sig möjligheterna. Man behöver också tydliggöra hur styrstrukturen i Sverige ska koppla an till de strukturer som byggs upp på EU-nivå, och hur Sverige ska representeras i olika sammanhang.
Det pågår en utveckling mot en enhetlig struktur för hälsodata på EU-nivå. Det är särskilt aktuellt för cancerområdet, eftersom EU:s cancerplan berör flera sådana initiativ. Utvecklingen på EU-nivå gör frågor om enhetlig struktur för hälsodata inom Sverige ännu mer angelägna.
7.5.2 En cancerstrategi behöver balansera flera olika mål kopplade till den medicinska utvecklingen
Inom cancerområdet pågår en utveckling mot nya avancerade diagnostiska metoder och behandlingsalternativ. De har möjliggjort tidigare upptäckt, ökad överlevnad och bättre livskvalitet för cancerpatienter. Precisionsmedicin medför en ökad träffsäkerhet vid val av behandlingsalternativ, och sjukvården får allt bättre möjligheter att sätta in behandlingar som kan ge god effekt.
Inriktningen i den nationella life science-strategin är att Sverige ska vara ett föregångsland när det gäller att införa precisionsmedicin i vården. Frågan om att stärka forskning och medicinsk utveckling bör vara en central del av den nationella cancer- strategin. Samtidigt behöver en cancerstrategi balansera flera olika mål kopplade till den medicinska utvecklingen. Å ena sidan är det positivt att patienter får tillgång till nya effektiva läkemedel, å andra sidan kan det medföra ökade kostnader och behov av prioriteringar. Ur den enskilda patientens perspektiv kan det vara angeläget att snabbt få tillgång till individuellt anpassade, effektiva och säkra läkemedel, oavsett vad de kostar. Ur ett samhällsekonomiskt perspektiv är det i större utsträckning motiverat att skapa så mycket hälsa som möjligt för hela befolkningen, utifrån de befintliga resurserna. Det innebär att det är nödvändigt att prioritera utifrån de grupper som har störst behov och att säkerställa cancervården inte tränger undan andra behov.
En tidigare introduktion av nya läkemedel kan innebära fördelar ur ett patientperspektiv eftersom en snabbare tillgång kan påverka överlevnaden och livskvaliteten. Ur företagens perspektiv kan tidigt införande också vara av en fördel eftersom kliniska resultat snabbare kan bidra till nya indikationer för ett läkemedel eller till att nya läkemedel kan utvecklas. En tidigare marknadsintroduktion kan även förlänga läkemedlets livscykel och ge möjligheter till företagen att få större intäkter.
Samtidigt kan en allt tidigare introduktion och ett snabbare införande innebära en rad utmaningar. Kunskapen om läkemedlets effekter och biverkningar kan vara begränsade, vilket kan medföra osäkerheter. Begränsade data om läkemedlen och deras effekter kan innebära att beräkningarna av kostnadseffektiviteten blir mindre tillförlitliga. För regionerna kan osäkerheten innebära att de väntar med att införa det nya läkemedlet till dess att kunskapen om läkemedlets effekt är större. En nationell process som styr mot snabbare införande av nya läkemedel kräver också att regionerna har processer och kapacitet att följa de nationella rekommendationerna. En utmaning ligger alltså i att hitta en balans mellan en snabb tillgång till läkemedel och andra värden, till exempel hög säkerhet och effektivitet samt möjligheter för regionerna att planera.
Utvecklingen av precisionsmedicin kommer även innebära flera utmaningar kopplade till exempelvis finansiering, införande och uppföljning. Det kommer finnas behov av att utveckla vårdens infrastruktur, till exempel diagnostik, it-system samt kompetens- och personalförsörjning. En utvecklad uppföljning anser vi utgör en nyckelfråga för att säkerställa att patienter får tillgång till kostnadseffektiva behandlingar. Vi ser att en cancerstrategi både behöver balansera mellan olika mål och stötta utvecklingen av en infrastruktur för precisionsmedicin och nya avancerade behandlingar.
7.5.3 Förändringar i organiseringen av cancervården
I det material vi samlat in lyfts framför allt två områden fram när det gäller organiseringen av de övergripande strukturerna för cancervården – relationen mellan RCC och CCC samt RCC och CCC i förhållande till statliga myndigheter.
Framväxten av CCC parallellt med RCC-strukturen skapar utmaningar. Från ett systemperspektiv lyfter flera aktörer fram att det ett behov av att från statlig nivå tydliggöra vilka roller RCC och CCC ska ha och hur de ska förhålla sig till varandra.
Det är viktigt bland annat för att undvika dubbelarbete och konflikterande styrsignaler samt ta tillvara respektive aktörs styrkor när det gäller att skapa förutsättningar för implementering och samverkan. Behovet av att skapa tydliga roller förstärks ytterligare av utvecklingen inom cancer på EU-nivå. Det behöver klargöras vilken eller vilka aktörer som ska representera Sverige i EU-sammanhang och hur Sverige kan spegla EU:s organisation på cancerområdet.
7.5.4 Omställningen till en god och nära vård
Den ökade medicinska kvaliteten och minskade dödligheten i cancersjukdomar har över tid medfört en förskjutning av cancervården mot ett behov av att hantera långsiktiga, och ibland kroniska tillstånd. Då blir behovet av till exempel långsiktig rehabilitering, kontinuitet i vården och stöd till att samordna insatser från olika aktörer mer framträdande. Det stämmer väl överens med de utgångspunkter som regeringen angett för omställningen till en god och nära vård, till exempel behovet av att stödja vid långvariga, kroniska och komplexa tillstånd.
Vår analys visar att det inom ramen för cancerstrategin har varit jämförelsevis svårt att arbeta med de frågor som är bredare än den specialiserade cancervården och som kräver samverkan med aktörer utanför specialistvården, till exempel prevention och rehabilitering. Enligt vår analys är det ofta oklart vem som har ansvaret för de här frågorna och i våra intervjuer lyfter flera fram brister inom dessa områden.
Sett till primärvårdens nya lagreglerade grunduppdrag ser vi att primärvården borde ta ett ansvar när det gäller områden som prevention, rehabilitering och samordning. Vår utvärdering av omställningen till en god och nära vård visar dock att primärvården ännu har svaga förutsättningar att ta det ansvaret och att det finns brister i samverkan med både specialiserad vård och den kommunala hälso- och sjukvården. Vår kartläggning av cancerstrategins implementering visar också att det inom dessa breda områden skapats egna specialiserade cancerspecifika strukturer – till exempel särskilda cancer- rehabiliteringscentrum, eller att resultaten är bättre för cancerpatienter inom palliativ vård, trots att den typen av insatser är eller borde vara likartade för många grupper av patienter.
Mot den bakgrunden blir det viktigt i arbetet med en ny cancerstrategi att upp- märksamma vilken roll primärvården ska ha i cancervården och hur den pågående omställningen till en god och nära vård kan påverka det. Även den kommunala hälso- och sjukvården kan förväntas få en allt större roll i vården av cancerpatienter, till exempel när det gäller långsiktig rehabilitering och palliativ vård. Det bör också uppmärksammas i en ny cancerstrategi.
Det är på motsvarande sätt också viktigt att regioner och kommuner, i genomförandet av omställningen till en god och nära vård, beaktar hur hälso- och sjukvården som helhet ska struktureras och planeras på kort och lång sikt. En fråga i det sammanhanget är vilka uppgifter det är rimligt att primärvården och den kommunala hälso- och sjukvården ska klara av, och om resurserna motsvarar uppdraget.
7.6 Medskick till arbetet med att revidera cancerstrategin
I vårt uppdrag ingår inte att lämna förslag till innehållet i en ny strategi men vi bedömer att våra slutsatser ändå ger vägledning om behovet av förändringar av strategin. Med utgångspunkt i vår analys av cancerstrategin och slutsatserna har vi identifierat tre områden som vi anser bör adresseras i arbetet med en reviderad cancerstrategi. Inom ramen för varje övergripande område finns ett antal delfrågor som närmare kan behöva övervägas i arbetet med att revidera strategin. Inom respektive område redovisar vi även medskick från alla de experter vi intervjuat och träffat på möten samt deltagare på vårt resultatseminarium.
7.6.1 En cancerstrategi som tar ett bredare grepp
Ett första övergripande medskick är att regeringen bör överväga om cancerstrategin ska utformas så att den tar ett bredare grepp. I vår analys av andra länders cancerstrategier, EU:s cancerplan och våra intervjuer framkommer att vissa aspekter skulle kunna ingå i cancerstrategin på ett tydligare sätt. Det handlar om att strategin kan omfatta alla åldrar, fler dimensioner av jämlikhet och tydligt belysa hela vårdkedjan. Flera uttrycker också ett behov av att tydliggöra att cancer är en av flera diagnoser som hälso- och sjukvården behöver förhålla sig till och att vården av cancerpatienter i stor utsträckning sker i verksamheter som ägnar sig åt fler patienter än cancerpatienter.
En cancerstrategi som på ett tydligare sätt belyser hela vårdkedjan
Överlevnaden i cancer har i många fall ökat. Det gör cancer till mer av en kronisk sjukdom, där livskvalitet, långsiktig rehabilitering och palliativ vård efter den akuta behandlingen blir mer framträdande. Mot den bakgrunden menar flera av våra intervjupersoner att det finns anledning att tydligare lyfta fram livskvalitet bland målen för att synliggöra delarna i vårdkedjan som sker efter behandling. Ett annat förslag är att standardiserade vårdförlopp även bör innefatta det som sker efter behandling, oavsett om det är rehabilitering eller palliativ vård.
Några intervjupersoner har också haft medskick kring hur palliativ vård och rehabilitering bättre kan integreras i vårdkedjan och tillgodoses på ett mer personcentrerat sätt. Det handlar till exempel om att skapa strukturer för de patienter som inte passar i dagens olika vårdförlopp, särskilt multisjuka patienter, och att individanpassa behandlingar. Representanter för rehabilitering och palliativ vård betonar också att det är viktigt att dessa delar av vårdkedjan inleds tidigare. Exempelvis bör inte rehabilitering ses som något som ska komma efter behandling, utan det finns stort värde i att inleda rehabiliteringsinsatserna redan före behandling. Även palliativ kompetens kan vara viktigt som förhållningssätt i tidigare skeden av vårdkedjan än i livet slutskede.
I vår undersökning har vi inte fördjupat oss i närståendeperspektivet och det har inte heller lyfts fram som ett utvecklingsområde i våra intervjuer, men under vårt resultatseminarium ansåg flera att närståendeperspektiv bör framgå tydligare i strategin. Utredningen om ett stärkt stöd till anhöriga till långvarigt eller allvarligt sjuka (Dir. 2023:77) kan förväntas ge viktiga medskick till strategin.
En cancerstrategi som uttalat omfattar cancervården av barn och unga vuxna
Ett medskick från flera intervjupersoner är att inkludera barn i strategin, bland annat eftersom det inte är hållbart att bygga parallella strukturer. Det finns också en risk för att barn ”glöms bort” i de strukturer som byggs upp, till exempel rehabiliteringscenter. Gruppen unga vuxna behöver också uppmärksammas i strategin utifrån de särskilda utmaningar som uppstår vid övergången från att vara barn till vuxen i vården och i kontakter med andra samhällsinstanser. Gruppen unga vuxna behöver definieras på ett tydligt sätt, till exempel med inspiration från EU:s cancerplan.
En synpunkt som kommit fram i våra intervjuer är att om en reviderad strategi innefattar barncancer, så bör målen formuleras så att det tydligt framgår att strategin omfattar alla åldrar.
Bredare grepp om jämlikhet
Minskade regionala skillnader i överlevnad är ett av cancerstrategins fem mål. Sedan cancerstrategin togs fram har det blivit ett större fokus på regionala skillnader i den politiska debatten, men även i insatserna inom cancerstrategin. Ett medskick är att överväga att omformulera målet om regionala skillnader till att fokusera på fler områden än överlevnad, exempelvis livskvalitet, insjuknande och omhändertagande. Men det handlar också om att adressera regionala skillnader i väntetider, kvalitet, prevention och screening. Vårt intryck är till exempel att kunskapen om hur det preventiva arbetet kan utformas för att bli mer träffsäkert gentemot de grupper som löper störst risk att drabbas av ohälsa har ökat sedan cancerstrategin togs fram. Ett medskick till det fortsatta arbetet är att ta ställning till hur den kunskap som finns kan omsättas i cancerstrategin. Enligt RCC pågår ett arbete med hälsoinformatörer i utsatta områden i några regioner. Det är ett exempel på arbete som kan generera kunskap om möjliga arbetssätt.
Andra synpunkter som lyfts i våra intervjuer och möten är att jämlik vård behöver definieras och att det behövs både tydligare mål och uppföljning när det gäller jämlikhet.
Det behöver tydliggöras att cancervården är en del av hälso- och sjukvården
Flera intervjupersoner och andra informanter har lyft fram att cancerstrategin kan bidra till att det uppstår parallella strukturer för cancer och vården i övrigt. Det kan till exempel handla om att insatser och utveckling inom den palliativa vården, prevention som rör ohälsosamma levnadsvanor eller rehabilitering sker separat för cancerområdet även när det inte finns ett sådant behov av specialisering. De menar att det kan finnas ett behov av ett större helhetsperspektiv, där cancer ingår som en del av hälso- och sjukvården i stort. Vissa menar att det behövs ställningstaganden om ifall breda frågor som prevention och palliativ vård bör ingå i en diagnosspecifik strategi eller hanteras på något annat sätt. Man pekar på svårigheten att inom ramen för en cancerstrategi ta sig an frågor som levnadsvanor i befolkningen och att det kan vara önskvärt med en smalare strategi fokuserad på några särskilt prioriterade områden. Andra menar att en cancerstrategi kan fungera som hävstång för vården i övrigt även i de mer övergripande frågorna.
I andra länder finns både exempel på strategier som i likhet med den svenska formulerar breda mål, och på exempelvis den danska cancerplanen från 2016 som har valt att lyfta ett fåtal, mer detaljerade mål inom särskilt viktiga områden.
Oavsett vilken linje som förespråkas – att breda områden inte ingår i cancerstrategin eller att cancervården ska fungera som föredöme för hälso- och sjukvården i övrigt – är många överens om att det behöver tydliggöras hur kunskapsöverföringen från cancervården till övrig vård ska ske. Till exempel behöver man fastställa strukturer och former för hur de kunskaper som genereras i cancervården ska tas tillvara i hälso- och sjukvården i stort.
Ett ytterligare medskick är att det är viktigt att tydliggöra varför det behövs en cancerstrategi. Enligt vissa intervjupersoner och andra informanter är det en vård som fungerar relativt väl, och som därmed eventuellt inte behöver hanteras i en särskild strategi.
7.6.2 Ett ökat genomslag för cancerstrategin
Ett andra övergripande område för medskick är insatser för att öka cancerstrategins genomslag i vården. Vi bedömer att det finns flera möjligheter att öka genomslaget. En viktig orsak till ojämn implementering är enligt flera intervjupersoner och andra informanter att den nationella styrningen är otydlig på övergripande nivå, med otydliga prioriteringar och bristande operationalisering av strategin. Flera intervjupersoner betonar att det är viktigt att cancerstrategin innehåller eller kompletteras med stöd för horisontella prioriteringar och att det finns en aktör med ansvar för det. Många lyfter även fram att styrningen behöver anpassas till regionala förutsättningar – det som ska göras måste också vara genomförbart – och att regionerna behöver finnas med på ett tydligare sätt i strategin. I dagsläget finns det en osäkerhet bland flera aktörer om regionerna står bakom strategin.
Stödet för prioriteringar kan förbättras
De flesta aktörer vi har intervjuat anser att prioriteringarna inom cancerstrategin och gentemot andra patientgrupper är avgörande för genomslaget av cancerstrategin. Mot bakgrund av utvecklingen inom precisionsmedicin och regeringens mål för life science-strategin blir prioriteringar särskilt viktiga.
När det gäller prioriteringar inom cancerstrategin ser vi att det behöver finnas tydligare stöd för prioriteringar mellan målområden, insatser och patientgrupper. Vissa menar att strategin behöver ett hållbarhetsperspektiv och att den bör bidra till att resurseffektivt hushålla med samhällets resurser. Andra menar att strategins viktigaste bidrag är underlag för att göra kloka kliniska val och prioriteringar.
När det gäller prioriteringar gentemot andra patientgrupper lyfter flera intervjupersoner fram frånvaron av nationellt stöd för horisontella prioriteringar som omfattar cancer. Ett medskick är att se över vilka behov av horisontella prioriteringar som finns kopplade till cancerområdet och att även överväga om Socialstyrelsen bör inkludera cancer i sina nationella riktlinjer igen.
Operationalisering av strategin
Några aktörer har föreslagit att cancerstrategin fortsatt bör fungera som ett sammanhållande paraply med övergripande och långsiktig inriktning för cancervården, men att strategin bör kompletteras med någon form av mer kortsiktiga ”delstrategier” eller handlingsplaner som revideras med tätare tidsintervall. De skulle kunna riktas in på exempelvis de mål som är högst prioriterade eller insatser som bedöms som särskilt relevanta vid en viss tidpunkt. De skulle också kunna innehålla mer konkreta och tidsatta mål.
En synpunkt som framförts är att betänkandet, som den nuvarande cancerstrategin baseras på, växlar mellan nivåer och går ända ner på operativa frågor i vissa fall. I stället menar vissa att en strategi behöver hålla höjd och inte gå in på till exempel olika diagnoser. Om cancerstrategin operationaliseras i handlingsplaner eller uppdateringar behöver det även klargöras vilken aktör som ansvarar för det, liksom för uppföljningen som de bör baseras på.
7.6.3 En cancerstrategi med tydligare roller och mandat
Ett sista övergripande medskick är att roller och mandat i cancerstrategin behöver bli tydligare. Som vi konstaterat i slutsatserna (se avsnitt 7.1.2) har otydliga mandat i vissa fall inneburit hinder för genomförandet av cancerstrategin. Strategin kan behöva en tydligare formell förankring, det vill säga att det tydliggörs vilka aktörer som står bakom strategin, vilka aktörer som ansvarar för genomförande av insatserna och finansiering i strategins olika delar. I dagsläget saknas även strukturer för att tillgodose behovet av horisontella prioriteringar i kunskapsstyrningen inom cancervården. Mot bakgrund av omvärldsfaktorer som det ökade EU-samarbetet, framväxten av CCC och omställningen till god och nära vård blir tydliga roller och mandat ännu viktigare.
Tydliggörande av roller
Som vi lyft fram i slutsatserna efterlyser flera aktörer ett ställningstagande om rollfördelningen mellan RCC och CCC. Olika aktörer har olika uppfattningar om vilka roller de bör ha. Vi kan urskilja två huvudlinjer: Den ena innebär att RCC bör ansvara för kunskapsstöd och vidareutbildning medan CCC:erna bör ansvara för mer specialiserad vård och forskning. Den andra innebär att RCC bör inordnas under CCC eller främst stötta CCC.
Flera menar att det är viktigt att ta tillvara de samverkansstrukturer, processer och arbetssätt som RCC upparbetat. Någon lyfter också fram att det kan finnas en övertro till att bygga nya strukturer. Samtidigt uppfattas det bland vissa att det finns ett alltför stort avstånd mellan RCC och vården och att processen för framtagande av vårdprogram blivit omständlig, vilket leder till att andra aktörer börjar ta fram egna dokument.
Även utvecklingen inom EU medför ett behov av att tydliggöra rollerna inom cancervården. Än så länge är det inte fullständigt tydligt vilka behov EU:s initiativ på cancerområdet kommer att medföra och inte heller hur regeringen och riksdagen avser att förhålla sig till EU:s initiativ. Utifrån utgångpunkten att Sverige kommer att delta helt och hållet är ett medskick från några intervjupersoner att det är angeläget att en reviderad cancerstrategi beaktar hur Sverige tar hand om, förvaltar och vidareutvecklar EU:s satsningar. Ett exempel på det är att stärka kopplingen mellan utlysningen av medel samt initiativ inom EU:s cancerplan och de årliga överenskommelserna mellan staten och SKR.
Behov av starkare förankring av strategin i regioner och kommuner
Vi har inte haft möjlighet att fullt ut undersöka cancerstrategin ur regionernas och verksamheternas perspektiv. Vi har inte analyserat de regionala handlingsplanerna eller intervjuat några representanter för regioner och kommuner på högre ledningsnivå. Det arbete och den samverkan som sker mellan framför allt RCC och dessa aktörer kan vi därför inte dra några slutsatser om. Det är också otydligt för flera av de aktörer vi talat med om strategin har stöd på regional nivå. De perspektiven bör undersökas vidare för att cancerstrategin ska kunna utformas så att den blir ett träffsäkert styrmedel som förmedlar rimliga förväntningar. Vi har i tidigare rapporter pekat på att staten med en stärkt dialog och involvering av regioner och kommuner kan skapa bättre förutsättningar för att belysa handlingsalternativ och hur statens styrning kan harmoniera med eller komplettera huvudmännens insatser (se till exempel Vård- och omsorgsanalys 2022).
Behov av nationell eller statlig styrning i vissa fall
I våra intervjuer nämner många respondenter de regionala skillnaderna och efterfrågar en ökad nationell styrning eller samordning på cancerområdet i syfte att öka jämlikheten. Det gäller det man uppfattar som statens generella ansvar för en jämlik vård och hälsa där både mål och uppföljningen av måluppfyllelse anses behöva vara ett statligt ansvar. Det decentraliserade sjukvårdssystemet innebär olika förutsättningar och prioriteringar och staten skulle kunna bidra till att utjämna de skillnaderna. I någon intervju nämns vidare att det uppstår många parallella processer i regionerna som borde kunna skötas mer samlat.
I flera intervjuer framkommer också en önskan om ett ökat statligt ansvarstagande eller ett tydligare formulerat uppdrag för någon aktör på en rad delområden som rör cancervården. Det gäller särskilt områden som uppfattas som svaga eller att utvecklingen där har gått långsamt, till exempel prevention, screening, rehabilitering, palliativ vård och fortbildning. Ett annat medskick vi tagit emot är att det behövs ökad nationell styrning på läkemedelsområdet mot bakgrund av ojämlik tillgång.
Referenser
Abuhasanein, S. m.fl. (2022). Standardized care pathways for patients with suspected urinary bladder cancer: the Swedish experience. Scandinavian Journal of Urology, 56:3 Adami H, Kalager M, Bretthauer M. (2023). The Future of Cancer Screening—Guided
Without Conflicts of Interest. JAMA Intern Med. 2023;183(10):1047–1048.
Andersson, E. Nyhlin, N., van Nieuwenhoven, M.A. (2021). The effectiveness of the colorectal cancer referral pathway – identification of colorectal cancer in a Swedish region. Scandinavian Journal of Gastroenterology, 56:5, 552–558.
Backman, C. Johansson, U. och Hellgren, M. (2021). Knowledge of and support for cancer patient pathways among general practitioners and other physicians – a study from Sweden. Scandinavian Journal of Primary Health Care, 39:1, 17–22.
Bretthauer M, Wieszczy P, Løberg M, m.fl.. (2023). Estimated Lifetime Gained With Cancer Screening Tests: A Meta-Analysis of Randomized Clinical Trials. JAMA Intern Med. 2023;183(11):1196–1203.
Campbell SM, Braspenning J, Hutchinson A, Marshall MN. (2002). Research methods used in developing and applying quality indicators in primary care. Quality & safety in health care, 11(4), ss. 358–364.
Cancerfonden. (2019). Cancerfondsrapporten – prevention. Stockholm: Cancerfonden. Cancerfonden. (2020). Cancerfondsrapporten – cancervård. Stockholm: Cancerfonden. Cancerfonden. (2021). Segregerad screening. Stockholm: Cancerfonden.
Cancerfonden. (2023). Cancerfondsrapporten – forskning. Stockholm: Cancerfonden. Cancerfonden. (u.å). Lättare val för folkhälsan – Resultaten. Stockholm: Cancerfonden.
Cancerfonden och Bröstcancerförbundet. (2021). Lika olika överallt. En kartläggning av tillgängligheten till rehabilitering för bröstcancerpatienter.
Cancerfonden, RCC i samverkan, Dieternas riksförbund, Riksförbundet HOBS. (2020). Prevention i primärvården – Novusrapport. Stockholm: Cancerfonden.
Danckert, B. (2021). Monitoring Standardized Cancer Pathways. Köpenhamn: Danish Cancer Society
Delilovic m.fl. (2019). Implementing standardized cancer patient pathways (CPPs) – a qualitative study exploring the perspectives of health care professionals. BMC Health Services Research.
Delilovic, S., Andersson, F. och Hasson, H. (2020). Standardiserade vårdförlopp inom cancervården – analys av undanträngningseffekter. Faktablad 2020:1, Stockholm: Centrum för epidemiologi och samhällsmedicin
Department of Health and Social Care. (2023a). Government Action on Major Conditions and Diseases. Statement made on 24 January 2023. https://questions-statements. parliament.uk/written-statements/detail/2023-01-24/hcws514 [hämtat 2023-12-21]
Department of Health and Social Care. (2023b). Call for evidence outcome. 10-Year Cancer Plan: call for evidence. https://www.gov.uk/government/calls-for-evidence/10-year- cancer-plan-call-for-evidence [hämtat 2024-01-15].
Doran, G. T. (1981). ”There’s a S.M.A.R.T. way to write management’s goals and objectives”. Management Review. 70 (11): 35–36
Europeiska kommissionen. (2022). Förslag till Europaparlamentets och rådets förordning om ett europeiskt hälsodataområde. COM(2022) 197 final. https://eur-lex.europa.eu/ legal-content/EN/TXT/?uri=COM:2022:197:FIN [hämtat 2023-12-21]
Europeiska kommissionen. (2020a). Conquering cancer: Mission possible. Report of the Mission Board for Cancer. Independent expert report. Bryssel: Europeiska kommissionen.
Europeiska kommissionen. (2020b). Knowledge Center on Cancer – infographic flyer. https://knowledge4policy.ec.europa.eu/cancer/about_en, https://joint-research-centre. ec.europa.eu/jrc-news-and-updates/commission-launches-knowledge-centre-fight- cancer-2021-06-30_en [hämtat 2023-12-21].
Europeiska kommissionen. (2021a). Europas plan mot cancer.
Europeiska kommissionen. (2021b). Mission on cancer. Implementation Plan. https:// research-and-innovation.ec.europa.eu/funding/funding-opportunities/funding- programmes-and-open-calls/horizon-europe/eu-missions-horizon-europe/eu-mission- cancer_en. [hämtat 2021-12-21].
Europeiska kommissionen. (2023a). Horizon Europe Work Programme 2023–2024: Missions, Mission on Cancer Implementation Plan, Horizon Europe Budget. https:// ec.europa.eu/info/funding-tenders/opportunities/docs/2021-2027/horizon/wp- call/2023-2024/wp-12-missions_horizon-2023-2024_en.pdf [hämtat 2023-12-21]
Europeiska kommissionen. (2023b). Genomförandet av EU:s förordning om utvärdering av medicinsk teknik. https: /health.ec.europa.eu/system/files/2023-09/hta_regulation- implementation_factsheet_sv.pdf [hämtat 2024-01-19].
Europeiska kommissionen. (u.å.a). European health data space. Factsheet. https://ec.europa. eu/commission/presscorner/detail/en/fs_22_2713 [hämtat 2023-12-21].
Europeiska kommissionen. (u.å.b). ECIR – European Cancer Inequalities Registry. https:// cancer-inequalities.jrc.ec.europa.eu/ [hämtat 2023-12-21].
Europeiska kommissionen. (u.å.c). EU4Health programme 2021-2027 – a vision for a healthier European Union. https://health.ec.europa.eu/funding/eu4health-programme- 2021-2027-vision-healthier-european-union_en [hämtat 2023-12-21].
Fjällström, P. m.fl. (2023). Reduction in the diagnostic interval after the introduction of cancer patient pathways for colorectal cancer in northern Sweden. Scandinavian Journal of Primary Health Care, 41:3.
Helse- og omsorgsdepartementet. (2018). Nasjonal kreftstrategi (2018–2022) Leve med kreft. Oslo: Helse- og omsorgsdepartementet
Independent Cancer Taskforce. (2015). Achieving World Class Cancer Outcomes: a strategy for England 2015-2020.
Institut national du cancer. (2021). Stratégie décennale de lutte contre les cancers.
Innovative partnership for action against cancer. (2021). Joint Action on network of Comprehensive Cancer Centres JA Crane. Preparatory activities on creation of National Comprehensive Cancer Centres and EU Networking. (EU4H-2021-JA-03). https: /health.ec.europa.eu/system/files/2021-12/ev_20211126_co03_en.pdf [hämtat 2024-01-04].
Institutet för Hälso- och Sjukvårdsekonomi (IHE). (2021). Deltagande i de nationella screeningprogrammen för cancer i Sverige – Kan geografiska skillnader i deltagargrad kopplas till socioekonomisk ojämlikhet och hur många liv hade kunnat räddas vid ett mer jämlikt deltagande? Konsultrapport. Lund: IHE.
Gralén. K. (2022). Tidigare upptäckt av lungcancer i primärvården – en intervjustudie med primärvårdsläkare. IHE Rapport 2022:9, IHE: Lund.
Ledningsgruppen för svenska palliativregistret. (2022). Årsrapport för svenska palliativregistet 2022.
Latham, G. P., & Locke, E. A. (2006). Enhancing the Benefits and Overcoming the Pitfalls of Goal Setting. Organizational Dynamics, 35(4), 332–340.
Ledningsgruppen för svenska palliativregistret. (2022). Årsrapport för svenska palliativregistet 2022.
Lif (2023). Uppföljning av cancerläkemedel brister. https://www.life-time.se/vardkvalitet/ uppfoljning-av-cancerlakemedel-brister/ [hämtat 2023-12-19].
Läkemedelsverket. (2015). SAMverkan Myndigheter och Sjukvård. Uppsala: Läkemedelsverket.
Nationella kvalitetsregister. (2021). Patientrapporterade mått – insamling och ansvar. Stockholm: Nationella kvalitetsregister.
Nationella vårdkompetensrådet. (2021). Statistikbaserade flödesbeskrivningar för yrkesgruppen biomedicinska analytiker. Stockholm: Nationella vårdkompetensrådet
NHS England. (2019). The NHS Long Term Plan 2019–2028.
OECI. (2023). What is OECI. https://www.oeci.eu/ [hämtat 2023-12-21]
Petersen C, Óskarsson T, Jarfelt M, Hjorth L. (2023). Long-term follow up after childhood cancer – during childhood and adult life. Läkartidningen. 2023;120.
RCC i samverkan. (2023). Statistik om cancervård. [hämtat 2022-06-15]. https:// cancercentrum.se/samverkan/vara-uppdrag/statistik/.
RCC i samverkan. (2016a). Långtidsuppföljning efter barncancer. Nationellt vårdprogram. Version 3.0. 2022-02-22.
RCC i samverkan. (2016b). Utvärdering av de nationella vårdprogrammen inom cancervården.
RCC i samverkan. (2018). Peniscancer – en rapport kring nivåstrukturering.
RCC i samverkan. (2019). Utvecklingsområden inom barncancer analys och förslag till fortsatt arbete.
RCC i samverkan. (2020a). Nationell cancerpreventionsplan 2020–2022.
RCC i samverkan. (2020b). Kortare väntetider i cancervården slutrapport 2020.
RCC i samverkan. (2020c). Styrdokument: Riktlinjer för framtagande av standardiserade vårdförlopp inom cancersjukvården. Version 2.0 2020-03-25.
RCC i samverkan. (2020d). Handlingsplan utvecklingsområden inom barncancervården.
RCC i samverkan. (2020e). Uppföljning av nationellt nivåstrukturerade verksamheter inom cancervården. Sammanställning och bedömning av verksamheternas 2- och 4-årsuppföljningar.
RCC i samverkan. (2021a). Jämlik och effektiv cancervård – delrapport.
RCC i samverkan. (2021b). Jämlik och effektiv cancervård – slutrapport.
RCC i samverkan. (2021c). Utveckling av uppföljningen av vårdprogram och kvalitet genom kvalitetsregister. Rekommendationer på vägar framåt.
RCC i samverkan. (2022a). Kompetensförsörjningsläget inom barncancervarden. RCC i samverkan. (2022b). Utvecklingsområden inom barncancer –årsrapport 2022. RCC i samverkan. (2022c). Utvecklingsområden inom barncancer. Delrapport 2022.
RCC i samverkan. (2022d). Utvärdering av nationella vårdprogrammet. Långtidsuppföljning efter barncancer.
RCC i samverkan. (2022e). Provtagning för tidig upptäckt av tjock- och ändtarmscancer. [uppdaterad 2022-10-31]. https://cancercentrum.se/samverkan/vara-uppdrag/ prevention-och-tidig-upptackt/screening-tjock-och-andtarmscancer/.
RCC i samverkan. (2022f). Användning av nya cancerläkemedel. Redovisning gällande ett urval av cancerläkemedel med registrerad insättning 1 januari – 31 december 2022. RCC i samverkan. (2023a). Patient och närstående. https://cancercentrum.se/samverkan/ patient-och-narstaende/patientsamverkan/patient–och-narstaendeforetradare/ [hämtat 2023-12-21]
RCC i samverkan. (2023b). Att bli ett ackrediterat Comprehensive Cancer Centre. https:// cancercentrum.se/samverkan/vara-uppdrag/ledning-och-styrning/comprehensive- cancer-centre/ [hämtat 2023-12-21]
RCC i samverkan. (2023c). Nationell Min vårdplan bröstcancer. https://cancercentrum. se/samverkan/cancerdiagnoser/brost/min-vardplan/ [hämtat 2023-11-01]
RCC i samverkan. (2023d). Vägen framåt.
RCC i samverkan. (2023e). Palliativ vård. https://cancercentrum.se/samverkan/vara- uppdrag/palliativ-vard/ [hämtat 2023-12-21].
RCC i samverkan. (2023f). Patientrapporterade mått, PROM och PREM. https:// cancercentrum.se/samverkan/vara-uppdrag/kunskapsstyrning/patientrapporterade- matt [hämtat 2023-12-21].
RCC i samverkan. (2023g). Att bli ett ackrediterat Comprehensive Cancer Centre. https:// cancercentrum.se/samverkan/vara-uppdrag/ledning-och-styrning/comprehensive- cancer-centre/fordelar-med-ackreditering/.
RCC i samverkan. (2023h). Nivåstrukturering inom cancervården. https://cancercentrum. se/samverkan/vara-uppdrag/kunskapsstyrning/nivastrukturering/ [hämtat 2023-12-21].
RCC i samverkan. (2023i). Kontaktsjuksköterska. [updaterad 2023-10-11]. https:// cancercentrum.se/samverkan/patient-och-narstaende/kontaktsjukskoterska/ [hämtat 2024-01-04].
RCC i samverkan. (2023j). Nationella vårdprogram cancer. https://cancercentrum.se/ samverkan/vara-uppdrag/kunskapsstyrning/vardprogram/ [hämtat 2024-01-04].
RCC i samverkan. (2023k). Nationella vårdprogram. Kunskapsbanken. https:// kunskapsbanken.cancercentrum.se/vardprogram/ [hämtat 2024-01-04].
RCC i samverkan (2023l). Patienternas upplevelser av standardiserade vårdförlopp (SVF). [updaterad 2022-05-13]. https://cancercentrum.se/samverkan/vara-uppdrag/statistik/ svf-statistik/patienternas-upplevelser/.
RCC i samverkan. (2023m). Nationell cancerpreventionsplan 2024–2030. https:// cancercentrum.se/globalassets/vara-uppdrag/prevention-tidig-upptackt/prevention/ vast/nationell-cancerpreventionsplan-2024-2030.pdf [hämtat 2024-01-04].
RCC Stockholm Gotland. (2019). Patientrapporterade erfarenhetsmått i uppföljningen av standardiserade vårdförlopp.
Regeringen. (2011). Nationell läkemedelsstrategi för framtiden. Stockholm: Regeringen. Regeringen. (2018). Långsiktig inriktning för det nationella arbetet med cancervården. Stockholm: Regeringen.
Regeringen. (2023a). S2023/02108 (delvis) Uppdrag att ta fram ett förslag till färdplan för genomförandet av en nationell digital infrastruktur för hälso- och sjukvården. Stockholm: Socialdepartementet.
Regeringen. (2023b). S2023/02109 (delvis) Uppdrag att utreda förutsättningarna för utveckling av en nationell teknisk lösning som möjliggör automatisk informationsöverföring till nationella kvalitetsregister. Stockholm: Socialdepartementet.
Regeringen. (2023c). S2023/00256 (delvis) Uppdrag att ta fram förslag till en nationell plan för hälso- och sjukvårdens kompetensförsörjning. Stockholm: Socialdepartementet.
Regeringen Danmark. (2016). Kræftplan IV, Patienternes Kræftplan.
Regionernas samverkansmodell för läkemedel. (2023a). Ordnat införande. Samverkans- modellen – Janusinfo.se [hämtat 2023-12-15].
Regionernas samverkansmodell för läkemedel. (2023b). Presentation Cancerdagen 4 oktober 2023, Kenneth Villman, ordförande NAC. Stockholm: Regionernas samverkansmodell för läkemedel.
Regionernas samverkansmodell för medicinteknik. (2023). Ordnat införande. Samverkansmodellen – Janusinfo.se [hämtat 2023-12-19].
Riksrevisionen. (2023). I väntan på vård – ineffektiv statlig styrning för kortare köer. RiR 2023:12. Stockholm: Riksrevisionen.
Scottish Government. (2016). Beating Cancer: Ambition and Action.
SKL. (2013a). Ännu bättre cancervård – delrapport 8 Kontaktsjuksköterskor. Stockholm: SKL.
SKL. (2013b). Ännu bättre cancervård – delrapport 1 Försöksverksamheten – mer patientfokuserad och sammanhållen cancervård. Stockholm: SKL.
SKL. (2013c). Ännu bättre cancervård – delrapport 9 Nya cancerläkemedel. Stockholm: SKL.
SKL. (2013d). Ännu bättre cancervård – delrapport 6 Patientrapporterade mått. Stockholm: SKL.
SKL. (2013e). Ännu bättre cancervård – delraport 10 Individuella vårdplaner inom cancervården. Stockholm: SKL.
SKR. (2016a). Barncancervården – Översyn av kompetensförsörjningen inom barncancer- vården på kort och lång sikt. Stockholm: SKL.
SKR. (2021a). Kartläggning av RCC i samverkans verksamhet. Stockholm: SKR.
SKR. (2021b). Generisk modell för rehabilitering. Nationellt system för kunskapsstyrning.
SKR. (2023). Jämlik och effektiv cancervård med kortare väntetider. Stockholm: SKR. Socialdepartementet. (2011). Kriterier som ska utmärka ett regionalt cancercentrum (RCC). Promemoria. Stockholm: Socialdepartementet.
Socialdepartementet. (2014). Uppdrag att utveckla uppföljningen av hälso- och sjukvårdens tillgänglighet. S2014/4157/FS. Stockholm: Socialdepartementet.
Socialdepartementet. (2020). Uppdrag om utveckling av den statligt nationella samordningen och uppföljningen av cancervården. S2020/09801. Stockholm: Socialdepartementet.
Socialdepartementet. (2023). Uppdrag att kartlägga cancerrehabiliteringen.
Regeringsbeslut. S2023/02344 (delvis). Stockholm: Socialdepartementet.
Socialdepartementet och SKL. (2010). Överenskommelse om utvecklingsarbete inom ramen för cancerstrategin år 2010. Överenskommelse mellan staten och Sveriges Kommuner och Landsting.
Socialdepartementet och SKL. (2011). Ännu bättre cancervård. Överenskommelse mellan staten och Sveriges Kommuner och Landsting om insatser inom ramen för den nationella cancerstrategin.
Socialdepartementet och SKL. (2012). Ännu bättre cancervård 2012 – överenskommelse mellan staten och Sveriges Kommuner och Landsting om insatser inom ramen för den nationella cancerstrategin.
Socialdepartementet och SKL. (2013). Överenskommelse om vissa utvecklingsområden inom hälso- och sjukvården 2013 – överenskommelse mellan staten och Sveriges Kommuner och Landsting.
Socialdepartementet och SKL. (2014). Överenskommelse om kunskapsstyrning och vissa utvecklingsområden inom hälso- och sjukvården 2014 överenskommelse mellan staten och Sveriges Kommuner och Landsting.
Socialdepartementet och SKL. (2015). Kortare väntetider i cancervården. Överenskommelse mellan staten och Sveriges Kommuner och Landsting 2015.
Socialdepartementet och SKL. (2016). Kortare väntetider i cancervården. Överenskommelse mellan staten och Sveriges Kommuner och Landsting 2016.
Socialdepartementet och SKL. (2017). Kortare väntetider i cancervården. Överenskommelse mellan staten och Sveriges Kommuner och Landsting 2017.
Socialdepartementet och SKL. (2018). Kortare väntetider i cancervården. Överenskommelse mellan staten och Sveriges Kommuner och Landsting 2018.
Socialdepartementet och SKL. (2019). Kortare väntetider i cancervården. Överenskommelse mellan staten och Sveriges Kommuner och Landsting 2019.
Socialdepartementet och SKR. (2020). Jämlik och effektiv cancervård med kortare väntetider 2020. Överenskommelse mellan staten och Sveriges Kommuner och Regioner.
Socialdepartementet och SKR. (2021). Jämlik och effektiv cancervård med kortare väntetider 2021. Överenskommelse mellan staten och Sveriges Kommuner och Regioner.
Socialdepartementet och SKR. (2022). Jämlik och effektiv cancervård med kortare väntetider 2022. Överenskommelse mellan staten och Sveriges Kommuner och Regioner.
Socialdepartementet och SKR. (2023). Jämlik och effektiv cancervård med kortare väntetider 2023. Överenskommelse mellan staten och Sveriges Kommuner och Regioner.
Socialstyrelsen. (2010). Samordning av canceruppdrag inom ramen för den nationella cancerstrategin. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2013). Nationellt kunskapsstöd för god palliativ vård i livets slutskede. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2015). Standardiserade vårdförlopp i cancervården. En baslinjestudie. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2018). Nationella riktlinjer för prevention och behandling. Stöd för styrning och ledning.
Socialstyrelsen. (2023). Statistikdatabasen. Cancerregistret. https://sdb.socialstyrelsen. se/if_can/val.aspx. [hämtat 2022-12-20].
Socialstyrelsen. (2011a). Öppna jämförelser av cancervårdens kvalitet och effektivitet – jämförelser mellan landsting 2011. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2014a). Uppföljning av regionala cancercentrum 2013. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2014b). Modell för bedömning, införande och uppföljning av nationella screeningprogrammet på cancerområdet. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2014c). Väntetider i cancervården. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2014d). Screening för tjock- och ändtarmscancer: Rekommendation och bedömningsunderlag. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2015a). Uppföljning av regionala cancercentrum 2014 – Uppbyggnad, styrkor och utmaningar. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2015b). Väntetider i cancervården. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2016a). Uppbyggnaden av regionala cancercentrum – En samlad bedömning från fyra års uppföljning. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2016b). Uppföljning av regionala cancercentrum 2015 – Förebyggande insatser, tidig upptäckt, klinisk forskning och innovation. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2017). Uppföljning av regionala cancercentrum 2016 – Nivåstrukturering och vårdprocesser. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2019a). Väntetider, patientperspektiv och strävan mot en jämlik vård. Effekter av satsningen på standardiserde vårdförlopp i cancervården 1. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2019b). Om lärande, prioriteringar och ekonomiska aspekter. Effekter av satsningen på standardiserade vårdförlopp i cancervården 2. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2019c). Framtidens cancerscreening. Stockholm: Socialstyrelsen. Socialstyrelsen. (2020a). Nationell utvärdering livmoderhalsscreening. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2020b). Standardiserad dokumentation kring cancerpatienter – delrapport 2020. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2021a). Dataanalyser av cancer 1975–2019. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2021b). Utveckling av den statligt nationella samordningen och uppföljningen av cancervården. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2021c). Standardiserad dokumentation kring cancerpatienter – slutrapport. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2021d). Analys av utvecklingen vid Regionala cancentrum. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2021e). Uppföljning och analys av Regionala cancercentrums arbete med standardiserade vårdförlopp och insatser inom barncancerområdet 2021. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2022a). Nationellt och regionalt arbete med standardiserade vårdförlopp 2022. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2022b). Cancerrehabilitering förslag till utveckling 2022. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2022c). Mot en mer samordnad cancerscreening. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2022d). Nationell utvärdering –bröstcancerscreening med mammografi. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2023a). Analys av utvecklingen vid regionala cancercentrum. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2023b). Cancerregistret. https://www.socialstyrelsen.se/statistik-och- data/register/cancerregistret/. [hämtat 2023-05-30].
Socialstyrelsen. (2023c). Delredovisning av uppdraget att samordna det nationella arbetet med att genomföra EU:s cancerplan. Stockholm: Socialstyrelsen.
Socialstyrelsen. (2023d). Läkemedelsförsäljning i Sverige – analys och prognos 2023– 2026. Stockholm: Socialstyrelsen.
SOU 2009:11. En nationell cancerstrategi för framtiden. Stockholm: Socialdepartementet. SOU 2017:4. För en god och jämlik hälsa – en utveckling av det folkhälsopolitiska ramverket. Stockholm: Socialdepartementet.
SOU 2017:47. Nästa steg på vägen mot en mer jämlik hälsa – slutbetänkande. Stockholm: Socialdepartementet.
SOU 2019:29. God och nära vård. Vård i samverkan. Stockholm: Socialdepartementet.
SOU 2023:83. Samordnat juridiskt stöd och vägledning för hälso- och sjukvårdens digitalisering. Stockholm: Socialdepartementet.
SOU 2023:76. Vidareanvändning av hälsodata för vård och klinisk forskning. Stockholm: Socialdepartementet.
Statskontoret. (2015). Utvärdering av regeringens strategi för alkohol-, narkotika-, dopnings- och tobakspolitiken. Stockholm: Statskontoret.
Statskontoret. (2018). Strategier och handlingsplaner. Ett sätt för regeringen att styra? Stockholm: Statskontoret.
Statskontoret. (2020). Utvärdering av En arbetsmiljöstrategi för det moderna arbetslivet 2016–2020 Stockholm: Statskontoret.
Statskontoret. (2023). Kunskapssammanställning om nationella strategier. Stockholm: Statskontoret.
Sveriges Kommuner och Regioner. (2023). Vården i siffror. Tillgänglig på: https:// vardenisiffror.se.
Sveriges regioner i samverkan. (2021). Generisk modell för rehabilitering. Nationellt system för kunskapsstyrning.
TLV. (2018). Uppföljning av läkemedelsanvändning och behandlingseffekter i klinisk vardag. Stockholm: Tandvårds- och läkemedelsförmånsverket.
TLV. (2020a). Uppföljning av cancerläkemedel och andra läkemedel via alternativa datakällor. Stockholm: Tandvårds- och läkemedelsförmånsverket.
TLV. (2020b). TLV:s uppdrag att genomföra hälsoekonomiska bedömningar av medicintekniska produkter. Rapport till Socialdepartementet. Stockholm: Tandvårds- och läkemedelsförmånsverket.
TLV. (2021a). Utvecklad uppföljning med hjälp av data från exempelvis nationella tjänsteplattformen. Stockholm: Tandvårds- och läkemedelsförmånsverket.
TLV. (2021b). Hur ska vi utvärdera och hur ska vi betala? Hälsoekonomiska bedömningar och betalningsmodeller för precisionsmedicin och ATMP. Stockholm: Tandvårds- och läkemedelsförmånsverket.
TLV (2022). Beräkning och betalning Fortsatt utredning om utvärderingsmetoder och betalningsmodeller för nya läkemedel som ATMP och precisionsmedicin. Stockholm: Tandvårds- och läkemedelsförmånsverket.
TLV. (2023). Utveckling värdebaserad prissättning. https://www.tlv.se/lakemedelsforetag/ utveckling-vardebaserad-prissattning.html [hämtat 2023-12-18]. Stockholm: Tandvårds- och läkemedelsförmånsverket.
Ung cancer. (2023). Inte längre barn, men inte heller vuxen. Rapport 2023:6 https:// ungcancer.se/wp-content/uploads/2023/11/Ung-Cancer_behovsanalys_summering_ drababde_2023.pdf [hämtat 2023-12-21].
Vinnova. (2022). Uppdrag att etablera en innovationshubb för produktionen av vacciner och andra avancerade läkemedel. Stockholm: Vinnova.
Vinnova. (2023). Delredovisning av uppdrag att stödja genomförandet av regeringens samverkansprogram. Stockholm: Vinnova.
Vinnova. (2018a). Rapport av regeringsuppdrag att bidra till uppbyggnad av en infrastruktur och testbädd som ska utgöra en öppen mötesplats för innovation, utveckling och industrialisering av teknologier för produktion av biologiska läkemedel. Stockholm: Vinnova.
Vinnova. (2018b). Uppdrag att utföra fortsatta insatser avseende digitalisering för bättre hälsa, vård och omsorg. Stockholm: Vinnova.
Vinnova. (2021a). Delredovisning av uppdrag inom life science. Stockholm: Vinnova.
Vinnova. (2021b). Delredovisning av uppdrag att stödja genomförandet av regeringens samverkansprogram samt ge stöd till offentliga aktörers arbete med regel- och policyutveckling. Stockholm: Vinnova.
Vårdanalys. (2016). Ordning i leden? Utvärdering av ordnat införande av nya läkemedel. Rapport 2016:5. Stockholm: Vårdanalys.
Vård- och omsorgsanalys. (2017a). Lapptäcke med otillräcklig täckning. Slututvärdering av satsningen på nationella kvalitetsregister. Rapport 2017:4. Stockholm: Vård- och omsorgsanalys.
Vård- och omsorgsanalys. (2017b). Cancerläkemedel – ett kunskapsunderlag om införande, användning och uppföljning. Rapport 2017:8. Stockholm: Vård- och omsorgsanalys.
Vård- och omsorgsanalys. (2020). Styra mot horisonten. Om vård efter behov som grund för horisontella prioriteringar. Rapport 2020:7. Stockholm: Vård- och omsorgsanalys.
Vård- och omsorgsanalys. (2021a). Genvägen till ökad precision – En framåtblickande analys av precisionsmedicin i hälso- och sjukvården. Rapport 2021:5. Stockholm: Vård- och omsorgsanalys.
Vård- och omsorgsanalys. (2021b). Ledas lika, ledas rätt? Ett kunskapsunderlag om standardiserade vårdförlopp. Rapport 2021:9. Stockholm: Vård- och omsorgsanalys.
Vård- och omsorgsanalys. (2021c). Nära vård i sikte? Utvärdering av omställningen till en god och nära vård: delrapport. Rapport 2021:8. Stockholm: Vård- och omsorgsanalys.
Vård- och omsorgsanalys. (2022). I rätt riktning? Användningen av riktade statsbidrag inom vård och omsorg. Rapport 2022:3. Stockholm: Vård- och omsorgsanalys.
Vård- och omsorgsanalys. (2023a). Kontinuitet och fast läkarkontakt Kartläggning av måluppfyllelsen i överenskommelserna om en god och nära vård. PM 2023:3. Stockholm: Vård- och omsorgsanalys.
Vård- och omsorgsanalys. (2023b). Ordnat för omställning? Utvärdering av omställningen till en god och nära vård: delrapport. Rapport 2023:2. Stockholm: Vård- och omsorgsanalys.
Vård- och omsorgsanalys. (2024). En för alla. (kommande) Stockholm: Vård- och omsorgsanalys.
Wells, Delilovic, Gunnarsson, Dervish, von Knorring, Hasson. (2021). Primary care physicians’ views of standardised care pathways in cancer care: A Swedish qualitative study on implementation experiences. Eur J Cancer Care, 2021;30:e13426.
World Health Organization WHO. (2020). WHO report on cancer: setting priorities, investing wisely and providing care for all.
Åkesson, L., & Tufvesson Stiller, H. (2019). Patientrapporterade erfarenhetsmått i uppföljningen av standardiserade vårdförlopp. Resultat, erfarenheter och lärdomar. RCC sydöst.
Bilaga 1: Generisk intervjuguide
Vi har gjort semistrukturerade intervjuer med utgångspunkt i en generisk intervjuguide, som anpassats utifrån den intervjuades roll.
- Vilka styrkor och svagheter ser du i dagens cancervård (inklusive forskningen)?
- På vilket eller vilka sätt tror du att den svenska cancerstrategin från 2009 har bidragit till eller påverkat dagens cancervård?
- Hur har din organisation bidragit till måluppfyllelsen i cancerstrategin?
- Finns det saker som ni hade velat göra men inte har kunnat göra/uppnå?
- På vilket eller vilka sätt tror du att styrningen av cancervården genom strategin och efterföljande aktiviteter har påverkat hälso- och sjukvården generellt?
- Finns det viktiga lärdomar att dra av styrning genom en nationell strategi?
- Vilka faktorer har underlättat eller hindrat genomförandet/implementeringen av den svenska cancerstrategin?
- Vad hade kunnat göras bättre?
- Är målen i cancerstrategin fortfarande relevanta?
- Har vissa av målen uppnåtts?
- Bör målen bli mer konkreta och mätbara?
- Finns det andra områden som bör lyftas in som mål i cancerstrategin, givet utvecklingen i omvärlden?
- Vilka aktiviteter behövs för att uppnå de fem övergripande målen i cancerstrategin?
- Finns det områden som man borde prioritera framöver som man hittills inte har prioriterat tillräckligt?
- Är strukturerna för styrning och samordning inom cancerområdet ändamålsenliga i dagsläget?
- Finns det områden i behov av internationell eller nationell styrning/samordning som ni anser är förbisedda i dagsläget?
- Ser du trender eller faktorer i omvärlden som aktualiserar någon förändring?
- Föranleder nedanstående faktorer några ändringar av den svenska cancervården och/ eller cancerstrategin?
- EU:s cancerplan
- Comprehensive cancer centers (CCC)
- Ny teknologi
- God och nära vård-omställningen
- Är det något övrigt eller några andra perspektiv gällande den svenska cancervården som du vill skicka med oss?
Bilaga 2. Intervjupersoner
Tabell A. Verksamheter och RCC
| Namn | Roll och verksamhet |
|---|---|
| Cecilia Winberg | Förbundsordförande, Fysioterapeuterna |
| Pia Klernäs | Styrelseledamot i sektionen för onkologisk och palliativ fysioterapi, Fysioterapeuterna |
| Cia Ihre Lundgren | Vice ordförande, Svenska läkaresällskapet |
| Edvard Abel | Centrumföreståndare, CCC Sahlgrenska |
| Ellen Brynskog | Ordförande i Nationella arbetsgruppen för cancerprevention |
| Eva Jolly | Verksamhetsansvarig, CCC Karolinska |
| Gunilla Gunnarsson | F.d. nationell cancersamordnare för SKL och ordförande RCC i samverkan |
| Helena Brändström | Nationell samordnare vårdprogram och standardiserade vårdförlopp, Sveriges kommuner och regioner |
| Karin Mellgren | Ordförande, Nationell arbetsgrupp för barncancerområde |
| Kerstin Carlsson | Ordförande, Riksföreningen för medicinskt ansvariga sjuksköterskor och medicinskt ansvariga för rehabilitering |
| Kjell Ivarsson | Nationell cancersamordnare, Sveriges kommuner och regioner (SKR) |
| Ulrika Berg Roos | Kommunikationsstrateg, Sveriges kommuner och regioner (SKR) |
| Maria Andersson | Specialistsjuksköterska i onkologi, Palliativregistret |
| Marie Nilsson | Vårdutvecklingsledare region Stockholm, CaPrim |
| Pernilla Grillner | Tf. verksamhetschef högspecialiserad barnmedicin, Astrid Lindgrens barnsjukhus |
| Annika McCarthy | Verksamhetschef omvårdnad, omvårdnadsområde högspecialiserad barnmedicin, Astrid Lindgrens barnsjukhus |
| Sara Fredriksson Emrooz | Sakkunnig policy, Lif |
| Dag Larsson | Senior sakkunnig policy, Lif |
| Signe Friesland | Ordförande, Svensk onkologisk förening |
| Silke Engelholm | Verksamhetschef för hematologi, onkologi och strålningsfysik på Skånes universitets- sjukhus (Sus), CCC Skåne |
| Helena Elding | Verksamhetschef, professor VO barnmedicin, Skånes universitetssjukhus |
| Stefan Santén | Verksamhetschef VO kirurgi och gastroenterologi, Skånes universitetssjukhus |
| Sofia A Bergström | Vårdprocesskoordinator och sjukvårdsregional RCC-samordnare, samt ordförande för Sjukvårdsregionalt nätverk för sjuksköterskor inom cancervården för övre gastrointestinal cancer (GI) |
| Ursula Scheibling | Ordförande, Nationella arbetsgruppen, personcentrerat sammanhållet vårdförlopp för palliativ vård |
| Ylva Hellstadius | Verksamhetsutvecklare, Centrum för cancerrehabilitering Sabbatsberg och ordförande, Nationella arbetsgruppen cancerrehabilitering |
Tabell B. Forskare
| Namn | Roll |
|---|---|
| Hans-Olov Adami | Professor emerius, Harvard University och Karolinska institutet |
| Mikael Svensson | Professor i hälsoekonomi, Göteborgs universitet |
| Roger Olofsson Bagge | Professor, Göteborgs universitet och verksamhetschef, avdelningen för bröst- och melanomkirurgi på Sahlgrenska |
Tabell C. Myndigheter
| Namn | Roll och verksamhet |
|---|---|
| Lina Keller | Samordnare för genomförandet av EU:s cancerplan, Socialstyrelsen |
| Katarina Fredriksson | Utredare, Socialstyrelsen |
| Louise Strandendahl | Utredare, Socialstyrelsen |
| Mattias Fredricsson | Avdelningschef, Socialstyrelsen |
| Malin Eklund | Programme Manager, Vinnova |
| Mef Nilbert | Socialstyrelsen, Professor i onkologi vid Lunds universitet |
| Caroline Ekstrand | Programme Manager, Vinnova |
| Jonathan Lind Martins- son | Enhetschef, Tandvårds- och läkemedelsförmånsverket |
| Ida Ahlberg | Samordnare, Tandvårds- och läkemedelsförmånsverket |
| Staffan Arvidsson | Forskningssekreterare, Forte |
Tabell D. Patientorganisationer
| Namn | Roll och verksamhet |
|---|---|
| Ebba Hemmingsson | Ansvarig intressepolitisk expert, Barncancerfonden |
| Sol Engvall | Intressepolitisk expert, Barncancerfonden |
| Margareta Haag | Ordförande, Nätverket mot cancer |
| Maria Stacke | Tematisk rådgivare, Ung cancer |
| Per Wahlstedt | Sakkunnig hälso- och sjukvård och cancervård, Cancerfonden |
| Siri Kautsky | Projektledare – Ung Cancer |
Bilaga 3. Enkätundersökning med patientorganisationer
Enkäten
- Vilken patientorganisation företräder ni?
- Vilka styrkor och svagheter ser ni i dagens cancervård?
- Är det några särskilda förändringar/initiativ som tagits inom ramen för cancerstrategin som varit viktiga ur ert perspektiv? Finns det behov av ytterligare förändringar/ initiativ?
- Är strukturerna för styrning och samordning inom cancervården ändamålsenliga ur ett patientperspektiv? (Exempel på sådana strukturer är RCC, nationella vårdprogram och standardiserade vårdförlopp.)
- Behöver den nationella samordningen eller styrningen av cancervården stärkas? I så fall hur?
- Är det något område i cancerstrategin som bör utvecklas mot bakgrund av kommande utmaningar och möjligheter samt utvecklingen i omvärlden? (Exempelvis teknisk utveckling, utveckling i samhället eller omvärlden.)
- Hur ser ni på cancerstrategins mål? Bör målen i strategin vara mer konkreta och mät- bara? Om ja, har ni exempel på hur?
- Är det något annat ni vill framföra till oss?
Deltagande organisationer
| Patientorganisationer |
|---|
| Blåscancerförbundet |
| Bröstcancerförbundet |
| Hjärntumörföreningen |
| Tarm-, uro- och stomiförbundet (ILCO) |
| Lungcancerföreningen |
| Melanomföreningen |
| Nätverket mot gynekologisk cancer |
| Prostatacancerförbundet |
| Sarkomföreningen |
| Ung cancer |
Bilaga 4. Frågor till regionala cancercentrum (RCC)
Frågor
Utgå från det RCC ni företräder, och vården i de regioner där ert RCC verkar.
- Vi har uppfattat att ert mandat/uppdrag i huvudsak kommer från de nationella överenskommelserna. Utöver det, i vilken utsträckning styrs er verksamhet av beslut av den/de regioner där ni verkar och era egna beslut?
- Anser ni att de nationella strukturerna för styrning och samordning inom cancervården (inkl. forskning) är ändamålsenliga? – Vilka styrkor och svagheter ser ni?
- Ser ni behov av ytterligare stöd i ert arbete från någon aktör på nationell nivå?
- Beskriv samordningen och arbetsfördelningen mellan de sex RCC. Vilka styrkor och svagheter ser ni?
- Beskriv ert samarbete med de regioner och kommuner som finns inom ert område. Vilka styrkor och svagheter ser ni?
- Hur har ni arbetat med nivåstrukturering av vården i de regioner där ert RCC verkar?
- Vilka är hindren för implementering av RCC:s kunskap i regionerna och i verksamheterna där ert RCC verkar?
- Inom vilka områden ser ni störst behov av insatser för att stärka cancervården? (till exempel delar av vårdkedjan eller förutsättningar för vården.)
- Vår bild är att det på några områden finns relativt få konkreta aktiviteter i cancerstrategin och i överenskommelserna. Det gäller framför allt kompetensförsörjning, jämlikhet mellan grupper, primärprevention och palliativ vård. Delar ni den bilden? Vad skulle kunna göras för att stärka dessa områden?
- Hur ser ni på cancerstrategins mål? Vilka fördelar och nackdelar ser ni med att göra målen mer konkreta och mätbara?
- Är det något område i cancerstrategin som bör utvecklas mot bakgrund av kommande utmaningar och möjligheter samt utvecklingen i omvärlden? (till exempel teknisk och medicinsk utveckling, demografisk utveckling eller organisatoriska och strukturella förändringar, som resurs- och kompetenstillgång eller EU-initiativ.)
- Är det något övrigt eller några andra perspektiv gällande den svenska cancervården eller cancerstrategin som ni vill framföra?
- OM tillämpligt: Beskriv rollfördelningen mellan RCC och CCC i er
- Vilka beslut om samordning eller rollfördelning mellan RCC och CCC har fattats regionalt eller nationellt?
- Ser ni några behov av förtydliganden av rollfördelningen eller andra förändringar?
Deltagande organisationer
| RCC |
|---|
| RCC Mellansverige |
| RCC Sydöst |
| RCC Syd |
| RCC Norr |
| RCC Stockholm Gotland |
Bilaga 5. Deltagare resultatseminarium
| Namn | Verksamhet |
|---|---|
| Anna-Lena Sunesson | Regionalt cancercentrum Norr |
| Cecilia Hultstrand | Nationella arbetsgruppen för cancerprevention |
| Ebba Hemmingsson | Barncancerfonden |
| Eva Jolly | Karolinska Comprehensive Cancer Center |
| Helena Brändström | Sveriges kommuner och regioner |
| Jeanette Winterling | Karolinska Comprehensive Cancer Center |
| Karin Mellgren | Drottning Silvias barn- och ungdomssjukhus |
| Kjell Ivarsson | Sveriges kommuner och regioner |
| Lina Keller | Socialstyrelsen |
| Maria Stacke | Ung cancer |
| Mef Nilbert | Socialstyrelsen |
| Per Wahlstedt | Cancerfonden |
| Roger Olofsson Bagge | Sahlgrenska universitetssjukhuset |
| Sara Fredriksson Emrooz | Lif |
| Ursula Scheibling | Nationell arbetsgrupp palliativ vård |
Bilaga 6. Den svenska cancerstrategin i internationell jämförelse
Många länder har en nationell strategi eller plan inriktad på cancer. Vi har gjort en översyn av cancerstrategier och cancerplaner i övriga Norden samt Storbritannien, Tyskland, Nederländerna och Frankrike. Av dessa har Norge, Danmark, Frankrike, Skottland, Wales och England nationella cancerstrategier eller cancerplaner som tagits fram senare än den svenska cancerstrategin. Vi har särskilt undersökt den norska cancerstrategin, som är den senaste cancerstrategin i de nordiska länderna och därför kan vara särskilt relevant för Sverige. Vi har också undersökt vilka rekommendationer som WHO har gett i sin senaste rapport kring nationella cancerplaner.
Nyare cancerstrategier jämfört med svenska cancerstrategin
Övergripande finns stora likheter mellan de olika ländernas cancerstrategier och den svenska strategin. En skillnad är dock att flera andra länders strategier ställer upp mer konkreta mål, som ibland även är tidsatta.
Strategierna har liknande utgångspunkter
En central utgångspunkt för strategierna i samtliga länder är behovet av att möta det ökande antalet cancerfall och den ökande överlevnaden som innebär att fler människor lever med cancer (Independent Cancer Taskforce 2015; Regeringen Danmark 2016; Scottish Government 2016; Helse- og omsorgsdepartementet 2018; NHS England 2019; Institut national du cancer 2021).
De övergripande målen för de nyare cancerstrategierna liknar generellt de fem målen för den svenska cancerstrategin. Samtliga har ökad överlevnad och prevention bland sina övergripande målsättningar. Merparten ställer också upp mål kring personcentrering, cancerpatienters livskvalitet samt jämlikhet mellan grupper i befolkningen.
Strategierna presenterar ofta liknande typer av åtgärder, även om länderna ligger olika långt fram med de olika åtgärderna. Åtgärderna är främst inriktade på personcentrering, förebyggande, tidig upptäckt, kompetensförsörjning och kapacitet. De nyare strategierna berör medicinsk teknologi som tillkommit sedan 2009, men grundfrågorna om tillgång, kompetens och kostnad som diskuterades i SOU 2009:11 kopplat till utvecklingen inom medicinteknik och läkemedel återkommer även i de nyare strategierna.
Skillnader i upplägg och innehåll
Det finns olika vägval kring hur man lagt upp nationella cancerstrategier, till exempel om strategin hålls bred eller inriktas på särskilt prioriterade områden, och hur konkreta målen är. Flera cancerstrategier kombinerar ett fåtal mer övergripande mål med ett större antal mer specifika målsättningar inom de olika områdena. Det finns också exempel på att man valt att inte avgränsa strategin till endast cancer. I exempelvis England beslutade regeringen 2023 att istället för att uppdatera cancerstrategin låta cancer ingå i en nationell strategi för 6 stora folksjukdomar (Department of Health and Social Care 2023b).
Något som betonas tydligare i flera nyare strategier från andra länder är att cancerpatienter och canceröverlevare allt oftare är äldre, vilket har implikationer kring till exempel samsjuklighet och livssituation och ställer krav på förändringar i vården (Independent Cancer Taskforce 2015; Scottish Government 2016; Helse- og omsorgsdepartementet 2018). Det finns även exempel på att olika befolkningsgruppers behov betonas mer, exempelvis särskilda behov hos personer med neuropsykiatrisk funktionsnedsättning (Independent Cancer Taskforce 2015) eller etniska minoriteter (Helse- og omsorgsdepartementet 2018).
Den norska cancerstrategin
Eftersom Norge är det nordiska land som senast uppdaterade sin nationella cancerstrategi har vi tittat närmare på den norska strategin, som kom 2018. Den norska cancerstrategin ställer upp fem övergripande mål om förebyggande, patientorientering, välfungerande vårdprocesser, överlevnad och livskvalitet, samt 30 mer konkreta delmål. Vissa av delmålen är mer allmänt hållna, exempelvis att cancerpatienter ska kunna medverka i beslut kring behandling och uppföljning. Andra är mer specifika, som att minska för tidig död orsakad av icke-smittsamma sjukdomar med en tredjedel till 2030. (Helse- og omsorgsdepartementet 2018)
Strategin beskriver att antalet cancerfall kommer att fortsätta öka, och att allt fler av de som får cancer är äldre. Detta ställer enligt strategin krav på kapacitet, kompetens och effektivitet. Vikten av förebyggande betonas också särskilt. Den nationella strategin för förebyggande av de fyra största icke-smittsamma folksjukdomarna pekas ut som central för cancerprevention. Fler cancerfall tillsammans med förbättrade behandlingar innebär också att allt fler lever med cancer. Den norska strategin betonar den vård som sker efter cancerbehandlingen, exempelvis övergången till primärvården och vikten av att ha ett brett perspektiv på canceröverlevares livskvalitet.
Utvecklingen inom diagnos och behandling medför enligt strategin att det kommer att ske en allt större individanpassning utifrån biologiska egenskaper, och att kostnaderna för nya behandlingar ökar. När behandlingarna blir mer kunskapskrävande behövs ökad specialisering. En stor del av de nya cancerläkemedlen har också otillräckligt dokumenterad effekt på överlevnad och livskvalitet. I ljuset av detta är det enligt strategin viktigt dels att säkra tillgång till den nya teknologin, dels att upprätta ett system för bedömning och uppföljning av nytta, kostnader och risker med nya behandlingar.
Uppdateringar av WHO:s rekommendationer
World Health Organization (WHO) rekommenderar att länder använder sig av nationella planer mot cancer. I den senaste WHO-rapporten ”Report on Cancer” från 2020 beskrivs flera utvecklingstendenser inom cancerområdet och man ger rekommendationer om vad cancerplaner bör inkludera.
Till att börja med lyfter man fram att det skett enorma framgångar inom cancer- behandlingar senaste 50 åren. Vissa nya behandlingar har signifikant påverkan på överlevnad och livskvalitet, men många av de nyaste behandlingarna har bara marginellt bättre effekt än äldre behandlingar. Kostnaden för läkemedel och medicinska teknologier beskrivs som ett av de främsta hoten mot fungerande cancerkontroll. WHO har definierat prioriterade interventioner till stöd för beslut kring nya medicinska tekniker och läkemedel. Palliativ vård och uppföljning av canceröverlevare bör enligt WHO ingå i cancerplaner. WHO pekar också på förbättrade möjligheter till lärande genom att koppla samman datakällor med individbaserade data. Cancercentrum beskrivs som viktiga knutpunkter för ökad kapacitet och effektivitet på cancerområdet.
WHO betonar i rapporten vikten av att prioritera primärprevention och tidig upptäckt. Det handlar om att motverka tobak, införa vaccinprogram mot HPV och hepatit B samt arbeta med övervikt, alkohol, arbetsmiljö och luftkvalitet. Dessutom bör man öka kunskapen hos befolkningen och se till att det finns kapacitet för snabb diagnos. Höginkomstländer bör prioritera screening av livmoderhalscancer, bröstcancer och tjock/ändtarmscancer.
WHO argumenterar för att nationella cancerplaner behöver prioritera insatser med utgångspunkt i förväntad effekt, kostnad och genomförbarhet. Aktiviteter, menar man, bör tidssättas och utvärderas. Slutligen betonar WHO att det är viktigt att hela kedjan för implementering av cancerplanen finns på plats. Saknas en länk, till exempel personal i viss del av vårdkedjan, skapas lidande för patienter och slöseri med resurser.
Beslut
Beslut om denna promemoria har fattats av generaldirektören Jean-Luc af Geijerstam. Utredaren Kajsa Hanspers har varit föredragande. Analyschefen Caroline Olgart Höglund, chefsjuristen Catarina Eklundh Ahlgren och projektdirektören Johan Strömblad har deltagit i den slutliga handläggningen.
